Sommaire du cours de Physiologie Animale.
P1 : Homéostasie.
P2 : Régulation de la calcémie.
P7 : Le système nerveux central.
P18 : Le système nerveux végétatif.
P21 : La digestion.
P42 : Circulation.
P52 : Respiration.
P55 : Les échanges gazeux.
P58 : L’excrétion.
P64 : L’appareil génital mâle.
P69 : L’appareil génital femelle.
P76 : Le problème hypothalamo-hypophysaire.
P83 : Absorption digestive.
Chapitre 1 : Homéostasie et Régulation Calcique .
Notion d’homéostasie
L’homéostasie est la faculté que possède un organisme de maintenir les équilibres de son milieu intérieur de façon stable et indépendante des fluctuations du milieu extérieur.
Détecter les changements intérieurs ou extérieurs, par le versant sensoriel (ou afférent) permet l’acquisition des informations.
L’intégration de ces informations (par le système nerveux central) se fait sur plusieurs niveaux : - niveau réflexe (moelle épinière) – niveau supérieur (système nerveux supraspinal).
Déclencher les réponses adaptées : c’est le rôle du versant moteur :
Le système nerveux somatique agit uniquement sur les muscles squelettiques
Le système nerveux végétatif (ou autonome) agit sur les muscles lisses, cœur et glandes.
Le système endocrinien.
Remarque : certaines cellules endocriniennes sont sensibles et n’ont pas besoin du système nerveux.
Régulation de la calcémie
La calcémie est la concentration de calcium plasmique (100 mg/L). Ce calcium est un constituant fondamental. Le calcium :
- assure la rigidité du squelette en formant la partie rigide des os en participant à la formation de l’hydroxyapatite,
- agit sous forme ionisée (Ca2+) dans plusieurs fonctions (contractions musculaires, transmission synaptique, coagulation sanguine),
- a un rôle de second messager dans les cellules.
La régulation du calcium est stricte, et sa valeur n’est modifiée qu’autour de 3% par rapport à la valeur moyenne. On trouve trois hormones de régulation :
- la parathormone (PTH),
- la vitamine D2 activée,
- la calcitonine.
I Distribution du calcium dans l’organisme.
Dans le hyaloplasme, la concentration en Ca est de 0,1 µM. Ce calcium est stocké dans les membranes cellulaires, dans le réticulum endoplasmique et dans les mitochondries. Sous l’influence de certains stimuli, la concentration de calcium augmente jusqu’à 100 fois.
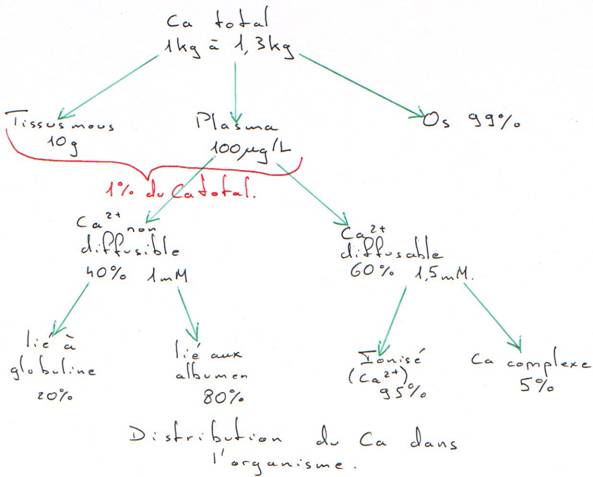
II Les mouvements calciques.
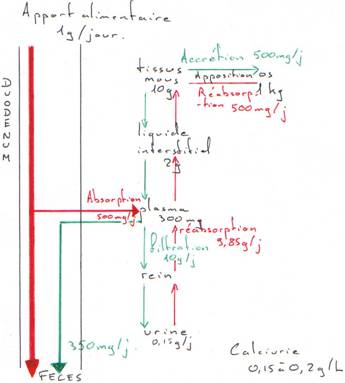
On a trois organes qui sont soumis à la régulation hormonale : le tissu inerte, le tube digestif et les reins.
III La parathormone (PTH).
A Synthèse.
La parathormone est synthétisée et sécrétée par quatre petites glandes de la thyroïde, la parathyroïde dont le poids total est de 120 mg.
La parathormone a une courte durée de vie (inférieure à 20 minutes).
Après une ablation totale de cette glande, si l’on réinjecte des extraits parathyroïdiens, on assiste à une augmentation de la calcémie. La PTH est une hormone hypercalcémiante.
C’est une protéine ayant deux précurseurs : la préproparathormone et la proparathormone.
La synthèse de PTH dépend de la calcémie :
- Quand la calcémie est inférieure à 120 µg/L, la synthèse de PTH augmente,
- Quand la calcémie est supérieure à 100 µg/L, la synthèse de PTH diminue.
Remarque : le niveau de PTH est toujours proche du niveau normal.
La glande parathyroïde sécrète la PTH qui va réguler la calcémie. Cette dernière va exercer un rétrocontrôle (ou feedback) sur la sécrétion de PTH.
B Effets.
Dans le sang, la parathormone se fixe sur les récepteurs membranaires des cellules cibles.
- Au niveau des os : en augmentant, la parathormone va permettre la résorption de Calcium.
- Au niveau des reins : une augmentation de la réabsorption calcique sur les tubules rénaux entraîne une diminution de l’excrétion rénale
- La stimulation enzymatique rénale est à l’origine du passage de la vitamine D3 en calcitriol.

- Au niveau du duodénum, la parathormone favorise l’absorption.
C Effets d’un déséquilibre.
· Carences en PTH : on obtient une tétanie à cause d’une hyperexcitabilité neuromusculaire. On peut avoir des spasmes pharyngés qui provoquent l’asphyxie.
· Excès en PTH : C’est une super sécrétion de parathormone qui entraîne donc une grande décalcification osseuse (à ostéomalacie) et parfois une augmentation de la calciurie.
IV La vitamine D3 (calciférol).
A Synthèse.
Chez les mammifères, la synthèse de la vitamine D3 a lieu dans les tissus cutanés profonds, à partir d’un précurseur thyroïdien (7-déhydrocholestérol)
Grâce aux UV, le 7-déhydrocholestérol donne de la vitamine D3 non active. Cette dernière est transportée vers le foie par la vitamine D3 binding protéine. Dans le foie, elle subit une première hydroxydation ( 25(OH)-D3 = calcidiol). Le calcidiol subit une seconde hydroxydation dans le rein, régulée par la parathormone, et donne le 1,25(OH)D3 (ou calcitriol).
25(OH)-D3 = calcidiol). Le calcidiol subit une seconde hydroxydation dans le rein, régulée par la parathormone, et donne le 1,25(OH)D3 (ou calcitriol).
B Effets.
· L’activation de la réabsorption osseuse entraîne une augmentation de la calcémie.
· L’intestin favorise l’absorption de calcium grâce à la perméabilité des tubules intestinaux.
· L’hormone qui active le transport intracellulaire du calcium pour la synthèse d’une protéine est la binding protéine (entérocyte) : c’est une hormone hypercalcémiante.
C Effets d’un déséquilibre.
Une carence en vitamine D3 entraînera chez les enfants du rachitisme et de l’ostéomalacie chez l’adulte.
Si la quantité de vitamine D3 diminue, on a alors une diminution de la calcémie qui entraîne une augmentation de sécrétion de parathormone, qui rétablira la calcémie en puisant dans le calcium osseux.
Un excès de vitamine D3 entraîne une augmentation de la calcémie et, par conséquent, des dépôts de calcium au niveau des reins.
V Calcitonine.
A Synthèse.
La calcitonine est une hormone sécrétée par les cellules parafoliculaires (cellules C) (cellules de la thyroïde) et, de moindre part, par la parathyroïde et le thymus.
Cette hormone est un polypeptide de 32 acides aminés dont la durée de vie est inférieure à 15 minutes. Son précurseur est composé de 136 acides aminés. C'est la seule hormone qui agit sur l'ostéoblaste de manière directe, importante, mais de façon transitoire pour diminuer la résorption osseuse : elle diminue le calcium sérique in vivo. C'est un antagoniste physiologique de la PTH.
La calcitonine a un rôle hypocalcémiant.
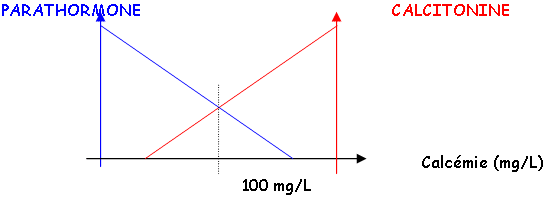
B Effets.
Au niveau des os : la calcitonine diminue la résorption osseuse. Il faut rappeler qu'actuellement, le rôle précis de la calcitonine endogène sur le métabolisme de l'os n'est pas clairement établi.
C Effets d’un déséquilibre.
Elle ne provoque aucun effet durable. C’est une hormone surtout utilisée en traitement de l’ostéoporose.
VI Autres hormones.
A Les hormones thyroïdiennes.
Elles agissent sur le remaniement osseux dans les deux sens bien leur action sur la résorption soit plus importante (hypercalcémique).
B Les œstrogènes.
Ils sont hypocalcémiants à court terme. Ils diminuent la sensibilité de l’os à la parathormone : ils augmentent donc la rétention osseuse.
C Les glucocorticoïdes.
Ils ont un rôle hypocalcémiant par leur diminution :
- de l’absorption osseuse
- des résorptions osseuses et rénales.
Quand ils sont sécrétés en excès, ils entraînent une ostéoporose.
D L’hormone de croissance.
Pas de rôle prépondérant.
Chapitre 2 :"Les Systèmes Nerveux".
Le système nerveux central
I Organisation du système nerveux.
Il est globalement bilatéral et symétrique et est composé en deux parties :
- Le système nerveux central se trouve dans les structures osseuses et est formé par la moelle épinière et par l’encéphale.
- Le système nerveux périphérique est formé de ganglions et de nerfs. Ces nerfs contiennent des faisceaux de fibres reliées à la base de l’encéphale par les douze paires de nerfs crâniens et à la moelle épinière par les 31 paires de nerfs rachidiens (ou spinaux).
Les fibres allant de la périphérie vers le système nerveux central sont appelées fibres sensorielles afférentes.
Les fibres transportant l’information du système nerveux central vers les effecteurs de la périphérie sont les nerfs moteurs efférents.
On subdivise le système nerveux périphérique en deux composantes :
- Le système nerveux périphérique somatique reçoit des fibres sensorielles en provenance d’organes sensoriels variés : de la peau, des muscles, des articulations. Il regroupe aussi les fibres motrices primaires (principalement) des muscles.
- Le système nerveux périphérique autonome (ou végétatif) : ses fibres innervent les muscles lisses, le cœur et les glandes.
Le système nerveux périphérique fournit l’information au système nerveux central et exécute les commandes motrices de celui-ci.
A Les grandes subdivisions du système nerveux central.
Le système nerveux central est découpé en 7 parties principales.
1 La moelle épinière.
Les neurones sensoriels des nerfs rachidiens arrivent à la moelle épinière par les racines dorsales (31 paires de nerfs rachidiens) où leur corps cellulaire se situe dans les ganglions rachidiens (ou spinaux) de la racine dorsale.
Les neurones quittent la moelle épinière par la racine ventrale et leur corps cellulaire se situe dans la moelle épinière.
La moelle se subdivise en plusieurs parties et elle est limitée au niveau de la première vertèbre lombaire.
Toutes les fibres nerveuses myélinisées se situent à l’extérieure de la moelle et forment la substance blanche.
La substance blanche est constituée de fibres de deux types :
- Les fibres sensorielles afférentes qui se regroupent en faisceaux (voies). Ce sont des voies ascendantes qui amènent les informations de la périphérie vers le cerveau.
- Les fibres motrices sont descendantes et regroupées en voies descendantes. Elles transportent les commandes motrices issues du cerveau par les neurones moteurs.
2 Le myélencéphale (bulbe rachidien).
Il contient de nombreux noyaux et faisceaux. On y trouve les centres nerveux responsables des fonctions autonomes (ou végétatives) qui contrôlent les rythmes cardiaque, pulmonaire et même la digestion.
3 et 4 Le métencéphale.
Il est constitué de deux structures : le pont et le cervelet.
- Le pont contient le centre des fonctions autonomes (et les noyaux moteurs).
- Le cervelet est relié au système nerveux central par les pédoncules cérébelleux. Il a un rôle dans la coordination de la fonction motrice et de l’équilibre.
5 Le mésencéphale.
Il contrôle le mouvement des yeux et de la motricité générale. C’est un centre de relais des informations visuelles et auditives. C’est un centre qui permet aux mal-voyants de faire certaines activités.
Remarque : le mésencéphale plus le pont plus le bulbe donne le tronc cérébral. C’est à ce niveau qu’arrivent les 12 paires de nerfs crâniens. Ces nerfs transmettent les informations motrices et sensorielles de la tête et du cou et les informations sensori-motrices qui viennent du système nerveux périphérique autonome.
Liste des douze nerfs crâniens :
- 1 : olfactif (sensoriel)
- 2 : optique
- 3 : oculomoteur
- 4 : trodléaire
- 5 : trijumeau
- 6 : abducens
- 7 : fascial
- 8 : vestibulochochléaire
- 9 : glosso-pharyngien (mixte)
- 10 : vague ou pneumogastrique (mixte)
- 11 : spinal
- 12 : hypoglosse.
Les formations réticulées, au niveau du tronc cérébral forment un ventre où se situe la vigilance qui caractérise le niveau d’éveil, du sommeil, de l’attention de l’individu.
6 Le diencéphale.
Le diencéphale comprend deux structures :
- Le thalamus est constitué de nombreux noyaux de relais qui traitent la plupart des informations sensorielles qui atteignent le cortex cérébral.
- L’hypothalamus contient de nombreux noyaux relais qui régulent le système nerveux périphérique autonome et la sécrétion d’hormones grâce à l’hypophyse.
A cause de ces fonctions, l’hypothalamus intervient dans un grand nombre de fonctions de l’organisme (dans presque toutes).
7 Le télencéphale.
Il est principalement constitué du cortex cérébral (la substance grise de l’encéphale) et de la substance blanche sous jacente à ce complexe. On distingue différentes parties :
- Le striatum : il fait parti d’un ensemble de centres nerveux, de noyaux gris qui jouent un rôle dans la régulation des mouvements. Le striatum contient deux parties, les noyaux codés et le putamen.
- L’hippocampe ; il jouerait un rôle dans la mémoire.
- L’amygdale joue un rôle dans l’émotivité et coordonne les systèmes nerveux et endocriniens.
Remarque : L’hippocampe et l’amygdale forment le système limbique.
8 Le cortex cérébral.
Le cortex cérébral s’est développé chez les primates et s’est énormément plissé chez l’homme. On y observe des sillons (scissures plus ou moins profondes) qui délimitent des circonvolutions (ou gyrus) cingulaires. Ces sillons délimitent quatre lobes cérébraux : le lobe occipital, le lobe pariétal, le lobe frontaltemporal. et le lobe
Remarque : Le lobe limbique : les neurones forment un circuit complexe et participent à la motivation, à la mémoire et aux émotions.
Les lobes sont divisés en aires fonctionnelles qui seront impliquées dans le traitement des informations sensorielles ou des activités motrices.
· Les aires corticales primaires :
- sensorielles : elles reçoivent les informations sensorielles après quelques relais et sont consacrées au traitement initial de l’information (visuelle, auditive, somesthésique). Ces aires se situent au niveau du sillon de Rolando.
- Motrices (une aire motrice dans chaque hémisphère) : elles contiennent des neurones qui vont directement agir sur les motoneurones de la moelle épinière, donc sur le mouvement. Ces aires se situent en avant du sillon de Rolando.
· Les aires corticales d’ordre supérieur
- sensorielles : elles reçoivent les informations des aires primaires correspondantes et vont intégrer et traiter ces informations sur un aspect plus complexe dans les lobes temporaux et pariétaux.
- Motrices : elles sont dans le lobe frontal, en avant des aires motrices primaires et envoient à ces aires motrices primaires des informations élaborées nécessaires à l’exécution d’un acte moteur.
· Les aires corticales d’association
Elles sont en majeure partie dans le cortex et entourent les aires d’ordre supérieur.
- sensorielles : elles intègrent les informations des différents systèmes sensoriels. Elles permettent des perceptions complexes. Elles se situent dans les lobes temporaux et pariétaux.
- Motrices : elles sont dans le lobe frontal et jouent un rôle dans la planification des mouvements volontaires.
- Limbique : elle est consacrée à la motivation à la mémoire et aux émotions.
è Les aires primaires du cortex sont consacrées à la réception et à la perception sensorielle. Elles se projettent sur les aires d’ordre supérieur qui se connectent avec les aires d’association, elles-même connectées avec les aires motrices (action sur les motoneurones, donc sur le mouvement) è d’où un lien entre sensation et action.
B Organisation en systèmes fonctionnels.
1 Conduite simple.
Les aires associatives ont besoin d’informations visuelles, sur la forme, la dimension, la texture et le mouvement de l’objet mais aussi d’informations somesthésiques comme la position des membres dans l’espace.
Ces différentes informations permettent alors d’agir en fonction de la trajectoire.
Les informations sensorielles vont planifier les différentes commandes motrices, qui sont transmises au système moteur primaire qui va coordonner les muscles pour un mouvement fin de la main et du bras et réguler la posture du corps pour pouvoir maintenir l’acte moteur.
Pour initier un mouvement, il faut l’intervention des systèmes de motivation (système limbique) qui sont capables d’intégrer de nombreuses informations sur l’état intérieur de l’organisme en fonction desquelles ils influencent le système moteur (somatique et autonome).
2 Organisation des systèmes fonctionnels.
L’organisation suit quatre principes.
a
Chaque système comprend des centres relais organisés en voies afférentes (sensorielles) et efférentes (motrices). On a une organisation hiérarchique ou séquentielle. Les neurones se relaient au niveau d’hyper structures du système nerveux central : noyaux de relais (moelle épinière plus encéphale).
Au niveau des noyaux de relais, l’information commence à être intégrée.
Remarque : les interneurones vont permettre une modification de l’information.
b Les voies distinctes parallèles.
Les systèmes sensoriels (visuels) possèdent des voies séparées différentes et parallèles pour traiter les textures, formes, tailles, couleurs afin de définir des mouvements adéquats.
On a la même chose pour le système moteur qui permet un contrôle précis des mouvements ou de la posture.
c Organisation topographique.
L’arrangement spatial des cellules réceptrices sensorielles est préservé tout au long des voies sensorielles.
Pour le système somesthésique, deux cellules vont se projeter au niveau du thalamus, puis au niveau du lobe cortical.
La carte topographique du corps est réalisée selon les différents niveaux de traitement jusqu’au cortex : c’est la somatotopie (organisation en système).
La plupart des systèmes fonctionnels croisent la ligne médiane du corps.
d Croisement de la ligne médiane.
Toutes les voies sont symétriques par rapport à la ligne médiane du corps et presque toutes la croisent vers le côté opposé (centre latéral) à différents niveaux  c’est la décussation.
c’est la décussation.
L’information sur un côté sera traitée par l’hémisphère opposé. Les mouvements volontaires prennent naissance du côté opposé à leur côté d’action.
II Les systèmes sensoriels.
Ils sont issus des organes sensoriels de la périphérie. On a d’abord la sensation puis la perception des informations au niveau cortical.
A Principes généraux.
1 Principales modalités sensorielles.
- vision
- audition
- olfaction
- gustation
- somesthésie
- équilibrage
Chaque modalité comporte des sous modalités. Avec la gustation, on trouve comme sous modalités les sensations de sucré, de salée, d’amer et d’acide.
2 Organisation des systèmes sensoriels.
Dans chaque système sensoriel, la sensation apparaît quand les facteurs environnementaux stimulent les cellules correspondantes à une modalité. Les cellules nerveuses, spécialisées, sont appelées récepteurs sensoriels.
|
Modalité
|
Stimulus
|
Type de récepteur
|
|
Vision
|
Lumière
|
Photorécepteur
|
|
Audition (équilibration)
|
Ondes de pression
|
Mécanorécepteur
|
|
Gustation et Olfaction
|
Chimique
|
Chémorécepteur
|
|
Somesthésique
|
Mécanique
Thermique
Chimique
|
Mécanorécepteur
Thermorécepteur
Chémorécepteur
|
a Codage de l’information.
Quelque soit la modalité, le sens, une stimulation va provoquer une variation de différence de potentiel transmembranaire du récepteur (potentiel de récepteur). La première étape de codage du stimulus est appelée transduction sensorielle.
On a alors la génération d’un ou plusieurs potentiels d'action qui se propage(nt) sur la première fibre sensorielle (fibre primaire).
b Codage des paramètres de stimulation.
La stimulation est codée en fonction de son intensité, de sa durée et de sa localisation.
· L’intensité est liée à la fréquence de décharge des potentiels d'action.
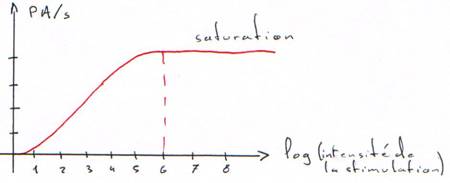
· La durée : les récepteurs s’adaptent tous à une stimulation prolongée (l’adaptation sera lente ou rapide).
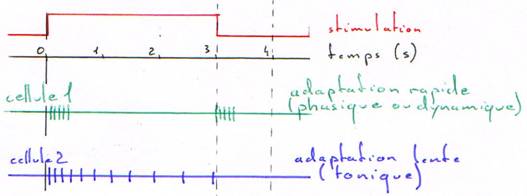
· localisation : chaque cellule peut être activée par un espace sensoriel (ou champ de réception). La taille des ces champs est proportionnelle : plus ils sont petits plus la résolution sera grande.
Les neurones sensoriels primaires convergent vers un second neurone sensoriel (neurone sensoriel secondaire). Ce dernier donne la somme de réception des deux neurones primaires. Les champs ne sont pas tous homogènes.
Les champs hétérogènes vont inhiber le neurone de deuxième ordre.
Plus les champs sont grands, plus ils sont complexes.
Toutes les voies sensorielles préservent les relations spatiales de ces récepteurs.
Somatotopie à Somesthésie. Rétinotopie à Vision. Tonotopie à Audition.
c Les organes des voies sensorielles.
Les informations sont codées puis véhiculées par les voies sensorielles pour atteindre le cortex primaire, aux modalités correspondantes à leur origine. Dans les aires primaires, on a un niveau important de la perception de la stimulation. Ces informations seront mémorisées et pourront participer au contrôle des mouvements, dans le maintien de l’éveil, dans la formation d’une image corporelle.
B Le système somesthésique.
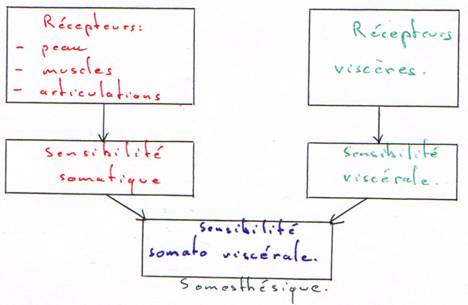
Il se distingue des autres systèmes sensoriels car il est distribué dans l’ensemble de l’organisme alors que les autres sont regroupés dans des organes sensoriels.
1 Les récepteurs.
|
Modalités
|
Récepteurs
|
Sensibilité
|
|
Toucher
|
Mécanorécepteur
|
Pression
Toucher
Vibration
|
|
Proprioception
|
Propriocepteur
- muscles<
- articulations
- tendons
|
Position relative des membres
|
|
Thermique
|
Thermorécepteur
|
Froid
Chaud
|
|
Douleur
|
Nocirécepteur
|
Température
Stimulation mécanique
Stimulation chimique
|
2 Les voies de projection principales.
On a deux voies principales et parallèles qui transmettent la sensibilité somesthésique.
a La voie des colonnes dorsales (lemniscales).
Elles transportent les informations tactiles, proprioceptives (informations sur la position du corps et des membres dans l’espace) du système somesthésique. Les informations transitent par trois relais : un au niveau du bulbe rachidien, un autre au niveau du thalamus et le dernier au niveau du cortex cérébral.
b Les faisceaux antérolatéraux (système spinothalamique).
Ces faisceaux transportent l’information thermique et nociréceptive vers le second relais du thalamus puis vers le troisième relais au niveau de l’aire somesthésique primaire.
III Le système moteur.
Ils s’organisent sur plusieurs niveaux.
A Les activités réflexes (au niveau de la moelle épinière).
On appelle arc réflexe une connexion sensori-motrice.
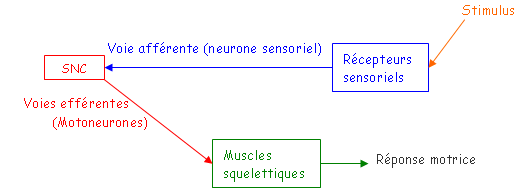
On a deux types de réflexes :
- Monosynaptique : c’est un réflexe rapide (réflexe myotatique) qui entraîne la contraction d’un muscle à son propre étirement. Le récepteur sensoriel se situe dans le muscle (il est intrinsèque). On a alors un contrôle fin de la longueur du muscle.
- Polysynaptique : l’information passe par deux ou plusieurs synapses. Il a un rôle de protection. C’est un réflexe ipsilatéral de flexion dont le récepteur est extrinsèque (à l’extérieur du muscle).
Les réflexes sont sans arrêt contrôlés par les structures supra-spinales qui agissent sur les motoneurones ou par l’intermédiaire des interneurones de la moelle épinière.
B Les activités posturales.
Les activités posturales permettent de lutter contre les effets de la gravité afin de maintenir l’équilibre du corps. Elles ont une activité permanente par le tonus musculaire.
Le réflexe myotatique occupe une place prépondérante au niveau du tronc cérébral.
1 Les formations réticulées bulbaires et pontiques.
Le niveau du tonus musculaire dépend de l’équilibre des influx excitateurs et inhibiteurs.
Ces formations réticulées reçoivent de nombreuses informations sensorielles en provenance d’autres neurones. Elles jouent un rôle important au niveau de la vigilance (activité excitatrice) et entraînent alors une augmentation du tonus musculaire.
Une activité inhibitrice entraînera, elle, une diminution de ce tonus musculaire.
2 Les noyaux vestibulaires bulbaires.
Ils contrôlent l’activité posturale par une action excitatrice au niveau des motoneurones. Ils interviennent pendant les ajustements posturaux de compensation (quand le déséquilibre est déjà établi). Les informations sont en provenance des récepteurs sensoriels à l’équilibration (labyrinthe ou vestibule).
Les noyaux vestibulaires bulbaires sont capables de réagir à un changement de position par rapport au tronc ou de position dans l’espace.
C Les mouvements volontaires.
Un acte moteur conscient est commandé à partir des aires corticales motrices.
1 Les aires corticales motrices.
a Les aires motrices primaires.
Tous les muscles y sont représentés. Ces aires sont organisées de façon somatotopique (la représentation est fonction des muscles).
Si l’on stimule un point, on a une contraction du muscle correspondant opposé.
Cette aire motrice est donc associée à l’exécution des mouvements.
b Les aires motrices d’ordre supérieur.
On distingue l’aire prémotrice (ou cortex prémoteur) et l’aire motrice supérieure (AMS).
Elles sont aussi organisés de façon somatotopique mais moins fine. Si l’on stimule l’aire prémotrice, on peut obtenir la contraction de tout un membre.
 Les arcs moteurs sont plus ou moins complexes. Les deux premières aires interviennent dans la programmation d’un mouvement. L’aire motrice supérieure est nécessaire pour concevoir et appréhender ce mouvement.
Les arcs moteurs sont plus ou moins complexes. Les deux premières aires interviennent dans la programmation d’un mouvement. L’aire motrice supérieure est nécessaire pour concevoir et appréhender ce mouvement.
2 Les voies motrices principales.
On a deux grands systèmes parallèles qui vont transmettre les commandes des aires motrices.
a Le système direct.
Il est constitué de deux voies principales :
· Cortico-bulbaire : elle contrôle la motricité volontaire des muscles de la face.
· Cortico-spinale (voie pyramidale) : elle contrôle la motricité volontaire de tous les autres muscles du corps. Elle est divisée en deux faisceaux cortico-spinaux, latéral et ventral.
b Le système indirect.
Il existe un système indirect, la voie cortico-rubro-spinale, qui effectue un relais au niveau du noyau gris, dans le mésencéphale. Il sert à affiner le mouvement.
3 Contrôle des mouvements volontaires.
Ce contrôle s’effectue à partir de trois sources d’informations :
- voie sensorielle : informations permanentes sur la position du corps et des muscles
- informations venant du cervelet
- informations venant des noyaux gris.
a Les informations sensorielles.
Ces informations viennent directement des récepteurs sensoriels ou des aires corticales sensorielles primaires d’ordre supérieur et associatif.
Le cortex pariétal postérieur est une grande source d’informations.
On a donc une adaptation des commandes motrices en fonction des circonstances.
b Les informations du cervelet.
Le cervelet régule aussi l’exécution des mouvements pendant qu’il y a lieu. Il reçoit de nombreux afférents, de la moelle épinière et du cortex moteur : il reçoit la copie du programme moteur donné par les aires motrices.
Le cervelet recueille aussi des informations sensorielles somesthésiques et du labyrinthe.
On a trois grandes régions du cervelet.
1 Le cervelet spinal.
Il est constitué du vermis et des hémisphères intermédiaires. Il reçoit les informations sensorielles (somesthésiques) et supervise les postures (cf. l’exécution des mouvements volontaires).
Il compare les commandes motrices avec les résultats de l’exécution de l’acte moteur et peut éventuellement modifier cette commande.
L’action se fait par :
- voie directe : du cervelet vers le tronc cérébral (la moelle épinière).
- voie plus longue : du cervelet vers le cortex cérébral moteur puis à la moelle épinière.
2 Le cervelet cérébral.
Il est constitué par la zone latérale des hémisphères. Cette zone établie surtout des relations avec le cortex cérébral moteur (relations bilatérales) lors de la programmation.
3 Le cervelet vestibulaire.
Il correspond au lobe flocculo-nodulaire. Il reçoit les informations du labyrinthe et visuelles. Il est impliqué dans toutes les réactions posturales ainsi que dans les mouvements conjugués de la tête et des yeux. Il est aussi organisé somatopiquement.
c Le noyau gris de la base.
Il comprend trois gros noyaux : le noyau coudé, le putamen (ces deux structures forment le télencéphale) et le pallidum.
Ces noyaux sont reliés entre eux et à d’autres structures comme le subthallamus (qui appartient au diencéphale) et à une substance noire (qui fait parti du mésencéphale).
Ces structures font intervenir de nombreux neurones transmetteurs. Elles sembleraient sélectionner les mouvements les plus adaptés dans une condition donnée.
La maladie de Parkinson (lenteur et pauvreté des mouvements) est le problème d’une voie allant de la substance noire au striatum (avec, comme neurotransmetteur : la dopamine).
La maladie de Huntington entraîne un excès de mouvements imprévisibles à cause de la dégénérescence des cellules du striatum.
Le système nerveux autonome,
Système neurovégétatif et système viscéral.
Le système nerveux autonome contrôle les fonctions organiques internes (nutrition et maintien de l’homéostasie). C’est un système qui échappe le plus souvent au contrôle de la volonté. Il s’oppose au système somatique (relations avec l’extérieur).
I Organisation générale du système nerveux autonome.
Il innerve principalement les organes internes. Les neurones sensoriels du système nerveux autonome transmettent les informations venant des fonctions viscérales vers le système nerveux central. Les motoneurones innervent les muscles lisses des viscères (muscle cardiaque et glandes).
Cet ensemble se divise en deux sous-systèmes :
- le système orthosympathique,
- le système parasympathique.
Le système orthosympathique est principalement impliqué dans les relations dites d’alerte (à court terme).
Le système parasympathique agit plutôt dans les conditions normales (durables).
A Organisation comparée des systèmes moteurs somatiques et autonomes.
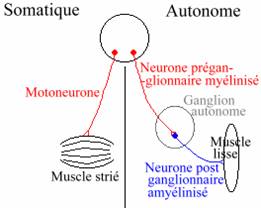
B Organisation comparée des systèmes orthosympathique et parasympathique.
Ils se différencient par trois critères :
- Origine des neurones préganglionnaires.
- Position des ganglions.
- Neurotransmetteurs agissant sur les organes effecteurs et récepteurs.
1 Le système orthosympathique.
Les corps cellulaires préganglionnaires se situent près de la moelle épinière thoracique et lombaire.
On a une chaîne ganglionnaire paravertébrale. Elle est composée de trois ganglions : cœliaque, mésentérique supérieur et inférieur.
Les neurones post-ganglionnaires quittent ces ganglions pour aller innerver les organes internes.
Cas particulier de la glande médullo-surrénale.
Elle est innervée par le système orthosympathique et correspond, elle-même, à un ganglion orthosympathique. Elle permet la libération d’Adrénaline et de Noradrénaline.
2 Le système parasympathique.
Les centres nerveux sont localisés à l’extérieur du neuraxe. Les ganglions sont situés près ou dans les viscères : le premier neurone est long alors que le second est très court. Dans ce cas, on a une disposition transmétamérique.
Le système parasympathique possède trois territoires :
- Le territoire céphalique : les fibres préganglionnaires empruntent au début le trajet des nerfs crâniens pour s’individualiser et finalement rejoindre les viscères. Par exemple, le troisième nerf est le nerf moteur oculaire commun qui innerve la pupille.
- Le territoire cervico-thoraco-abdominal : il est innervé par un nerf parasympathique important, le nerf vague (ou pneumogastrique).
- Le territoire pelvien : les fibres parasympathiques suivent en partie les nerfs rachidiens pour s’en séparer et innerver les viscères qu’elles commandent.
- le contingent supérieur innerve la vessie, l’utérus, le rectum et le colon.
- Le contingent inférieur innerve les organes génitaux externes.
Remarque : certains organes sont innervés par les deux systèmes à la fois. Le foie et les vaisseaux sanguins le sont seulement par le système orthosympathique.
C Les neurotransmetteurs.
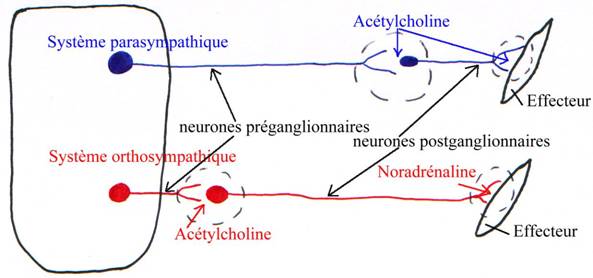
- Les récepteurs à Acétylcholine : ce sont des récepteurs nicotiniques, agonistes à l’acétylcholine avec la nicotine et situés sur le neurone postérieur.
- Les récepteurs muscariniques : la muscarine est agoniste de l’acétylcholine. On les trouve sur le muscle final innervé par le système parasympathique.
- Les récepteurs  1,2 noradrénergiques et
1,2 noradrénergiques et  1,2 noradrénergiques : ils sont situés sur les muscles innervés par le système orthosympathique.
1,2 noradrénergiques : ils sont situés sur les muscles innervés par le système orthosympathique.
Au niveau d’une même cellule, on peut trouver tous les types de récepteurs.
II Intégration des systèmes autonomes.
L’intégration s’effectue sur plusieurs niveaux :
- Le niveau réflexe : les nerfs afférents vont s’articuler sur les nerfs moteurs par l’intermédiaire d’un interneurone. On a donc un arc réflexe viscéro-viscéral (on peut aussi trouver des arcs somato-viscéraux). De nombreuses fonctions autonomes sont contrôlées par des réflexes : digestion, pression artérielle, sudation.
- Le niveau supérieur : l’hypothalamus est le régulateur essentiel des neurones … mais aussi externes en contrôlant ainsi le fonctionnement du système nerveux autonome.
En général, les systèmes orthosympathique et parasympathique ont des effets opposés.
- Le système orthosympathique intervient dans la réponse au stress par une accélération du rythme cardiaque, de la pression artérielle et par la mobilisation des réserves énergétiques : il prépare l’organisme à l’action.
- Le système parasympathique permet le maintient des ressources corporelles (diminution du rythme cardiaque et de la pression artérielle). Il favorise la digestion. è ce système prépare le corps à la relaxation et au repos.
Chapitre 3 : La Digestion.
I INTRODUCTION.
Les cellules de l’organisme ont besoin de nutriments : glucides, lipides, protéines, vitamines, sels minéraux et eau ; ces nutriments existent dans nos aliments, mais sous une forme complexe, incapables de traverser les membranes cellulaires.
La digestion a donc pour rôle de simplifier le bol alimentaire, l’amenant progressivement vers des formes physiques et chimiques, compatibles avec leur absorption digestive et leur transfert dans le système de distribution cellulaire : le sang et la lymphe. Ce rôle est assuré par le tube digestif dont le fonctionnement peut se résumer par :
• Une activité mécanique : aspiration, mastication, déglutition, brassage, remplissage et vidange.
• Une activité chimique et biochimique, surtout enzymatique, faisant intervenir des sucs élaborés par des cellules ou des glandes.
La température, l’osmolarité, le pH du bol alimentaire, la dimension des particules, leur liposolubilité et leur hydrosolubilité seront amenés progressivement par le travail des différents segments du système digestif à des caractéristiques favorables au passage trans-membranaire.
II ANATOMIE
A Structure générale
Le système digestif comprend le tube digestif dont les éléments sont la bouche, le pharynx, l’œsophage, l’estomac, l’intestin grêle, le côlon, le rectum et les glandes annexes, comme les glandes salivaires, la vésicule biliaire et certaines parties du foie et du pancréas.
On peut assimiler le tube digestif à un conduit de calibre variable, traversant le corps de la bouche à l’anus, sa longueur est d’environ 5m, sa lumière est en continuité avec le milieu extérieur, si bien que son contenu ne fait pas partie intégrante de l’organisme : c’est l’exemple des bactéries très présentes dans la partie terminale de l’intestin où elles sont inoffensives et même utiles mais, si elles pénètrent dans l’organisme, elles deviennent rapidement pathogènes, c’est ce qui se passe lors des crises d’appendicite.
L’anatomie de chaque segment du tube digestif sera détaillée lors de l’étude des différentes étapes de la digestion.
B Histologie.
L’histologie du tube digestif est identique sur toute sa longueur. En allant de l’extérieur vers la lumière du tube digestif, on rencontre :
• une séreuse qui enveloppe le tube,
• une 1ère couche de muscles lisses orientée longitudinalement,
• une 2ème couche de muscles lisses circulaires,
• une 3ème couche appelée « muscularis mucosae » ou pour être plus explicite “la musculaire de la muqueuse” ; elle est constituée de fibres circulaires et de fibres longitudinales ; elle se situe exactement entre la sous-muqueuse (qui est au contact de la couche de muscles lisses circulaires) et la muqueuse.
• la muqueuse est la couche cellulaire au contact de la lumière ; c’est là que se trouvent les glandes exocrines qui déversent les produits de leur sécrétion dans la lumière et les villosités épithéliales chargées de l’absorption des nutriments. C’est une couche plissée qui accroît la surface de contact avec le bol alimentaire.
La sous-muqueuse est un tissu conjonctif qui contient quelques cellules glandulaires exocrines mais surtout les vaisseaux sanguins et lymphatiques qui draineront les nutriments absorbés.
SE = séreuse
CML = couche de muscles lisses
< ---- > PLEXUS 1
CMC = couche de muscles circulaires
SM = sous-muqueuse
MM = musculaire de la muqueuse
< ---- > PLEXUS 2
M = muqueuse
La surface du tube digestif n’est pas lisse, mais finement plissée, surtout au niveau de l’intestin grêle (100 à 150m²).
Tous ces muscles sont formés de faisceaux de myofibrilles anastomosées, c’est-à-dire dont les membranes fusionnent par endroits pour former “les nexus”, zones de contact privilégié où la résistance électrique est moindre favorisant ainsi la dépolarisation. Ces fibres lisses sont formées de myosine (1 filament épais par fibre) entourée d’actine (environ 15 filaments fins par fibre), dont le glissement provoque la contraction de la fibre ; le principe de la contraction est le même que celui du muscle strié (avec intervention de Ca2+, de l’ATP pour donner de l’énergie), mais la réponse du muscle à l’excitation est plus longue et la contraction est plus soutenue.
Les contractions de ces muscles peuvent être localisées (activité segmentaire), servant au brassage des aliments ou propagées (péristaltisme) assurant ainsi le transit du bol alimentaire le long du tube digestif.
C Commande neuro-humorale de l’activité sécrétoire et motrice.
Les activités motrice et sécrétoire du tube digestif sont sous un double contrôle nerveux et endocrinien. L’activité sécrétoire est à la fois exocrine et endocrine.
Les glandes exocrines sont situées dans la paroi même du tube digestif mais aussi à distance du tube digestif : glandes salivaires, foie, pancréas ; leur production est déversée dans la lumière du tube digestif par des canaux plus ou moins longs.
Les glandes endocrines sont situées dans la muqueuse du tube digestif ; elles sécrètent trois principales hormones :
• la gastrine (estomac),
• la sécrétine et la cholécystokinine (première portion du grêle) qui sont drainées directement par le sang (voie veineuse) et redistribuées (voie artérielle au tube digestif dont elles peuvent affecter la motilité et la sécrétion, même en des portions parfois éloignées de leur point d’origine (lieu de sécrétion).
Les activités motrices et sécrétoires du tube digestif sont commandées :
• d’une part et en grande partie, par son propre système nerveux local (intrapariétal) ; il s’agit des plexus, qualifiés d’intrinsèques ou intra-muraux,
• d’autre part, par des voies nerveuses longues du système végétatif qui peuvent, soit se connecter sur les plexus, soit innerver directement le tube digestif.
Autrement dit, la commande nerveuse sur les systèmes sécrétoire et moteur est essentiellement locale, c’est-à-dire intrapariétale grâce aux plexus intramuraux. Elle peut aussi dépendre du système nerveux végétatif qui va agir directement ou indirectement. Il existe des réflexes :
- courts qui relient les récepteurs aux effecteurs par les plexus;
- longs qui relient les récepteurs au système nerveux central ---> plexus --->neurones ---> effecteurs.
1 Régulation nerveuse : les plexus.
Les plexus sont faits de corps neuroniques, avec leurs prolongements axoniques et dendritiques, et des terminaisons nerveuses des fibres longues, ortho et parasympathiques.
• le plexus myentérique (ou d’Auerbach), situé entre la couche musculaire circulaire et la couche musculaire longitudinale
• le plexus sous-muqueux (ou de Meissner) situé entre la muqueuse et la couche musculaire circulaire.
Ces plexus existent tout le long du tube digestif, de l’œsophage à l’anus ; leurs neurones se relaient entre eux par des synapses à l’intérieur d’un même plexus. Le plexus myentérique a des rapports plus étroits avec la musculature du tube digestif que le plexus sous muqueux qui aurait un rôle dans les activités sécrétoires et régulatrices du tube digestif et, à un moindre degré, motrices.
Les fibres du système nerveux végétatif, ortho et parasympathiques pénètrent dans la paroi du tube digestif et font synapse avec les neurones du plexus ; leurs actions s’exercent donc en grande partie par l’intermédiaire des plexus, mais parfois ces fibres court-circuitent les plexus et se terminent directement sur les muscles ou les glandes du tube digestif. C’est en partie le cas pour le nerf vague (X ou pneumogastrique), dont les fibres se distribuent aux parois de l’estomac, de l’intestin grêle et du côlon. Parmi ces fibres, certaines sont afférentes et d’autres efférentes.
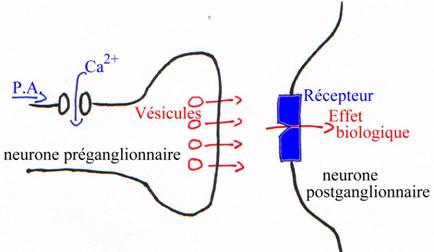
Le contact entre les fibres nerveuses et les fibres musculaires se fait sans structure différenciée de type plaque motrice, mais par simple contiguïté ; la cellule nerveuse sécrète son médiateur au voisinage de la membrane musculaire sur laquelle il arrive par diffusion pour se fixer sur son récepteur spécifique. Il y a les neuromédiateurs classiques, l’acétylcholine et la noradrénaline mais aussi d’autres substances comme la sérotonine, l’histamine ou les prostaglandines, qui peuvent avoir des actions directes ou indirectes, activatrices ou inhibitrices.
2 Régulation hormonale.
· A l’inverse de ce que l’on observe pour les éléments endocriniens (gonades, surrénales, hypophyse, thyroïde), les cellules qui sécrètent les hormones du TD sont des cellules isolées à travers tout l’épithélium de l’estomac et de l’intestin grêle ; c’est-à-dire qu’elles ne sont pas groupées en petits organes ou glandes.
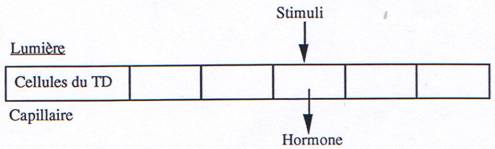
La stimulation a lieu au niveau de la lumière du TD, la sécrétion se fait au niveau des capillaires c’est-à-dire de l’autre côté de la cellule cible.
On retrouve certaines hormones en petites quantités également dans la lumière du TD (rôle paracrine des hormones).
Une douzaine d’hormones sont considérées comme des hormones gastro-intestinales, seules trois le sont réellement : Sécrétine - CCK - Gastrine.
Les autres substances sont des hormones que l’on appelle candidats :
- Bombésine - GIP (Peptide Inhibiteur Gastrique) - Motiline - Somatostatine - VIP (Peptide Vaso-actif Intestinal) - Villikinine - Entéroglucagon.
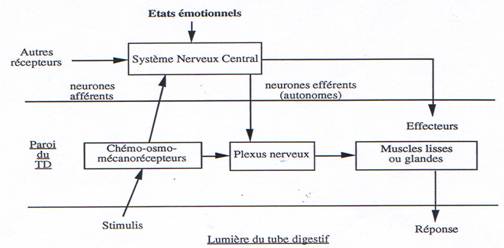
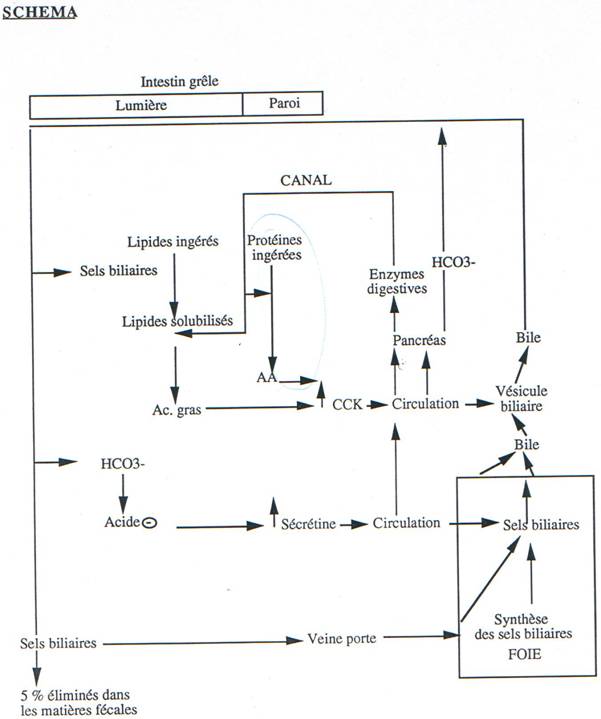
3 Schéma général du contrôle du tube digestif
Les muscles lisses et les glandes exocrines du tube digestif sont sous trois influences directes :
1- l’innervation extrinsèque.
2- l’innervation intrinsèque.
3- les hormones issues des propres parois du tube digestif.
Quant aux glandes endocrines responsables de l’élaboration et de la mise en circulation des facteurs hormonaux, elles sont aussi sous l’influence des commandes précédentes, mais elles répondent aussi aux changements de la composition et du volume du contenu du tube digestif.
Les récepteurs locaux sont sensibles aux caractéristiques chimiques du contenu du tube digestif et à la tension pariéale. Ces informations peuvent être transmises, soit aux plexus, soit aux centres supérieurs. Dans le premier cas, on a un réflexe dit court, à base de l’autorégulation digestive mais il n’échappe pas au contrôle supérieur, surtout lorsque le réflexe court est mis en jeu par des récepteurs situés loin du tube digestif (vue, odeur des aliments).
III PHYSIOLOGIE.
A Digestion.
1 Généralités.
a Mécanismes généraux des sécrétions digestives.
Grâce à ses glandes à mucus, le tube digestif sécrète un film lubrifiant et protecteur contre l’agression mécanique et chimique des aliments. Ce film contient :
* des glycoprotéines, ou mucopolysaccharides, sécrétées par des glandes superficielles, ou par les glandes supérieures des cryptes ; elles participent à l’ajustement du pH, grâce à leur pouvoir tampon, leur sécrétion est permanente mais accélérée par le contact alimentaire.
* des sucs sécrétés par des glandes très diverses ; ces sucs contiennent d’une façon générale :
- des bicarbonates d’origine plasmatique (pour une faible part) mais surtout synthétisés.
- des électrolytes qui viennent aussi du plasma en concentration variable, du fait des mécanismes de sécrétions et de réabsorption.
- des protéines enzymatiques synthétisées de façon classique par les cellules.
Ces sécrétions sont sous le double contrôle neuroendocrinien avec une innervation végétative qui agit directement sur les cellules sécrétrices mais aussi sur les glandes endocrines qui libèrent des hormones régulatrices (activatrices ou inhibitrices) de la sécrétion des sucs. Leur libération peut se faire sous l’action du SNV mais aussi sous l’effet des actions mécanique et chimique des aliments, ce dernier facteur étant prépondérant.
Il y a une inter-relation fonctionnelle constante, nerveuse et hormonale ; les deux systèmes peuvent se potentialiser mutuellement, ou s’autoréguler, en formant des boucles de rétro-inhibition ou feed-back.
Exemples :
- La stimulation du nerf vague sensibilise la glande de l’estomac à l’action de la gastrine.
- La sécrétion de gastrine active les cellules stomacales sécrétant l’HCl ; les ions H+ libérés abaissent le pH qui inhibe la sécrétion de gastrine.
b Conditions générales des hydrolyses enzymatiques
Le bol alimentaire va subir des modifications physiques et chimiques.
- fragmentation par la mastication.
- ramollissement, dissolution et dispersion par l’eau.
- action acide du suc gastrique.
- action des nombreuses enzymes qui scindent les molécules.
Ces réactions enzymatiques ont une vitesse qui dépend de la température (en fait peu d’augmentation car elle est uniforme dans le tube digestif) et surtout du pH spécifique à chaque enzyme : pepsine -> pH acide - trypsine -> pH neutre.
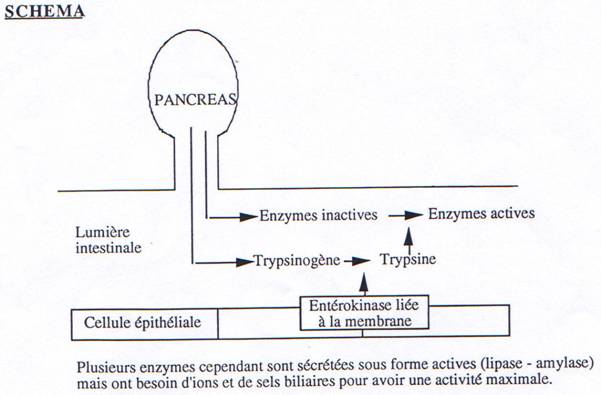
Les enzymes protéolytiques sont livrées par la glande sous forme de précurseurs inactifs :
Pepsinogène, trypsinogène, etc. qui sont activés par amputation d’un segment qui masque le site actif de l’enzyme ; ces amputations sont réalisées par des protéases, appelées kinases, plus ou moins spécifiques et qui nécessitent souvent la présence de l’ion Ca2+.
Les lipases n’agissent que lorsque le substrat est en émulsion fine et stable, d’où la présence d’agents émulsifiants tels que les sels biliaires.
Enfin, il y a des enzymes digestives endo-cellulaires qui n’agissent que lorsque le substrat pénètre dans la cellule, ou lorsque la cellule est desquamée, libérant ainsi son enzyme dans le tube digestif.
c Méthodes générales de l’exploration de la fonction digestive
1 Exploration de la mécanique digestive
On peut suivre les variations de la pression endo-cavitaire des différents segments. Elles sont le reflet du tonus pariétal et des contractions rythmiques. On utilise des sondes ouvertes, des sondes à ballonnets, des jauges de contrainte ou des capsules radio-émétrices.
On peut aussi mesurer les activités électriques du tube digestif à l’aide d’électrodes qui mesurent des potentiels d’actions. Le transit peut être apprécié sur toute la longueur du tube digestif grâce à des colorants ou des traceurs radioactifs que le sujet ingère et dont on suit l’élimination en fonction du temps.
La radiographie et la radio-cinématographie permettent, grâce à l’ingestion de produits radiopaques, plusieurs possibilités :
• visualiser les dimensions et la forme des cavités digestives ; déceler à leurs niveaux d’éventuelles anomalies : sténoses, stases, ulcères, tumeurs, etc.
• analyser les mouvements et mesurer les temps intermédiaires de transit (oesophagien, stomacal, etc.)
2 Exploration des sécrétions digestives et de leur régulation.
On peut recueillir les différents sucs digestifs par des fistules temporaires ou chroniques chez l’animal. Chez l’Homme, on utilise en général une sonde placée par voie naturelle (tubage gastrique ou duodénal). On peut ainsi recueillir des sucs digestifs et en préciser les principales caractéristiques physico-chimiques : volume, pH, viscosité, électrolytes, etc. On peut également mesurer in vitro, sur des substrats adéquats, les activités enzymatiques de ces sucs digestifs.
En ce qui concerne les hormones, on utilise des techniques de radio-immunologie qui permettent de doser, dans le sang et dans les tissus, de très petites quantités d’hormones (nano ou picogrammes).
Le principe de ces dosages sera détaillé au cours d’autres enseignements, on peut ainsi doser la gastrine, la sécrétine ou la cholécystokinine.
3 Mesure du coefficient d’utilisation digestive (CUD).
Des méthodes permettent d’évaluer les possibilités digestives et surtout d’absorption digestive d’un individu. On peut doser dans le sang certains aminoacides mais la méthode la plus utilisée consiste à doser l’azote dans l’ingéré (aliments) et dans les excrétats (urine et fèces) afin de connaître par différence, l’azote retenu par l’organisme ; on peut ainsi déterminer certains coefficients, comme le CUD, le CEP, etc.
1 Bouche - Pharynx - Oesophage.
L’extrémité orale constitue un organe de préhension grâce à ses muscles (joues, lèvres, langue) ; les aliments solides vont être l’objet, dans la bouche, d’actions mécaniques (mastication) et chimique (insalivation).
a Mastication
Les fonctions essentielles des dents sont de mordre et de mastiquer pour prélever et réduire cette bouchée en fragments assez petits pour être déglutis. La pression exercée par les dents est très grande ; pression des incisives : 10 à 25 kg ; des molaires environ 100 kg.
La mastication prolongée est une caractéristique de l’Homme. De nombreux animaux (chat, chien) avalent sans mâcher ; l’action essentielle de la mastication est de réduire la taille des morceaux pour éviter des accidents.
La contraction des muscles masticateurs (temporal, masseter) est sous le contrôle nerveux de la branche motrice du trijumeau (nerf crânien n05), dont l’origine serait un centre masticateur dans le bulbe rachidien. La mastication peut être volontaire mais aussi déclenchée par un mécanisme réflexe avec, comme point de départ, des récepteurs situés dans la bouche (un animal décortiqué conserve la mastication quand un aliment est placé dans sa bouche).
En plus du contrôle volontaire (nerfs somatiques) des muscles squelettiques de la bouche et de la mâchoire, les mouvements rythmiques de la mastication sont déclenchés de façon réflexe par la pression des aliments sur les gencives, les dents, le palais et la langue (àinhibition des muscles qui maintiennent la bouche fermée).
b Salivation.
Trois paires de glandes exocrines sécrètent la salive (chez l’Homme, environ 1 à 2 litres /24 H) ; ce sont les glandes parotides, sous maxillaires et sublinguales.
La salive parotidienne est fluide (riche en eau) ; les 2 autres salives sont plus visqueuses (mucus). La salive contient 99 % d’eau, des sels minéraux et des protéines (1 %).
Les protéines les plus caractéristiques sont :
• les mucines qui, mélangées à l’eau, forment le mucus qui imbibe et lubrifie le bol alimentaire : glycoprotéines, mucopolysaccharides.
• la ptyaline c’est une amylase qui dégrade les polysaccharides en disaccharides ; ce travail commence dans la bouche et se poursuit dans l’estomac, tant que le pH acide n’inhibe pas cette enzyme.
La composition de la salive varie en fonction du débit de sécrétion et du stimulus qui est à l’origine de la salivation ; il y aura une sécrétion primaire assurée par les acinus et remaniée au cours de son écoulement par des phénomènes de réabsorption (Na+), (C03H-) ou de sécrétion (K+), pour aboutir à une salive définitive.
La sécrétion salivaire est permanente mais son débit varie selon les circonstances.
Les glandes salivaires reçoivent une double innervation végétative: ortho-sympathique (adrénergique) et parasympathique (cholinergique) et, contrairement au cas général, il n’y a pas antagonisme entre les deux systèmes ; ils sont tous les deux activateurs, le parasympathique étant, et de loin, le plus actif.
La boucle réflexe comprend une stimulation des récepteurs buccaux (chimio-récepteurs et mécano-récepteurs), un cheminement par des fibres jusqu’aux centres bulbaires d’intégration puis retour par d’autres fibres jusqu’aux effecteurs. Les fibres cholinergiques agiraient surtout au niveau de la sécrétion primaire (production d’eau et d’électrolytes) et les fibres adrénergiques agiraient plutôt sur les cellules des canaux excréteurs (K+,C03H-).
Les stimulus les plus efficaces sont les solutions acides diluées (jus de citron : 7 - 8 ml/min) ; le point de départ peut aussi être extra-buccal (œsophage, vue, odeur, sons). Ces réflexes sont très conditionnables ; c’est le réflexe classique de Pavlov ; par exemple l’expression « l’eau à la bouche ».
Il n’y a pas de commande hormonale spécifique de la salivation, mais certaines hormones peuvent avoir une action, comme l’ADH et l’aldostérone. L’ADH réduit le débit ; l’aldostérone augmente la réabsorption du Na+ et la sécrétion du K+.
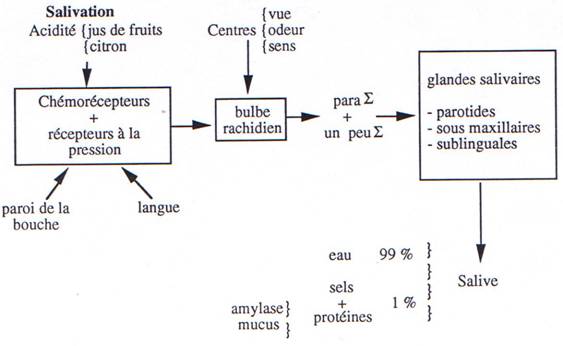
Les rôles de la salive sont donc multiples :
- commencer l’hydrolyse de certains glucides.
- humecter la bouche (indispensable à l’élocution).
- solubiliser les substances chimiques qui peuvent ainsi stimuler les papilles gustatives.
- enrober le bol alimentaire de mucus pour permettre sa déglutition.
c Déglutition.
C’est un acte réflexe complexe qui est provoqué lorsque le bol alimentaire poussé par la langue est propulsé dans l’estomac. Il existe des récepteurs mécaniques du pharynx qui envoient des influx sensitifs vers le centre bulbaire de la déglutition. Ce centre coordonne les mouvements de la déglutition en envoyant à son tour des influx moteurs vers les effecteurs, constitués par les 25 muscles du pharynx, du larynx et de l’œsophage. Une fois amorcée, la déglutition ne peut plus être arrêtée ; c’est le type de réflexe du tout ou rien, coordonné, automatique, programmé par les connections synaptiques.
On distingue classiquement trois temps dans ce réflexe de déglutition:
• le temps buccal : Il est assuré par la langue, sous contrôle volontaire : il permet de propulser par ses mouvements, le bol vers le pharynx.
• le temps pharyngien : La langue obture l’orifice buccal pour empêcher le retour dans la bouche ; il y a fermeture des fosses nasales par le voile du palais, fermeture des voies respiratoires par la glotte, puis par l’épiglotte, empêchant ainsi toute fausse route du bol, ouverture du sphincter oesophagien supérieur et passage des aliments
• le temps oesophagien : Dans l’œsophage, le bol est poussé vers l’estomac par une onde péristaltique qui se propage de proche en proche (2 à 4 cm/s) Elle est commandée au début par le système nerveux végétatif puis, en fin de parcours, par les plexus. Plusieurs ondes peuvent être nécessaires pour vider l’œsophage (bol trop gros) ; elles sont puissantes et permettent le passage contre la pesanteur (tête en bas).
Note : pendant la grossesse, la pression abdominale augmente : le contenu stomacal est en parti refoulé ; l’œsophage est irrité par le suc gastrique : -> pyrosis.
La déglutition des aliments solides ou pâteux dure 1-2 secondes dans la bouche, moins de 1 seconde dans le pharynx, 3-5 secondes dans l’œsophage. La déglutition des liquides est plus rapide ; on peut aussi déglutir de l’air jusqu’à 500 mL, dont la plus grande partie ne dépasse pas l’œsophage, car il est expulsé par éructation, mais il peut aussi arriver dans l’estomac (100 mL), puis dans l’intestin.
1 Digestion dans l’estomac
L’estomac est un réservoir qui sécrète un acide fort, l’HCl et plusieurs enzymes. La digestion stomacale consiste en un morcellement du bol alimentaire en molécules, ou ensemble de molécules, encore trop important pour être absorbé : on parle du chyme stomacal.
a Digestion mécanique.
L’estomac est une poche très plissée, d’un volume moyen de 50 mL à vide et qui se déplisse lors du remplissage (1,5 L) ; sa structure est décrite dans le paragraphe précédant de l’anatomie. C’est au niveau de l’estomac que les plexus sont les plus nombreux (coup de poing) et les fibres orthosympathique et parasympathique assurent la liaison avec l’axe cérébro-spinal.
Il y a une activité électrique de base, sous forme d’ondes, qui provoque des contractions musculaires lentes qui vont du cardia au pylore.
La première bouchée déglutie arrête cette activité et l’estomac reste immobile pendant 30 à 60 minutes après le début du repas ; les aliments ingérés se disposent en couches successives.
Après ce délai, les ondes reprennent, mélangent les aliments et les sucs ; elles poussent le bol vers le pylore dont le sphincter est fermé ; le bol reflue vers le cardia et ce brassage continue jusqu’à ce que le chyme réponde aux critères de pH et de granulométrie. L’estomac se vide par petites éjaculations successives et le temps d’évacuation peut aller de 20 mn pour les liquides, à 5-6 heures pour les repas normaux à 12, 18 et même 24 heures pour les grandes “bouffes”. Ces mouvements sont régulés par réflexes courts (plexus) et par réflexes longs (SNV) : les stimuli sont thermiques, mécaniques et chimiques. La stimulation du nerf vague renforce l’activité gastrique et le système orthosympathique la diminue. Ces actions sont complétées par l’intervention de diverses hormones : la gastrine les augmente ; le glucagon, la sécrétine et le VIP les diminuent.
b Suc gastrique.
Sur le plan sécrétoire, on distingue deux parties fonctionnellement distinctes dans l’estomac :
• la muqueuse de la poche principale (fundus) qui élabore les enzymes (cellules principales) et dont les cellules pariétales, ou bordantes, sécrètent les ions H+.
• la région antro-pylorique (antre ou antrum), dont les glandes donnent des sécrétions alcalines riches en bicarbonates. La gastrine y est aussi sécrétée.
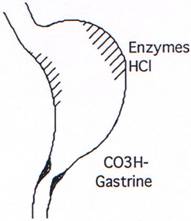
1 Composition.
Le suc gastrique est sécrété de façon permanente (environ 2 litres/24 h) ; il augmente au cours des repas ; c’est un liquide incolore, visqueux et acide ; il contient du mucus, des électrolytes (H+, Cl, Na+, K+, CO3H-, des enzymes, surtout des pepsines et une glycoprotéine le facteur intrinsèque de Castle, qui est nécessaire à l’absorption de la vitamine B 12).
1- l’HCl :
C’est un acide fort, totalement dissocié dans la lumière gastrique. On ne connaît pas le mécanisme moléculaire précis de sa sécrétion par les cellules pariétales. L’ion H+ peut être produit par oxydo-réduction (pompe rédox) ou par dissociation de l’eau. Sa production et sa libération par le pôle muqueux de la cellule sont des mécanismes actifs consommateurs d’énergie (ATP). L’ion OH- (dans le cas de la dissociation de l’eau) est neutralisé dans la cellule pariétale par les bicarbonates formés à partir du C02 sanguin qui, sous l’action de l’anhydrase carbonique, forment des ions HCO3- rejetés dans le plasma au pôle séreux de la cellule pariétale. L’ion Cl- se déplace, du pôle séreux au pôle muqueux, par un phénomène actif, contre un gradient électrochimique. C’est finalement de l’HCl qui est déversé dans la lumière amenant le pH au voisinage de 1.
2- les protéines enzymatiques gastriques :
Ce sont des protéases, lipases et uréases. Leur synthèse est classique : réticulum endothélial, appareil de Golgi.
Pour les protéases, seule la pepsine a une activité digestive importante ; elle est sécrétée sous forme de pepsinogène ; l’amputation du fragment inhibiteur est induite par l’HCl et se poursuit par l’action de la pepsine
La lipase n’agit que sur des acides gras à chaîne courte. Le rôle de l’uréase est inconnu.
Remarque : Chez les ruminants, la présure est une peptidase qui agit sur la caséine du lait ; chez l’homme, ce rôle est joué par la pepsine.
2 Actions.
Grâce à l’HCl, le suc gastrique “cuit” les aliments ; il dissout la cellulose et les fibres conjonctives des faisceaux musculaires des viandes qui se fragmentent. Son action protéolytique est due aux pepsines. Ce sont des endopeptidases qui agissent à pH 1-3, 5, surtout sur la fonction amine d’acides aminés aromatiques (phénylalanine, tyrosine) ; elles digèrent donc incomplètement les protéines.
Le suc gastrique stimule les chimio-récepteurs et inhibe la sécrétion de gastrine.
Remarque : La digestion gastrique n’est pas indispensable ; certains individus, privés partiellement ou totalement d’estomac (ulcères, cancer, nécessitant une gastrectomie) digèrent des aliments fragmentés et supplémentés en vitamine B 12.
3 Régulation de la sécrétion (gastrine, CCK).
Les productions d’acides et d’enzymes sont sous un double contrôle : nerveux et hormonal.
On distingue :
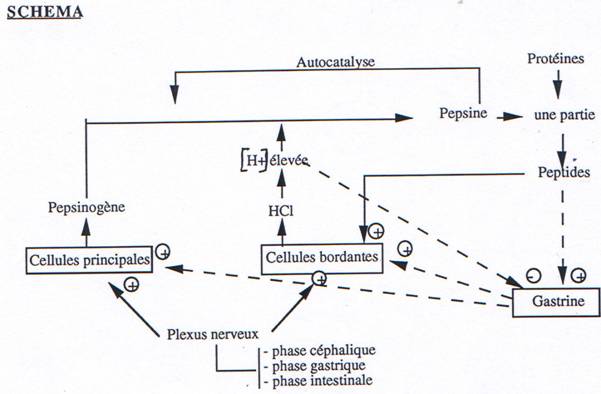
• La phase céphalique : Au cours de cette phase, la sécrétion s’accroît avant que les aliments n’aient atteint l’estomac. C’est par la voie vagale, dont les fibres parasympathiques servent de relais entre l’estomac et les centres nerveux supérieurs, que se réalise cette sécrétion psychique qui peut être déclenchée par la vue, l’odeur, le goût et le souvenir d’un aliment. Ce suc d’amorce est important ; il accueille les aliments et commence la digestion des protéines en peptides qui deviennent à leur tour des stimulateurs de la sécrétion gastrique.
• La phase gastrique : L’arrivée des aliments dans l’estomac déclenche la sécrétion gastrique d’HCl et d’enzymes. Cette sécrétion est due à la gastrine produite par les cellules de la muqueuse de l’antrum. Le stimulus le plus puissant de la sécrétion de gastrine est la présence de protéines alimentaires dans l’estomac mais les protéines intactes sont moins efficaces que les fragments peptidiques et que certains acides aminés. La stimulation mécanique de l’antrum déclenche aussi la sécrétion de gastrine ainsi que la stimulation du nerf vague.
Remarque : L’alcool, la caféine, le cola sont de forts stimulateurs de cette sécrétion. Leur prise est souhaitable avant le repas ; elle est néfaste en dehors des repas (acidité en augmentation). L’anesthésie de la muqueuse antrale supprime la sécrétion de gastrine il s’agit donc de réflexes locaux qui stimulent les cellules à gastrine, par contre, ces cellules sont inhibées par les ions H+, la sécrétine, le glucagon et la somatostatine.
LA GASTRINE :
C’est un peptide de 17 acides aminés, dont les 5 derniers sont responsables de ses effets. Elle possède de nombreux sites d’action tout le long du tube digestif.
En terme de biologie moléculaire, on peut voir les homologies de certaines séquences de la gastrine humaine et de celle du porc. Elles ne diffèrent entre elles que par un seul acide aminé.
On peut comparer aussi avec une autre hormone, la cholécystokinine qui possède la même séquence terminale d’acides aminés ; mais elle est moins efficace que la gastrine car l’efficacité dépend aussi de l’autre partie de la molécule qui est différente entre les 2 hormones et qui est responsable de l’affinité pour le site récepteur.
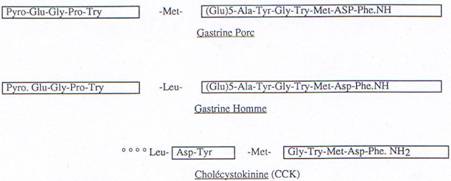
Les actions cellulaires de la gastrine consistent surtout à stimuler la sécrétion d’HCl par les cellules pariétales. Ces cellules ont au moins trois types de récepteurs : gastrine, histamine et ACh. La gastrine stimule aussi la sécrétion de pepsine et celle des enzymes pancréatiques ; elle favorise le développement et la régénération de la muqueuse gastrique ; elle renforce la motricité du sphincter oesophagien inférieur et celle de l’antrum.
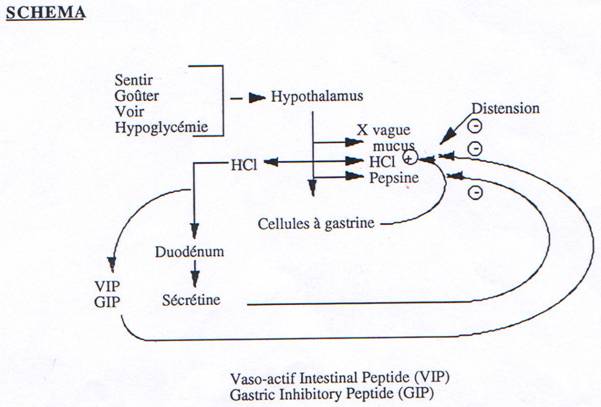
Les facteurs qui inhibent la sécrétion acide de l’estomac sont les mêmes que ceux qui inhibent la sécrétion de gastrine ; ce sont surtout les peptides hormonaux produits par la muqueuse de l’intestin grêle et par le pancréas : sécrétine, glucagon, G.I.P et V.I.P.
Cette phase d’inhibition de la sécrétion gastrique est souvent qualifiée de phase intestinale.
2 Digestion dans l’intestin grêle.
L’intestin grêle reçoit le chyme gastrique et les sucs pancréatique, biliaire et intestinal ; il est le siège de la majeure partie de la digestion enzymatique.
a Digestion mécanique
Il y a deux types de contractions.
• les contractions segmentaires : Elles apparaissent sur un segment de 2 à 3 cm, disparaissent et réapparaissent sur le segment voisin. Ce type de mouvements favorise le brassage des aliments mais n’est pas propulsif.
• les contractions propulsives : Elles sont dues aux muscles circulaires qui se contractent en amont et se relâchent en aval, formant ainsi un anneau de contraction qui pousse en avant le bol alimentaire. La régulation de cette motricité se fait par voie réflexe : ce sont les réflexes gastro-iléal, iléo-gastrique et intestino-intestinal. Les stimuli sont chimiques et mécaniques ; les voies afférentes sont nombreuses (nerf splanchnique) ; les centres sont médullaires qui envoient par les voies adrénergiques ou cholinergiques des réponses activatrices ou inhibitrices.
>Deux hormones renforcent la motricité du grêle : la gastrine et la cholécystokinine.
b Suc pancréatique.
Le suc pancréatique est élaboré par le pancréas exocrine ; il est déversé par un canal dans le duodénum. Pour l’emplacement du pancréas, voir le schéma du tube digestif ; de même pour la structure du pancréas qui est constitué de lobules regroupant des acini exocrines, s’ouvrant sur des canalicules excréteurs, qui confluent vers le canal principal, ou de Wirsung, abouché au duodénum par l’ampoule de Vater ; cette ampoule est contrôlée par le sphincter d’Oddi. Il y a aussi un ou plusieurs canaux accessoires, dits de Santorini. Enfin, parmi les lobules, de place en place se trouvent des amas de cellules endocrines, formant les îlots de Langerhans.
1 Composition.
Le suc pancréatique est sécrété au taux moyen de 1 à 2 litres /24 h. C’est un liquide incolore muqueux, pH 8,5 ; il contient des électrolytes : Na+ ; K+ ; Cl- et CO3H-, sécrétés par les cellules canaliculaires, des protéines enzymatiques dont une amylase ou 1-4 glucosidase qui hydrolyse les disaccharides en sucres simples, une lipase qui libère des acides gras et des monoglycérides à partir des triglycérides émulsionnés et des phospholipases dont la phospholipase A, des pro-enzymes inactives activées sous l’action de la trypsine, elle-même y compris :
- le trypsinogène activé en trypsine dans le duodénum par l’entérokinase. C’est une endopeptidase qui hydrolyse à pH alcalin certains acides aminés basiques (lysine, arginine).
- le chymotrypsinogène donnera la chymotrypsine, endopeptidase qui hydrolyse les liaisons d’acides aminés aromatiques (phénylalanine, tyrosine).
- La proélastase donne l’élastase, une endopeptidase active sur les liaisons des acides aminés courts (glycocolle, alanine).
- la procarboxypeptidase, activée en carboxypeptidase, qui libère l’acide aminé C-terminal de la protéine.
La ribonucléase et la désoxyribonucléase : ce sont des estérases des acides nucléiques qui les transforment en mononucloéotides libres.

Toute cette partie organique du suc pancréatique est sécrétée par les cellules acineuses.
2 Régulation de la sécrétion.
La régulation de la sécrétion pancréatique est à la fois nerveuse et hormonale. Les sécrétions électrolytiques et protéiques, bien que simultanées, ont chacune leur propre régulation.
- Régulation nerveuse : Le pancréas est innervé par le nerf pneumo gastrique, cholinergique, et le nerf splanchnique, adrénergique. Les stimulus de départ sont la vue, le goût, l’odeur et le contact des aliments.
- Régulation hormonale : il y a intervention de la sécrétine, de la cholécystokinine et de la gastrine.
• SECRETINE :
C’est à partir des travaux de Bayliss et Starling sur la sécrétine, en 1902, qu’a été dégagée la notion d’hormone ; elle a été isolée en 1961 et séquencée en 1969. C’est un peptide de 27 acides aminés dont les principales actions sont :
- Stimuler la sécrétion de la pepsine gastrique.
- Inhiber celle de l’HCl.
- Stimuler les sécrétions biliaire et intestinale.
- Stimuler la sécrétion pancréatique, surtout celle des bicarbonates mais très peu celle des enzymes
La sécrétion de sécrétine est stimulée par les fibres cholinergiques (nerf vague), les peptides, quelques acides aminés et acides gras et surtout par les ions H+.
• CHOLECYSTOKININE = PANCREOZYMINE :
On a longtemps cru, de 1928 à 1964, qu’il s’agissait de deux hormones différentes, alors que c’est un principe actif unique, un peptide dont les actions sont les suivantes :
- augmentation de la sécrétion biliaire (action cholagogue),
- potentialise l’action de la sécrétine sur le pancréas,
- augmente la sécrétion du pancréas surtout celle d’enzymes,
- augmente la sécrétion d’HCl et d’enzymes par l’estomac (comme la gastrine).
La CCK a les mêmes facteurs d’activation que la sécrétine.
• GASTRINE (cf. pages précédentes).
En résumé, la sécrétion pancréatique est sous la dépendance :
- d’une phase céphalique : réflexe par voie vagale,
- d’une phase gastrique par la gastrine,
- d’une phase intestinale avec la sécrétine et la cholécystokinine.
L’action du pancréas est déterminante, car les bicarbonates amènent le pH à une valeur moins agressive pour la muqueuse (plus propice aux activités enzymatiques qui attaquent tous les types de nutriments), l’amylase pancréatique prend le relais de l’amylase salivaire ; la lipase digère les lipides et les protéases hydrolysent plus avant les protéines.
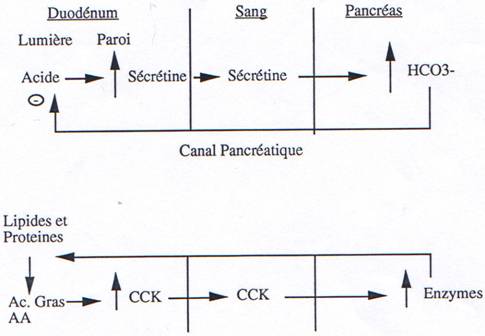
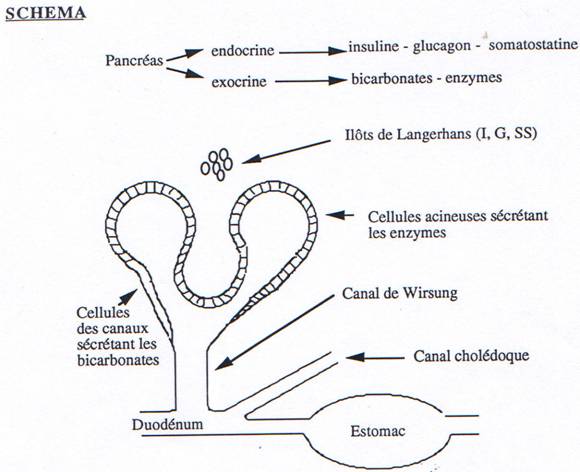
Comme la quantité de bicarbonates sécrétés par le pancréas est contrôlée de façon réflexe par la quantité d’acide qui pénètre dans le duodénum en provenance de l’estomac, la quantité de HCO3- sécrétée par le pancréas est approximativement normalement égale à la quantité d’acide sécrétée par l’estomac. Ceci signifie que les HCO3- libérés dans le sang sont normalement égaux à la quantité d’acide libérée dans le sang par le pancréas. (Diarrhée = perte d’HCO3- = accumulation d’acide dans le sang ; idem vomissements ; donc alcaliniser le sang).
Plusieurs enzymes cependant sont sécrétées sous forme actives (lipase - amylase) mais ont besoin d’ions et de sels biliaires pour avoir une activité maximale.
c Bile (Foie).
La sécrétion biliaire est sécrétée au taux de 0,5l /24 h. La bile est sécrétée par le foie ; puis elle est excrétée par les voies biliaires dans le duodénum.
1 Composition.
La bile est un liquide jaune, ambré, qui verdit par oxydation, ; elle est constituée de plusieurs éléments:
- soluté aqueux d’ions : Na+, K+, Ca2+, Cl-, CO3H-.
- substances organiques : pigments, protéines, mucus ;
- lipides comme les sels biliaires (70 %), les lécithines (25 %) et le cholestérol (5%).
Parmi les pigments, il faut citer la bilirubine, fabriquée par le foie à partir de l’hème de l’hémoglobine issue de la lyse des vieilles hématies. Le cholestérol et les lécithines émulsifient les lipides.
Les sels biliaires sont importants sur le plan physiologique : ils sont synthétisés à partir des acides taurocholique et glycocholique, qui sont fabriqués par le foie, à partir des acides cholique et désoxycholique, qui ont une partie hydrophile et qui sont conjugués à deux acides aminés, la taurine et le glycocolle, pour être encore plus hydrophiles. Les sels biliaires jouent le rôle de détergents qui, par la formation de micelles, solubilisent les lipides dans l’eau ; ils sont en partie réabsorbés par l’intestin et reviennent au foie par la veine-porte ; ils sont ensuite réutilisés grâce au cycle ENTERO-HEPATIQUE.
2 Régulation de la sécrétion.
L’influence du SNV est peu importante ; les crises de foie d’origine psychique sont douteuses ; ce sont surtout les hormones : gastrine, sécrétine et cholécystokinine qui stimulent la vidange de la vésicule biliaire.
3 Rôle.
Grâce aux bicarbonates, la bile participe à la neutralisation du chyme gastrique ; grâce aux sels biliaires, elle permet l’émulsion stable des lipides alimentaires (cholestérol, vitamines liposolubles [A, D, E, K] et lipides) permettant leur absorption. Les sels biliaires augmentent la motricité colique et favorisent la défécation.
d Suc intestinal.
1 Composition.
La muqueuse duodénale sécrète du mucus et des bicarbonates (surtout par les glandes de Brünner), dont le rôle est de protéger la muqueuse et de neutraliser le pH. La muqueuse est très plissée, avec de nombreuses villosités recouvertes d’une couche unicellulaire d’entérocytes, dont le pôle apical est hérissé de microvillosités donnant l’aspect d’une bordure en brosse.
L’activité enzymatique du suc intestinal vient des enzymes libérées par la rupture des cellules desquamées (200 g/24 h). Entre les villosités, s’ouvrent des cryptes, les glandes de Lieberkuhn, dont la paroi est constituée de divers types de cellules :
- cellules à gastrine (Cellules G) ;
- cellules à sécrétine (Cellules S) ;
- cellules à cholécystokinine (Cellules I) ;
- cellules à somatostatine (Cellules D) ;
- cellules à entéroglucagon (Cellules E) ;
- ainsi que d’autres cellules qui sécrèteraient d’autres peptides hormonaux.
Le suc intestinal contient des électrolytes, du mucus et peu d’enzymes, sauf l’entérokinase qui active le trypsinogène.
2 Régulation de la sécrétion.
La sécrétion du suc intestinal est dépendante du SNV. La gastrine déclenche la sécrétion duodénale. La régulation de l’excrétion d’eau et des électrolytes est sous la dépendance, en partie, du système AMPc - adénylate cyclase ; c’est par ce biais qu’interviennent le VIP, la sécrétine et les prostaglandines.
3 Activité digestive de la muqueuse intestinale.
L’activité digestive de la muqueuse intestinale consiste en une série d’hydrolyses, de plus en plus poussées, par des osidases (lactase, maltase, saccharase) et par des peptidases pour donner des oses et des acides aminés. Ces molécules simples (oses ou diosides, acides aminés ou peptides, acides gras ou monoglycérides, eau et électrolytes) ont des tailles et des caractéristiques physico-chimiques compatibles avec l’absorption intestinale.
3 « Digestion » dans le gros intestin (côlon).
Du fait de l’absorption digestive, le côlon reçoit seulement un mélange encore liquide, qui correspond aux résidus alimentaires (fibres de cellulose) et aux cellules intestinales desquamées.
a Motricité colique et défécation.
Le côlon comprend 3 segments le côlon ascendant droit, le côlon transverse, et le côlon descendant gauche ; puis il débouche dans le rectum par le côlon sigmoïde.
L’innervation du côlon droit et des 2/3 du côlon transverse est parasympathique par le nerf vague ; elle est orthosympathique par le nerf splanchnique ; le reste est innervé par les nerfs pelviens (ou érecteurs) cholinergiques et par des nerfs hypogastriques adrénergiques.
Les mouvements de segmentation sont très lents et non propulsifs ; ils permettent au bol de séjourner dans le côlon, de 18 à 24 h, pour que les bactéries se multiplient. Deux à trois fois par jour, la motricité s’accroît pour donner des contractions en masse, dans le côlon ascendant et dans le côlon transverse, poussant ainsi le bol vers le côlon descendant, dont les mouvements péristaltiques amènent les fèces au rectum. La distension du rectum sous l’effet des fèces déclenche le réflexe de défécation.
Ce réflexe de la défécation est surtout le fait des plexus locaux. La réponse est une contraction de la musculature rectale avec relâchement du sphincter anal et accélération du péristaltisme du côlon pelvien. La défécation et momentanément aidée par une augmentation de la pression abdominale, obtenue par la contraction des muscles du thorax et de l’abdomen, après une profonde inspiration et fermeture de la glotte. La défécation est un réflexe conditionnable (le journal) et sujet à des croyances (si on ne va pas à la selle une fois par jour, on s’intoxique par les bactéries qui prolifèrent).
Remarque : on a relaté le cas d’un sujet qui a passé un an sans aller à la selle, sans pathologie, sauf un inconfort évident (environ 25 à 30 kg de selles, au lieu des 150 g/j habituels).
b Phénomènes chimiques dans le côlon.
La muqueuse du côlon est lisse; sa surface est creusée de cryptes; il y a peu de villosités, mais de nombreuses cellules à mucus ; sécrétion aqueuse peu abondante, alcaline car riche en bicarbonates ; absence d’enzymes digestifs. Du mucus et les bicarbonates enrobent les selles, dont le pH de surface est neutralisé ; les selles liquides ou molles sont mal neutralisées et irritantes pour les muqueuses.
Le système cholinergique renforce la sécrétion colique et le système adrénergique la réduit.
Le côlon est surtout un lieu où se parfait la réabsorption de l’eau et des électrolytes.
Chapitre 4 : La Circulation.
I Introduction.
La circulation sert au maintien de l’homéostasie. C’est le sang, phase circulante du milieu interne, qui va en déterminer le réglage.
La circulation a un rôle dans :
- La nutrition (distribution des nutriments),
- le transport des gaz respiratoires (O2 et CO2),
- l’élimination des déchets,
- le transport des informations (hormones),
- l’équilibrage de la température,
- la défense de l’organisme.
Le sang est distribué par le cœur vers les vaisseaux. L’ensemble du sang, des vaisseaux et du cœur forment l’appareil cardio-vasculaire.
Remarque : la circulation lymphatique est un système de drainage qui participe à la défense de l’organisme. Elle fonctionne sans pompe mais avec les vaisseaux. La lymphe rejoindra la circulation sanguine.
Le système cardio-vasculaire est clos (pas de contact direct entre le sang et les cellules). Il se ramifie en artères (1/5 du volume sanguin), veines (2/3 du volume sanguin) et capillaires qui relient les artères aux veines et assurent les échanges entre le sang et les tissus.
A La grande circulation (ou générale).
Elle permet l’irrigation des différents organes et des tissus. Le cœur gauche propulse le sang dans l’aorte, dans les artères, les artérioles, les capillaires, les veinules puis les veines qui ramènent le sang au cœur droit.
Le système est exclusivement composé de sang veineux. Il récupère le sang du tube digestif vers le foie où il est épuré. Il rejoint la grande circulation par la veine sus-hépatique au niveau de la veine cave.
B La petite circulation (ou pulmonaire).
Elle se charge des échanges entre l’air alvéolaire et le sang. Ce dernier est ramené (au cœur gauche) par quatre veines pulmonaires.
II Physiologie cardiaque.
A Anatomie.
Le cœur est un muscle creux qui par sa contraction rythmique assure la progression du sang dans les vaisseaux : c’est une pompe.
Il repose sur le diaphragme et est composé de quatre cavités.
Il est divisé longitudinalement en deux parties indépendantes. Le cœur gauche est le plus puissant car il doit irriguer tout le corps.
On trouve la cloison inter-auriculaire entre les oreillettes et la cloison inter-ventriculaire entre les ventricules.
Pendant le développement embryonnaire, il existe une communication entre les oreillettes.
1 La paroi du cœur.
Le cœur est enfermé dans un sac protecteur : le péricarde. Celui-ci est formé de deux feuillets séparés par une cavité. Le premier feuillet, externe, permet l’attachement au diaphragme : péricarde pariétal. Le deuxième feuillet, interne, est appelé péricarde viscéral ou épicarde, c’est un simple épithélium.
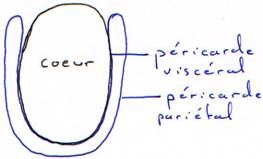
Le myocarde : il forme la paroi des ventricules et des oreillettes. Il est composé de plusieurs couches cellulaires. On trouve des couches musculaires transversales et obliques.
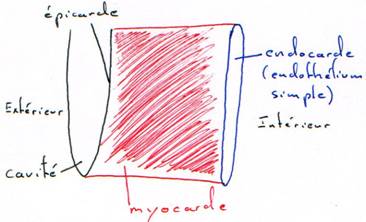
2 Les valvules.
Les valvules forment une zone de transition entre oreillette et ventricule et entre ventricule et artère. C’est un ensemble conjonctif (comme une membrane). Elles ont une fonction de clapet.
A partir de ces valvules partent des cordages fibreux ou tendineux. Ces cordages se rattachent à des muscles papillaires.
La valvule auriculo-ventriculaire du cœur gauche est appelée valvule mitrale. La valvule du cœur droit est appelée valvule tricuspide.
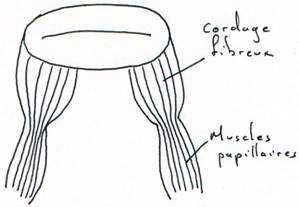
Les valvules sigmoïdes ou semi-lunaires, situées au niveau du départ des artères résistent à de fortes pressions. Elles permettent d’éviter le retour du sang. Quand elles ne peuvent pas se fermer, on parle du « souffle au cœur ».
3 La circulation coronaire.
Le cœur a son propre système de vascularisation qui forme une couronne autour du cœur. Les deux artères coronaires partent de la base de l’aorte. La gauche prend en charge 85% du débit sanguin irriguant le cœur et la droite, seulement 15%. Le sang revient par des veines qui se jettent dans le sinus veineux qui rejoint le cœur au niveau de l’oreillette droite.
B Révolution cardiaque.
La révolution cardiaque comprend tous les phénomènes à partir du début d’une contraction cardiaque jusqu’au début de la suivante. Cette révolution peut être divisée en quatre phases.
- 1 : remplissage des ventricules (droit et gauche) ; cœur relâché : diastole.
- 2 : les ventricules se contractent ; début de la systole.
- 3 : éjection du sang.
- 4 : relâchement ventriculaire : diastole.
Le cœur est relativement « fainéant » car il se repose plus qu’il ne travail.
1 Mise en évidence du fonctionnement cardiaque.
Il existe des signes externes de l’activité cardiaque : le pouls, les bruits du cœur (les bruits sourds sont dus aux valvules auriculo-ventriculaire « toum », les bruits secs sont dus aux valvules sigmoïdes « ta »).
Un électroencéphalogramme permet d’analyser l’activité électrique du cœur : il se dégage une onde particulière.
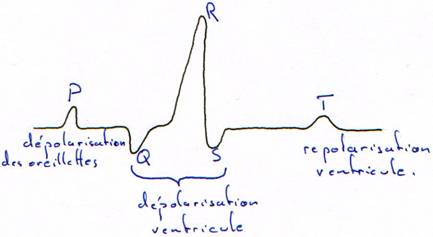
2 Automatisme cardiaque.
Un cœur séparé de son organisme et convenablement perfusé peut se contacter pendant des heures : le cœur a son propre fonctionnement : on parle d’activité intrinsèque. Cet automatisme est régulé par le système neurovégétatif.
A l’intérieur, le tissu nodal est responsable de l’activité cardiaque. Il est représenté par 1% des cellules cardiaques. Elles sont situées dans les parois du cœur.
Ce tissu prend son départ au niveau de l’oreillette droite (le nœud sion-auriculaire ou nœud sinusal ou nœud de Keith et Flack). Il initie la fréquence cardiaque : le pacemaker (100 battements par minute).
L’influx nerveux part ensuite au fond de l’oreillette par une jonction en arc ventriculaire jusqu’au nœud auriculo-ventriculaire ou nœud de Aschoff Tawara.
Cet influx continue par le faisceau de His, dans la cloison inter-ventriculaire. Il se divise ensuite en deux branches qui se ramifient à la pointe des ventricules et donnent le réseau de Parkinge.
C Débit cardiaque et régulation.
1 Débit cardiaque, définition.
Le débit cardiaque est volume de sang pompé par caque ventricule par unité de temps. Il dépend donc de la fréquence cardiaque et du volume d’éjection systolique (exprimé en L/min).
Dc = Fc × Vs (à 5L/min = 70 bpm × 70 mL/min).
Pour les calculs, on considère essentiellement le volume du ventricule gauche.
750 mL iront vers le cerveau, 250 mL vers le cœur, 1,1 L vers les reins et 1,2 L vers les muscles. Pendant un exercice, le volume de sang allant vers les muscles augmente, celui allant vers le système digestif diminue.
2 Régulation.
On a trois types de régulation : Intrinsèque, Extrinsèque et Hormonale.
a Régulation intrinsèque.
Elle concerne le cœur. Il adapte son débit au retour veineux : une augmentation de sang veineux entraîne une élévation de sang éjecté (amplification du travail cardiaque).
Loi de Starling : plus le muscle est étiré, plus le travail cardiaque est important.
b Régulation extrinsèque.
Le système neurovégétatif module l’activité du cœur en fonction de l’activité générale de l’organisme.
- Système cardio-modérateur (système parasympathique). Le médiateur est l’acétylcholine. Il implique le nerf vague dont la stimulation va diminuer la fréquence cardiaque au niveau du nœud auriculo-ventriculaire.
- Système cardio-accélérateur (système orthosympathique). Le médiateur est la noradrénaline. Toutes les stimulations du système orthosympathique vont accélérer la fréquence cardiaque.
c Régulation hormonale.
L’adrénaline sera activée par les glandes médullo-surrénales en condition de stress. Son effet sera une accélération du rythme cardiaque.
Les hormones thyroïdiennes sont aussi capables d’augmenter la fréquence cardiaque.
d Autres facteurs.
L’hypothermie fait ralentir le rythme cardiaque alors que la fièvre l’augmente.
III Physiologie des vaisseaux.
A Caractères généraux.
1 Les artères.
Les artères sont constituées de trois couches :
- l’intima : endothélium
- la média : formée de fibres élastiques et de fibres musculaires lisses
- l’adventice : formée de fibres élastiques et de fibres conjonctives.

Selon le type d’artère, on a une variation des fibres musculaires et élastiques.
Plus les fibres sont grosses, plus le nombre de fibres élastiques augmente
Plus les fibres sont petites, plus le nombre de fibres musculaires augmente.
 Ces variations mettent en évidence la vasomotricité qui régule le débit sanguin pour un organe donné.
Ces variations mettent en évidence la vasomotricité qui régule le débit sanguin pour un organe donné.
2 Les veines.
Elles contiennent les mêmes couches que les artères mais les parois sont beaucoup plus minces. Leur média comporte beaucoup moins de fibres élastiques et musculaires è la média est moins développée dans les veines que dans les artères.
L’intima forme des replis qui donneront des valvules anti-reflux à circulation en sens unique vers le cœur. Ces valvules seront surtout présentes dans les membres inférieurs.
3 Les capillaires.
Ils sont formés d’une paroi mince (une seule couche de cellules endothéliales). La circulation sanguine, dans ces vaisseaux, est à faible vitesse afin de permettre les échanges entre les deux compartiments. Les échanges sont faits par diffusion.
4 Les vaisseaux lymphatiques.
Le liquide interstitiel est drainé et filtré par les vaisseaux lymphatiques qui passent dans tous les organes. Ce liquide est composé de liquide sanguin en excès. Sa composition est comparable à celle du plasma (ni hématies ni plaquettes). Les capillaires lymphatiques sont disposés en réseaux concentrés, puis en canaux et enfin en veine. La lymphe est collectée par deux grands collecteurs :
- la grande veine lymphatique : elle recueille le liquide interstitiel venant de la tête, du cou et des membres supérieurs. Elle se jette ensuite dans la veine sous-clavière droite.
- le canal thoracique : il collecte le liquide interstitiel de tout le reste du corps. Il se jette finalement dans la veine sous-clavière gauche.
La lymphe rejoint ensuite la circulation sanguine.
Remarque : les canaux lymphatiques au niveau de l’intestin sont appelés les canaux chylifères.
B Fonctionnement du système circulatoire.
1 Définition, systèmes basse pression et haute pression.
L’écoulement du sang se fait toujours d’une région de haute pression vers une région de basse pression.
· Système haute pression. Il est composé du cœur gauche, de l’aorte et des artères systémiques. La pression est de 100 mm de Hg. On a donc un écoulement rapide du sang vers les organes. Ce système rassemble 20% de la masse sanguine. Il permet de faire face à des variations locales de débit.
· Le système basse pression. Il est composé du cœur droit, de la circulation pulmonaire, des veines systémiques et des capillaires. La pression est de 15 mm de Hg. Ce système comprend 80% de la masse sanguine. Il sert aux échanges avec les organes.
2 Circulation dans un système à haute pression.
a Notion de débit et de pression.
Haute pression : Assure un transport rapide du sang vers les organes.
L’écoulement du sang est fonction du débit et des résistances à l’écoulement de ce sang (viscosité et diamètre des vaisseaux).
Débit : C’est la variation de pression entre deux points et de la résistance à l’écoulement.
 Q= dP/R
Q= dP/R
b Elasticité.
L’élasticité est une caractéristique importante des grosses artères : elles renferment beaucoup de fibres élastiques (plus que de musculaires). L’élasticité sert à amortir l’amplitude des variations de pression : elle sert à la régulation du débit à un organe donné.
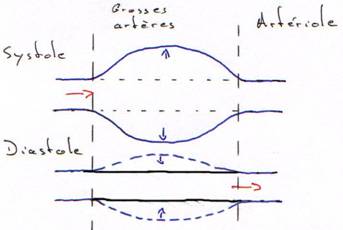
Le flux discontinue à la sortie du cœur se transforme en un flux continue grâce à l’élasticité des artères.
La tension maximale pendant la systole est comprise entre 110 et 140 mm de Hg.
La tension minimale pendant la diastole est comprise entre 60 et 80 mm de Hg.
La différence entre ces deux valeurs donne la tension différentielle.
c La vasomotricité.
La vasomotricité s’intéresse aux artères moyennes et aux artérioles (elles possèdent plus de fibres musculaires que de fibres élastiques).
Cette vasomotricité est contrôlée de deux façons :
- contrôle local qui s’exerce sur les fibres musculaires lisses de la paroi des artérioles, déclenché par une diminution locale de la pression artérielle qui entraîne une réduction du débit des capillaires et des taux d’oxygène. On a alors une contraction réflexe des artérioles.
Le contrôle local est du aux concentrations en O2, CO2 et autres métabolites : c’est une auto-régulation du débit sanguin vers les organes.
- voie nerveuse. L’activité des fibres du système orthosympathique va activer la contraction des artérioles. La fixation de la noradrénaline sur les récepteurs a et b adrénergiques entraîne deux résultats différents : quand le récepteur a est activé, on a une vasoconstriction et une vasodilatation si le récepteur b est activé.
Ce double contrôle intègre les variations au niveau global de l’organisme.
Remarque : les hormones : l’angiotensine permet la vasoconstriction. L’ANF (Facteur Atual natriurétrique) produit par le cœur est un vasodilatateur.
d La pression artérielle et sa régulation.
P = Dc × R (pression = débit cardiaque × résistances)
Cette pression est ajustée en permanence. Elle est dépendante de l’efficacité du cœur, du volume sanguin et du calibre des vaisseaux (vasomotricité).
La pression est régulée en permanence et de façon immédiate par la régulation nerveuse. Sur un plus long terme, on a une régulation hormonale.
· Régulation nerveuse.
Dans les parois du sinus veineux et de l’aorte, on trouve des récepteurs sensibles aux changements de pression. Ils sont dans des zones barosensibles dans la crosse aortique et la bifurcation carotidienne : ce sont les barorécepteurs.
L’information remonte au bulbe par des voies afférentes sensibles représentées par les nerfs de Cyon et de Hering.
Ces voies ont toujours un rôle de « frein » sur l’activité cardio-vasculaire.
Quand les centres cardio-vasculaires sont informés, ils envoient les informations au cœur et aux vaisseaux par les fibres efférentes du système parasympathique et du système orthosympathique.
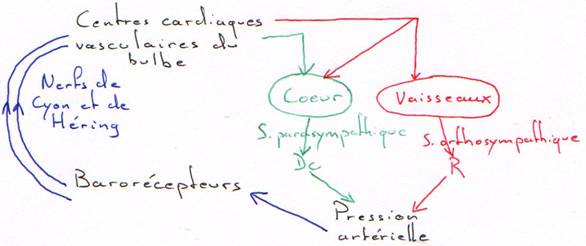
Une diminution de la pression artérielle entraîne une augmentation de la stimulation du système parasympathique (qui va accélérer la fréquence cardiaque) et une diminution de l’activité du système orthosympathique (qui diminuera son action vaso-constrictrice).
· Régulation hormonale.
Pour réguler le volume sanguin, on trouve des volo-récepteurs (sensibles au volume).
L’intervention d’hormone joue sur la volémie :
- L’ADH (vasopressive ou anti-diurétique) est sécrétée par la post-hypophyse. Elle est libérée après une stimulation des récepteurs. Elle va compenser le volume sanguin avec le volume urinaire.
- L’ANF.
- La Rénine, sécrétée par le rein, elle permet de transformer l’angiotensine pour être activée. Quand elle est active, elle entraîne une vasoconstriction des artérioles qui va modifier la pression artérielle. La Rénine peut provoquer la sécrétion d’aldostérone par le complexe surrénalien.
Une diminution de l’activité du système parasympathique entraîne une diminution de l’inhibition cardiaque qui permet l’augmentation de la fréquence cardiaque.
L’accroissement de l’activité du système orthosympathique entraîne une augmentation de la pression cardiaque.
3 Circulation dans le système à basse pression.
a Au niveau des capillaires.
Ce sont les segments spécialisés dans les échanges entre les tissus et le sang. Leur paroi permet la filtration des nutriments, de l’oxygène et des hormones vers le liquide interstitiel ainsi que de réabsorber les produits du métabolisme (CO2, déchets azotés).
Le réseau de capillaires forme un entrelacement de 50 km de long. Toutefois, tous les capillaires ne sont pas fonctionnels en même temps. Dans un organe au repos, le sang circule dans 5% des capillaires. La modulation du passage sanguin est due à des sphincters pré-capillaires. Ils sont situés à la terminaison des artérioles. Ils contrôlent l’adaptation des échanges en fonction des cellules. La distance entre les cellules et le capillaire est de 100 µm.
Deux forces jouent un rôle dans les échanges :
- la variation de la pression hydrostatique (mouvements d’eau).
- la variation de pression osmotique.
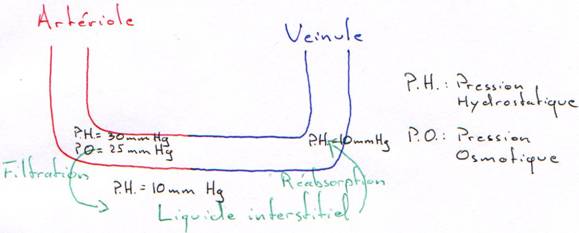
90% du liquide interstitiel filtré est réabsorbé. Les 10% restant sont pris en charge par la circulation lymphatique.
b Au niveau des vaisseaux lymphatiques.
Deux litres par jour de liquide interstitiel sont pris par les vaisseaux lymphatiques (les 10%). La lymphe rejoint ensuite la circulation veineuse.
c La circulation veineuse.
Elle collecte le sang des capillaires pour le ramener au cœur droit. C’est elle qui maintien la réserve sanguine, disponible en cas de nécessité.
Il n’y a pas de fibre musculaire pour ramener le sang au cœur. C’est l’activité du cœur (aspiration quand il se contracte) qui fait remonter le sang.
Les mouvements respiratoires entraînent une compression du diaphragme qui va comprimer les veines et faire remonter le sang au cœur par aspiration.
L’activité contractile des muscles fait aussi remonter le sang vers le cœur.
Les valvules anti-reflux facilitent la remontée de ce sang.
 Ce sont tous des facteurs extérieurs aux vaisseaux.
Ce sont tous des facteurs extérieurs aux vaisseaux.
Chapitre 5 : La Respiration - Les Echanges Gaezux.
Partie 1: La Respiration.
I Introduction.
Le but de la respiration est d’amener l’oxygène à toutes les cellules de l’organisme en fonction de leurs besoins et de prendre en charge le CO2 rejeté.
L’oxygène sert au processus d’oxydation au niveau des mitochondries.
II L’appareil respiratoire.
Cet appareil respiratoire est composé des voies aériennes qui relient l’air atmosphérique à l’air alvéolaire des poumons.
A Les voies aériennes.
Du milieu extérieur, l’oxygène passe dans le tractus respiratoire par les fosses nasales, le pharynx, le larynxtrachée et les bronches (primaires qui se ramifient en bronchioles avec des fibres musculaires). (début de la trachée), la
Ces voies ont un rôle conducteur mais servent aussi à réchauffer, hydrater et dépoussiérer l’air. Cette dernière fonction est prise en charge par des cellules sécrétrices dont le mucus piège les différentes particules. On a aussi des cellules ciliées qui déplacent ces particules vers le pharynx.
B Les poumons.
Les poumons sont limités ventralement par le diaphragme. Ils sont divisés en lobes (3 à droite et 2 à gauche). Ils sont enveloppés par un feuillet viscéral contre les poumons et par un feuillet pariétal qui tapisse la paroi thoracique.
Entre les deux feuillets se situe la cavité pleurale qui est remplie d’un liquide qui joue un rôle protecteur.
Dans un lobe de poumon, on trouve :
- une bronche primaire,
- des bronches secondaires,
- des bronches tertiaires et
-des bronchioles à l’extrémité desquelles on trouve les sacs alvéolaires.
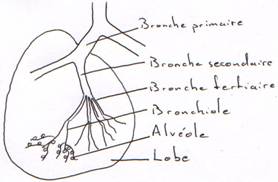
On parle d’arbre bronchique.
La paroi des alvéoles est fine (une couche de cellules épithéliales) et très vascularisée.
Les cellules de la paroi sont des pneumocytes. On distingue deux groupes de pneumocytes : les primairessecondaires qui sécrètent un liquide (le surfactant), mélange de phospholipides (90%) et de protéines (10%), qui va former un film à la surface des alvéoles. Ce sont des substances tensioactives. Ce liquide évite aux alvéoles de se replier sur elles-mêmes et facilite les échanges entre les deux compartiments. et les
Le gaz se diffuse à travers la paroi dont la surface totale est très importante (300 millions d’alvéoles par poumon), autour de 70 m2 par poumon.
III Mécanique respiratoire et ventilation.
Le but de cette respiratoire est d’assurer la ventilation des parties profondes des poumons afin de renouveler l’air.
La ventilation correspond aux mouvements d’air à l’intérieur et à l’extérieur des poumons (inspiration et expiration).
Le renouvellement de l’air est dépendant des différences de pression entre l’air extérieur (atmosphérique) et l’air intra-alvéolaire.
Inspiration : La pression est de 760 mm de Hg dans les poumons (plus faible que la pression atmosphérique).
Expiration : la pression des poumons est supérieure à la pression atmosphérique et l’air est expulsé.
A Inspiration.
L’inspiration est un phénomène actif. La variation de volume est due aux mouvements de la cage thoracique. Les muscles intercostaux externes se contractent et les muscles relevant les côtes se contractent. On a ainsi une augmentation du volume de la cage thoracique sur un plan horizontal.
Le diaphragme se contracte, donc s’abaisse. Le volume augmente sur un plan vertical.
Les poumons suivent passivement les mouvements de la cage thoracique car ils sont solidaires de la cage thoracique.
B Expiration.
L’expiration est un phénomène passif. Les muscles contractés se relâchent et le diaphragme remonte. Le volume de la cage thoracique diminue. Les poumons reprennent leur volume initial.
Grâce à la différence de pression, l’air est expiré.
Remarque : les expirations forcées sont des phénomènes actifs qui demandent la contraction des muscles intercostaux internes et des muscles abdominaux.
Cette mécanique peut être étudiée par un spiromètre (appareil qui permet aussi la détection de l’asthme).
Quand 500 mL d’air rentrent, seuls 350 mL pénètrent dans les alvéoles. L’air en surplus reste dans les voies aériennes qui sont dites « espace respiratoire morte ».
On a 7,5 L d’air inspiré par minute et 450 L inspiré par heure.
IV Régulation de la respiration.
La succession de cycles respiratoires permet de déterminer un automatisme ventilatoire. Il est du à des neurones situés dans le bulbe qui constituent les centres respiratoires (inspirateur et expirateur). Ces nerfs (moteurs et phréniques) innervent les muscles respiratoires (diaphragme et intercostaux).
Les stimuli sensitifs partent des poumons, passent par le nerf vague et vont informer les centres respiratoires sur l’état d’inflation.
A Influence des stimuli chimiques.
Le rythme et l’amplitude des mouvements respiratoires sont réglés par des variations de paramètres sanguins (pression partielle en CO2, O2 et pH).
Ces paramètres sont perçus par des chémorécepteurs. Les chémorécepteurs centraux (au niveau du bulbe) sont sensibles aux variations de pH du liquide céphalo-rachidien).
Une augmentation de la concentration en CO2 entraîne l’augmentation de la ventilation.
Les barorécepteurs, au niveau de la crosse aortique et de la bifurcation carotidienne, sont sensibles à la pression partielle en CO2.
è L’augmentation de la pression partielle en CO2 ou la diminution de celle en O2 entraîne l’augmentation de la ventilation.
B Autres influences.
- Etat d’activité (sommeil, exercices physiques, repos …)
- Volonté
- Emotions
- Toux
- Eternuements
- Douleurs.
Au niveau des bronchioles, les muscles lisses sont sensibles à la pression partielle en CO2 : si la quantité de CO2 augmente, les muscles lisses se relâchent en entraînant une broncho-dilatation et l’excès de CO2 est expiré.
Partie 2: Les échanges gazeux.
I Propriété fondamentale des gaz.
A Pression atmosphérique.
La pression atmosphérique correspond à la pression au niveau de la mer.
760 mm Hg ó 1013 hPa. Cette pression diminue avec une augmentation d’altitude.
B Pression partielle.
La pression partielle est la pression exercée par les molécules d’un gaz donné dans un mélange de gaz.
Au niveau de la mer, on a :
- 21% d’O2 ó PO2 = 158,8 mm Hg,
- 0,03% de CO2 ó PCO2 = 0,23 mm Hg,
- 78,97% de N2 ó PN2 = 601 mm Hg.
La diffusion des gaz respiratoires est effective seulement si les gradients de pression partielle en O2 et CO2 sont maintenus de part et d’autre de la surface d’échange. Ceci est possible grâce au renouvellement permanent du sang (par le cœur) et de l’air alvéolaire (par la ventilation).
Cette diffusion dépend de la solubilité des gaz dans un liquide.
A l’équilibre, la pression partielle d’un gaz est équivalente dans l’air ou dans l’eau.
Loi de Henry : la quantité de gaz qui se dissout dans un liquide est directement proportionnelle à la pression partielle du gaz et de son coefficient de solubilité (à température constante). Si la température augmente, la quantité de gaz dissout diminue.
Remarque : le CO2 est 23 fois plus soluble que l’oxygène.
II Le mélange gazeux moléculaire.
A L’air inspiré.
C’est un mélange en O2, CO2 et N2. Quand l’air arrive dans les voies respiratoires, il devient saturé en vapeur d’eau, ce qui entraîne une modification de la pression partielle de chacune des molécules de gaz.
La pression intra-pleurale joue un rôle dans l’inspiration. Elle diminue pendant l’inspiration et permet à l’air de rentrer dans les poumons (elle augmente quand l’air est expiré).
B L’air alvéolaire.
Le sang s’équilibre avec l’air alvéolaire qui contient : 14% d’O2 (PO2=105mm Hg), 5,5% de CO22=40mm Hg). (PCO
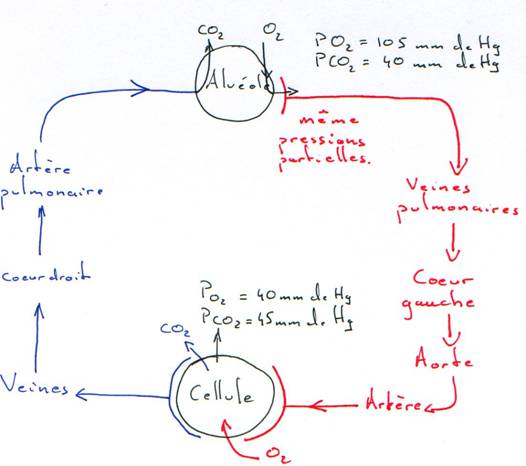
III Transport de l’oxygène.
A L’O2 dissout.
0,3 mL d’O2 est dissout pour 100 mL de sang. C’est insuffisant pour couvrir les besoins cellulaires (20 mL d’O2 sont nécessaires pour 100 mL de sang).
B L’O2 combiné.
L’O2 se combine à l’hémoglobine de façon réversible en fonction de la pression partielle en O2 à un niveau donné.
L’hémoglobine : C’est une protéine des hématies, constituée de quatre sous-unités, chacune formée d’une chaîne polypeptidique (la globine) à laquelle est fixé un hème (Fe2+) qui fixe l’O2. Chaque molécule d’hémoglobine peut fixer quatre molécules d’O2.
Quand l’O2 est fixé, on parle d’oxyhémoglobine.
On a à peu près 15g d’hémoglobine pour 100mL de sang et 1g d’hémoglobine fixe 1,39mL d’O2.
La pression partielle en O2 est le principal facteur de fixation de l’O2. L’affinité de l’hémoglobine est élevée au niveau alvéolaire pour l’O2 : on parle d’hémoglobine saturée (à 90%).
Au niveau cellulaire, le pourcentage de saturation est de 75% : il y aura, à ce niveau, libération d’O2 plus facile pour qu’il puisse rentrer dans la cellule.
Le 2,3 diphosphoglycérate est un glucide produit par les hématies.
IV Transport du CO2.
A Le CO2 dissout.
2,5 à 3mL de CO2 sont dissous pour 100mL de sang. Un litre de sang contient 500mL de CO2. Ce type de transport représente 10% du total de CO2 transporté.
B Transport combiné du CO2.
· Le CO2 peut se combiner à l’eau et donner de l’acide carbonique.
CO2 + H2O <-> H2CO3 <-> HCO3- + H-.
Dans les hématies, on a une enzyme, l’anhydrase carbonique, qui accélère la formation des ions HCO3-. Ces ions vont diffuser dans le plasma en faisant rentrer des ions Cl- dans les hématies. è 60% du CO2 est transporté sous cette forme.
· Combinaison avec l’hémoglobine.
L’hémoglobine peut fixer et libérer le CO2 au niveau des globines, on parle alors de carbamino-hémoglobine.
Au niveau des tissus, la libération de CO2 entraîne une diminution du pH qui tend à dissocier l’O2 de l’hémoglobine.
La libération d’un proton donne une recombinaison de HCO3- puis une dissociation en H2O + CO2 qui sera évacué.
Chapitre 6 : L’excrétion.
I Introduction.
Les reins font parti du système excréteur. Leur rôle est le maintien de l’homéostasie par régulation du volume et de la composition du milieu intérieur : contrôle de l’équilibre hydrominéral et acido-basique.
Les reins assurent l’épuration du sang en éliminant les déchets métaboliques qui seront excrétés par le système urinaire.
Les reins produisent la rénine et l’érythropoïétine. Elles stimulent la formation des hématies.
II Anatomie.
A Appareil urinaire.
Les reins sont disposés en position rétro-péritonéale. A cause du foie, le rein droit est plus bas que le rein gauche.
Le rein est entouré d’une gaine conjonctive (capsule rénale).
La zone externe est la zone corticale ou cortex.
La zone interne est la zone médullaire ou medulla.
Dans la medulla, on a des structures pyramidales (les pyramides de Malpighi), au nombre d’une quinzaine, à l’extrémité desquelles se trouvent les pores urinaires qui débouchent dans un tube (le petit calice). On a autant de petits calices que de pyramides. Ils se regroupent par 5 pour former les grands calices (3 grands calices). Ils débouchent sur le bassinet (point de départ de l’uretère). On y trouve la veinel’artère rénale. Toutes ces formations sont présentes au niveau du repli du hile. et
Ces voies urinaires sont constituées des calices, du bassinet, des uretères et de la vessie. La paroi des uretères est composée de trois couches :
- La muqueuse : elle sécrète le mucus qui a un rôle contre l’acidité de l’urine.
- La couche musculaire : elle est formée de fibres circulaires et longitudinales qui permettent les mouvements péristaltiques.
- Les tissus conjonctifs et adipeux.
La vessie a une position différente chez les hommes ou chez les femmes. Elle est constituée de quatre couches :
- Une muqueuse,
- Une sous-muqueuse,
- Des muscles lisses très puissants : le détrusor. On trouve les muscles longitudinaux et circulaires qui forment un sphincter interne. On a aussi un sphincter externe constitué de fibres musculaires striées.
- Une séreuse dans la partie supérieure de la vessie (essentiellement).
Le volume de cette vessie est 300 mL mais elle est extensible.
La miction est la vidange de la vessie, sous le double contrôle nerveux du système végétatif (réflexe) et du système nerveux central (volontaire). Pour l’activité réflexe, les récepteurs à l’élongation active le système parasympathique qui va entraîner la contraction de la vessie et le relâchement du sphincter interne. Le système nerveux central agit sur le sphincter externe.
L’urètre transporte l’urine à l’extérieur du corps. Elle prend son départ à la base de la vessie, au niveau du trigome. L’urètre est différent selon le sexe de l’individu. Chez l’homme, c’est un conduit urogénital de 20 cm et chez la femme, c’est un conduit exclusivement urinaire de 4 cm de long.
B Les néphrons.
Le néphron est l’unité structurale et fonctionnelle du rein. On trouve plus d’un million de néphrons par rein, chez l’homme. Ils se juxtaposent entre eux pour former les pyramides. On a deux types de néphrons :
- les néphrons corticaux : ils sont courts et situés au niveau du cortex,
- les néphrons juxtamédullaires : ils descendent profondément jusqu’à la médulla.
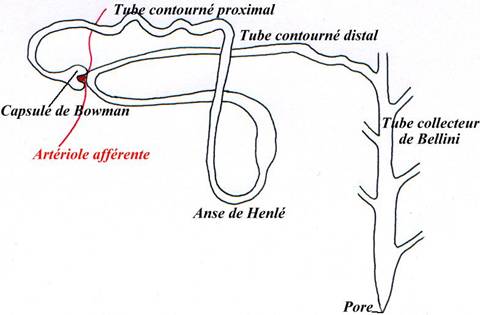
1 La capsule de Bowman.
C’est elle qui compose le segment initial du néphron. Elle est formée d’une double paroi à cellules aplaties (feuillet viscéral et feuillet pariétal).
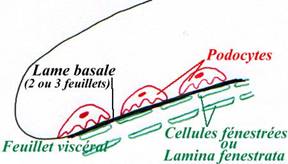
>Dans la concavité de la capsule de Bowman arrive l’artériole afférente qui se capillarise en un floculus ou glomérule de Malpighy. (capsule de Bowman + flocules = corpuscule de Malpighy)
2 Le tube contourné proximal.
Il est caractérisé par des cellules en brosse (grande capacité de réabsorption).
C’est un tube en « U » avec une branche descendante grêle et une ascendante grêle qui s’élargit ensuite.
Les néphrons peuvent être profonds ou superficiels. Il se forme alors un gradient cortico-papillaire.
La branche descendante de Henlé est relativement imperméable au sodium et perméable à l’eau. C’est l’inverse pour la branche ascendante.
3 Le tube contourné distal.
Ce tube fait parti de l’appareil juxtaglomérulaire. Il est formé de l’artériole afférente, l’artériole efférente et de la pars maculata.
Ce tube est l’appareil producteur de rénine. Le facteur déterminant de la rénine est la diminution de la concentration en sodium du sang.
4 Le tube collecteur de Bellini.
Ce tube traverse totalement la pyramide, il reçoit d’autres tubes collecteurs. Il débouche dans le petit calice correspondant, au niveau d’un pore urinaire.
Le long de son trajet dans le tubule, l’urine subit des modifications de concentrations à cause des échanges entre tubule, tissu interstitiel et vaisseaux sanguins.
C Irrigation.
1 Irrigation générale.
Les deux artères rénales sont issues de l’aorte. Après ramifications successives, on arrive aux artères radiées. Le circuit veineux : on passe des veines radiées aux veines rénales puis à la veine cave inférieure. 1800 litres de sang passent tous les jours dans la circulation générale.
2 Irrigation du néphron.
De l’artère radiée part l’artériole afférente qui se résout en capillaires fénestrés dans la capsule de Bowman.
Le sang repart part l’artériole efférente puis se capillarise autour des tubules. Au niveau de l’anse de Henlé, il existe un réseau artério-veineux : le vasa-recta.
Le système porte artériel permet une augmentation de la filtration. Le système artério-veineux permet, lui, la réabsorption.
III Physiologie de l’urine.
A Généralités sur l’élaboration de l’urine.
L’urine est une solution aqueuse avec des substances minérales et organiques. La densité de l’urine peut passer de 0,002 à 0,03 afin de réguler la volémie.
Cette composition est le résultat de trois étapes fonctionnelles fondamentales (filtration, réabsorption et sécrétion).
La filtration comprend le passage d’eau et de composés du sang vers le tubule.
La réabsorption comprend du tubule vers le sang.
La sécrétion est le passage direct du sang vers le tubule sans filtration ou de la cellule rénale vers l’urine.
Suivant l’intensité de chacun des processus, une substance se trouvera à une concentration plus ou moins grande dans l’urine. Des mécanismes homéostatiques fins régulent ces trois étapes.
B La filtration.
Sur 1800 litres de sang, passant par jour on distingue : 180 litres d’eau, 180g de glucose, 154g d’urée et 630g de sodium.
Le filtrat est isotonique au plasma (300 milliosmol par litre).
La force motrice principale est la pression sanguine (50 à 60 mm de Hg).
Deux forces s’opposent à ce passage :
- la pression oncotique : pression due aux protéines qui ne peuvent sortir des capillaires (20 à 25 mm de Hg)
- la pression capsulaire (10 à 15 mm de Hg).
 PF = PS – (PO + PC) = 10 à 20 mm de Hg.
PF = PS – (PO + PC) = 10 à 20 mm de Hg.
C Réabsorption.
C’est le passage des éléments du filtrat vers le sang. Cette réabsorption a lieu dans la région du tube contourné proximal.
Sont réabsorbés : 85% de l’eau, 85% du sodium, 98% du potassium et 100% du glucose.
1 Le transport actif.
Ce type de transport nécessite un transporteur, de l’O2, de l’ATP. C’est un transport saturable.
2 Le transport passif.
Il suit les lois de l’osmose (cas du sodium, de l’urée).
3 Exemple du glucose.
Le glucose subit un transport actif saturable : on obtient alors un transport maximal.
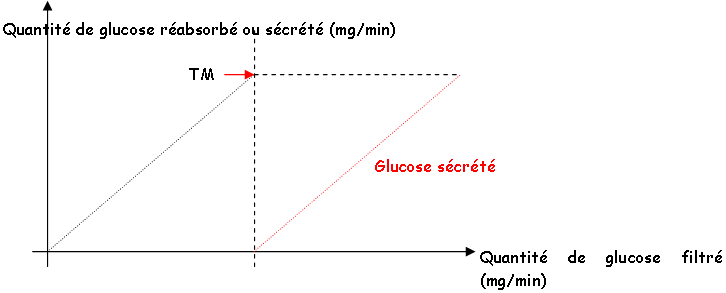
4 Exemple du sodium..
Une partie du sodium passe dans le liquide interstitiel au niveau de la Anse de Henlé. Dans la branche descendante, l’eau sort car il y a beaucoup de sodium. Dans la branche ascendante, le sodium sort. è Il s’établit dans le liquide interstitiel, un gradient osmotique entre la pression corticale et la pression médullaire qui peut aller de 300 millimosmol à 1000 millimosmol (et même 1400 milliosmol sous l’influence régulatrice de l’aldostérone).
Ce sont les néphrons à anse longue qui sont responsables de ce phénomène.
5 Le cas de l’eau.
L’eau permet la régulation de la volémie (ou équilibre hydrominéral). Il y a réabsorption obligatoire de 85% d’eau au niveau de tube contourné proximal mais il reste 10 à 15% d’eau réabsorbée de façon facultative en fonction de l’équilibre hydrominéral. è l’urine est plus ou moins diluée.
Au niveau du tube contourné distal et du tube collecteur de Bellini, il y a réabsorption d’eau à cause de l’ADH et de la nature anatomique (gradient cortico-papillaire).
Dans les conditions normales, 1,5 litres d’urine. Dans des conditions anormales, sous l’influence de récepteurs à l’osmorégularité et à la volémie, la posthypophyse diminue sa sécrétion d’ADH pour perméabiliser les parois du tube contourné distal et du tube collecteur de Bellini à l’eau. L’eau sort grâce au gradient cortico-papillaire.
D Sécrétion.
La sécrétion correspond au passage direct d’une molécule du sang vers le tubule ou des cellules sécrétrices vers le tubule. Fonction exogène : médicaments… ; fonction endogène : H+, K+, acide urique…
Le système Rénine – Angiotensine.
La rénine est sécrétée quand la pression diminue dans l’artériole afférente.
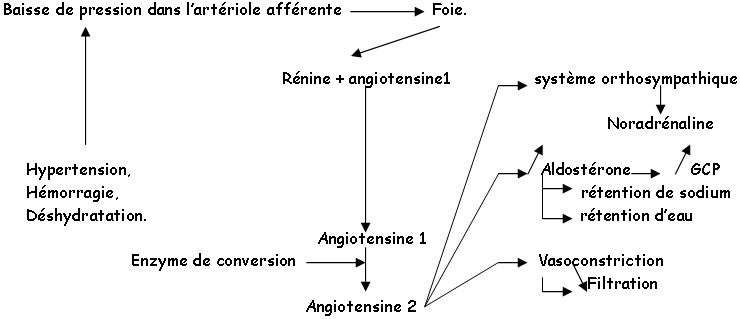
Ce système permet la récupération de l’eau : il a un rôle récupérateur.
Chapitre 7 : Les Appareils Reproducteurs.
L'appareil reproducteur mâle.
I Différenciation sexuelle.
A Différenciation à partir du génome.
Chez les animaux supérieurs, la différenciation sexuelle est fonction du code génétique.
Chez les poissons, cette différenciation est fonction des conditions extérieures (température, ....).
B Le sexe gonadique.
Pendant la vie embryonnaire, il n'y a pas de différenciation sexuelle avant la sixième semaine : on a alors un appareil indifférencié.
Chez le mâle, la différenciation entraîne la formation de tubes séminifères dans les gonades. En même temps on a la différenciation des canaux de Müller et de Wolf. Le canal de Müller donne la trompe utérine chez la femelle et dégénère chez le mâle. Le canal de Wolf donne les canaux déférents qui dégénèreront chez la femelle.
Au départ, la différenciation sexuelle est féminine. Le mâle a besoin de testostérone et des testicules pour synthétiser des hormones anti-müllériennes.
C Le sexe somatique.
Il correspond à la mise en place des structures internes puis des caractères sexuels secondaires qui en découlent. Du sexe génétique, on passe au sexe gonadique, avec la mise en place des organes sexuels, puis, au sexe somatique avec l'apparition des caractères sexuels secondaires et enfin au sexe légal.
II Anatomie.
A Les testicules.
Les testicules ont une double fonction:
- fonction endocrine: production d'hormones du genre de la testostérone.
- fonction exocrine: production de spermatozoïdes.
Les testicules sont coiffés par l'épididyme. Leur partie inférieure est fixée à la paroi du scrotum. Elles sont enfermées dans une capsule riche en tissu conjonctif et en structures musculaires. Ces différentes parties composent l'albuginée qui formera des cloisons dites inter-lobulaires.
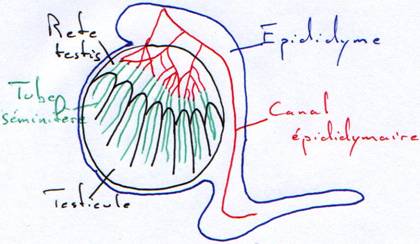
Les tubes séminifères se terminent par les tubes droits qui se jettent dans le Rete testis. Après les tubes droits, on a les canaux efférents qui vont jusqu'à la tête de l'épididyme.
- Irrigation.
L'artère testiculaire est issue de l'artère spermique. Elle forme des circonvolutions autour des testicules tout comme les veines. Ces dernières se mettent sur les artères et donne un système à contre-courant qui permet une circulation inverse afin de refroidir les spermatozoïdes.
- les différents types cellulaires.
On trouve des cellules allongées : les cellules somatiques ou cellules de Sertoli qui ont un rôle nourricier et qui sont capables de synthétiser de l'inhibine.
Les cellules de la lignée germinale : elles donneront les spermatogonies, les spermatocytes 1 et 2 et les spermatides.
A l'extérieur, on a un liquide interstitiel conjonctif lâche qui renferme les cellules de Leydig. Ces cellules sont responsables de la fonction endocrine des testicules.
- Spermatogenèse.
La multiplication des cellules germinales primordiales permet la formation des spermatogonies qui restent au repos jusqu'à la puberté. La spermatogenèse commence à cette étape. La spermatogenèse va de la périphérie vers la lumière des tubes séminifères et se fait de façon synchrone entre les différentes cellules.
La spermatogenèse est composée de trois phases
- phase de multiplication : elle donne les spermatocytes d'ordre 1 par mitoses.
- phase de maturation : les spermatocytes 1 subissent la première division de la méiose et donnent des spermatocytes d'ordre 2. Ces derniers vont subir la seconde division méiotique et donner des spermatides (haploïdes).
- phase de différenciation : elle permet la formation des spermatozoïdes è c'est le début de la spermiogenèse qui mettra en place le flagelle, la pièce intermédiaire et l'acrosome (dans la tête des spermatozoïdes).
B Les voies génitales.
Les voies génitales assurent le transport des spermatozoïdes.
Au départ, on a les canaux spermiques (les tubes droits + le Rete testis). On a ensuite les canaux efférentstête de l'épididyme. Le canal suivant est le canal épididymaire qui se trouve dans le corps de l'épididyme. On trouve enfin le canal déférent dans la queue de l'épididyme.La maturation des spermatozoïdes est réalisée dans le canal épididymaire qui ne permet qu'un transit lent et qui est donc un "lieu de stockage". qui forment la
Remarque : les spermatozoïdes ne sont fécondants que lorsqu'ils sont dans les trompes utérines.Le canal déférent s'élargit et donne l'ampoule déférente qui se déverse dans un canal qui reçoit les conduits des glandes annexes. Après connexion, ce canal rentre en contact avec le canal éjaculateur. Ce dernier va pénétrer dans la prostate puis communiquer avec l'urètre.
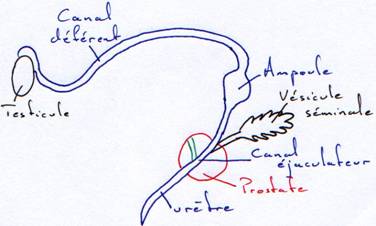
C Les glandes annexes.
1 Les vésicules séminales.
Les vésicules séminales forment un "suc" qui participent à la formation du liquide séminal. Elles sécrètent aussi du fructose et de la prostaglandine.
2 La prostate.
La prostate entoure l'urètre. Ses sécrétions alcalines vont neutraliser l'acidité du liquide séminal. Se sont des sécrétions de faible volume riches en zinc (le zinc a un pouvoir bactéricide).
3 Les glandes de Cooper.
Les glandes de Cooper, ou bulbo-urétrales, se situent de chaque côté de l'urètre et débouchent dans ce conduit à l'entrée du pénis. Elles sécrètent un fluide alcalin afin de neutraliser l'acidité au niveau de l'urètre.
4 Les glandes de Tyson ou prépussiales.
Ces glandes n'ont pas de rôle défini chez l'homme. En revanche, chez les animaux, elles sont des sources de phéromones.
D Le pénis.
Le pénis est formé d'organes érectiles:
- les corps spongieux se trouvent autour de l'urètre.
- les corps caverneux se trouvent de part et d'autre des corps spongieux.
Ces corps sont enfermés dans des enveloppes riches en fibres musculaires et élastiques. Les aréoles sont des cavités qui se remplissent de sang. Quand ce dernier y arrive, il y a un gonflement qui est limité par les enveloppes : c'est la rigidité du pénis.
La vascularisation du pénis est très complexe. Les vaisseaux sont très contractiles.L'érection est un phénomène vasomoteur, sous contrôle du système parasympathique. Elle est due à une vasodilatation des artères érectiles.
La fermeture de la circulation veineuse permet qu'il y ait plus de sang entrant que sortant. La fermeture se fait par contraction des fibres musculaires au niveau des organes érectiles et par contraction des fibres musculaires lisses de la paroi des aréoles. Tous ces phénomènes entraînent une augmentation de la pression.
L'éjaculation : toutes les glandes annexes rejettent leur contenu dans l'urètre. La contraction des muscles par le système orthosympathique entraîne l'expulsion du sperme. On trouve 300 millions de spermatozoïdes par éjaculation normale.
III Fonction endocrine des testicules.
A Production des hormones androgènes.
Ces hormones stéroïdes sont produites à partir de cholestérol. L'hormone principale est la testostérone. On trouve aussi l'androstène-dione et la DHEA (DiHydroEpiAndrostérone).
B Transport et effets des hormones.
Le transport des hormones est assuré par différentes protéines. On retrouve la SBP (Stéroïd Binding Protéine) qui transporte la testostérone. Cette dernière sera éliminée dans les urines sous forme libre ou sous forme conjuguée.Les effets de la testostérone sont visibles au niveau de la différenciation sexuelle, sur la spermatogenèse (caractères sexuels primaires avant la puberté), et par les caractères secondaires (à partir de la puberté).
Les androgènes agissent sur les organes génitaux externes et sur les glandes annexes, sur la croissance st sur le métabolisme (ce sont des anabolisants).
IV Régulation des sécrétions testiculaires.
Le taux de sécrétion testiculaire est faible jusqu'à la puberté. Il commence à augmenter après l'activation de l'hypothalamus qui sécrète de plus en plus de GnRH. Donc, de plus en plus de FSH et de LH sont synthétisés par l'hypophyse.
La LH stimule les cellules de Leydig qui synthétisent la testostérone.
La FSH stimule les cellules de Sertoli qui produisent les protéines liant les androgènes (Androgène Binding Protéine). Elle favorise aussi la spermatogenèse au niveau des tubes séminifères.
Les rétrocontrôles:
- La testostérone exerce un rétrocontrôle négatif sur l'hypothalamus (GnRH) et sur l'hypophyse (LH).
- L'inhibine (synthétisée par les cellules de Sertoli) exerce un rétrocontrôle négatif sur la production de FSH et diminue ainsi la spermatogenèse.
Physiologie de l’appareil génital femelle.
I Anatomie.
A Les ovaires.
Les ovaires sont situés dans la cavité pelvienne. Ils sont recouverts par le pavillon de la trompe utérine et sont maintenus dans leur position par différents ligaments. Les ovaires sont composés de trois couches :
- couche externe : épithélium
- couche dense : tissu conjonctif : albuginée
- zone corticale où se trouvent les différents follicules ovariens (à différents stades de croissance). De la puberté à la ménopause, on assiste à la libération d'ovocytes et de sécrétions hormonales nécessaires à la fécondation et à l'implantation de l'oeuf.
1 Ovogenèse.
Chez l’embryon, il y a colonisation des gonades primitives par les cellules germinales primordiales.
On a ensuite une phase de multiplication : les ovogonies se multiplient et donnent des ovocytes Is’arrête jusqu’à la puberté en cours de prophase 1. (diploïdes).La première division de la méiose
Après la puberté, l’ovocyte I complète sa première division méiotique. On alors deux cellules (un globule polaire et un ovocyte II). La seconde division méiotique débute et s’arrête en métaphase 2.
La division reprendra s’il y a fécondation.A la fin de la méiose, on obtient un deuxième globule polaire et un ovule.
2 Le cycle ovulatoire.
Les cycles se succèdent tous les 28 jours. A chaque fois, un ovocyte est libéré.
L’ovocyte est entouré de cellules : follicules primordiaux. Au stade fœtal, on a 500 000 follicules primordiaux par ovaires. Ils sont tous localisés dans le cortex ovarien.Pendant la période allant de la puberté jusqu’à la ménopause, on a une dégénérescence des follicules : l’atrésie. Finalement, seuls 400 à 500 ovocytes se développent.Pour ceux qui se développent, on a :
- Première phase : La phase folliculaire (qui conduit à l’ovulation).
Un follicule se développe ; les cellules folliculaires s’étendent et donnent la granulosa. Il y a formation d’une thèque interne et d’une externe. Ces deux thèques sont séparées par une membrane basale. La thèque externe est très vascularisée. Les cellules de la granulosa sécrètent un liquide qui donnera l’antrum.
La corona radiata : elle est au contact entre la thèque interne et les cellules de la granulosa grâce au cumulus oophorus. Ce cumulus suit l’ovocyte quand il est libéré.
Le follicule mature ou follicule de Graaf.
L’ovulation a lieu à J+14 par la rupture du follicule, grâce à différentes enzymes. L’ovocyte est expulsé grâce aux hormones hypophysaires.
- Seconde phase : La phase lutéale.
Mise en place d’une glande endocrine temporaire : le corps jaune. Il se met en place avec ce qui reste du follicule. Les cellules de la granulosa donnent les cellules lutéales dont la sécrétion de progestérone est sous la dépendance des hormones hypophysaires (LH).
S’il n’y a pas fécondation, le corps jaune dégénère (en une dizaine de jours) : c’est la lutéolyse. Le corps jaune donnera alors le corps albicans. C’est à ce moment que la menstruation commence.
S’il y a fécondation, le corps jaune persiste et reste actif pendant plusieurs semaines grâce aux hormones produites par le placenta : on parle de corps jaune gestatif.
B Les voies génitales.
1 L’utérus.
L’utérus est un organe musculaire creux dont la partie principale est appelée le corps. Ce dernier reçoit les trompes de Fallope. La partie cylindrique (ou isthme) est en continuité avec le col utérin (ou cervix).

L’utérus est constitué de trois épaisseurs :
- à l’extérieur : la séreuse,
- une couche musculaire épaisse : le myomètre,
- une muqueuse : l’endomètre qui voit épaisseur, vascularisation et rythme de sécrétion modifiés pendant tout le cycle menstruel.
Pendant le cycle, on a trois phases distinctes (trois utérus) :
- jours 1 à 4 : phase menstruelle
- jours 5 à 14 : phase proliférative : reconstitution de l’endomètre grâce aux œstrogènes.
- jours 15 à 28 : phase sécrétoire : les cellules se multiplient, les glandes augmentent en épaisseur et en longueur è l’endomètre est très vascularisé (à partir du 20ème jour).
2 Le vagin.
Le vagin est un conduit musculo-membraneux. Il commence au niveau du cervix et se termine à l’extérieur.
Il est composé de trois couches : une séreuse, une musculeuse et une muqueuse.
Le cycle vaginal est caractérisé par la présence de cellules desquamées dans la première partie du cycle.
II Fonctions endocrines de l’ovaire.
A Les hormones stéroïdes ovariennes.
Les principales hormones sécrétées sont la progestérone et les œstrogènes (œstradiol, œstrone). L’ovaire est capable de fabriquer des hormones androgènes (mâles) en faible quantité.
1 Taux au cours du cycle.
Pendant la phase 1, les œstrogènes augmentent progressivement jusqu’au 14ème jour. Il y a un pic avant l’ovulation. Le taux diminue mais il y a un second pic faible vers le 20ème jour. La progestérone apparaît après l’ovulation. Son taux est maximal juste avant les règles. S’il n’y a pas fécondation, le taux va diminuer. S’il y a fécondation, le taux reste constant.
2 Synthèse.
Le précurseur de toutes les hormones stéroïdes est le cholestérol. Ce cholestérol est métabolisé en prégnènolone qui a deux possibilités de suite:
- la prégnènolone donne directement la progestérone,
- il sert à la formation d’œstrogènes à partir d’hormones mâles.
Ces hormones sont dans le follicule et leur formation débute quand l’antrum se forme. Ce sont les cellules de la thèque interne qui élaborent les précurseurs des œstrogènes à partir de cholestérol, sous l’influence de LH. La transformation des hormones androgènes en œstrogènes est réalisée par une enzyme (aromatase) synthétisée par les cellules de la granulosa, sous l’influence de FSH. La progestérone est synthétisée par la granulosa (quand les cellules de la granulosa ont donné les cellules lutéales) et par les cellules de la thèque interne.
Ces hormones sont sécrétées puis éliminées dans les urines.
3 Transport et action des hormones sexuelles.
Les hormones sont véhiculées par le sang et liées à des transporteurs (protéines). Parmi ces transporteurs, on a :
- La SBP : Stéroïde Binding Protéine. Elle lie essentiellement les œstrogènes mais peut aussi transporter la testostérone et la progestérone.
- La CBG : Corticostéroïde Binding Globuline.
- La transcortine : elle se lie essentiellement à la progestérone.
Ces hormones ont un rôle essentiellement sur le tractus génital.
a Les œstrogènes.
Les œstrogènes ont un effet prolifératif et leur action a lieu au niveau de l’endomètre utérin pour une augmentation de son épaisseur et pour la croissance des glandes utérines.
Au niveau du col de l’utérus leur action entraîne l’apparition de glaires cervicales. Au niveau du vagin, leur action permet une prolifération de l’épithélium. Au niveau des ovaires, les œstrogènes stimulent la croissance folliculaire. Au niveau des glandes mammaires, ils agissent sur les canaux galactophores.
Action métabolique : ils agissent sur la rétention d’eau et de sodium. Ils ont aussi un effet protecteur contre l’artériosclérose.
b La progestérone.
La progestérone intervient dans la différenciation cellulaire. Au niveau de l’endomètre utérin, elle est responsable de la dentelle endométriale. Elle rend la muqueuse utérine apte à la nidation et au maintien de la gestation. Au niveau du col utérin, elle est responsable du durcissement de la glaire cervicale qui empêche alors l’entrée des spermatozoïdes. Au niveau des glandes mammaires, elle augmente la croissance des ascini.
L’action thermogénique de la progestérone entraîne une augmentation de 0,5°C après l’ovulation.
B Les cybernines ovariennes.
Les cybernines sont des polypeptides sécrétés par l’ovaire et qui modulent l’activité de ces ovaires. Leur intervention est locale et de longue durée (pendant toutes les étapes de formation du follicule) :
- La OMI (Inhibiteur de la Maturation de l’Ovocyte) : elle serait sécrétée par les cellules de la granulosa. La libération de l’ovocyte permet la reprise de la méiose car il n’est plus sous l’influence de l’OMI.
- La FSH-BI : elle inhibe la fixation de la FSH. S’il n’y a pas de fixation de FSH, le follicule dégénère.
- La LI : c’est un inhibiteur de la lutéinisation
- L’inhibine : elle permet la régulation de l’axe hypothalamo-hypophysaire. L’inhibine est produite par les cellules de la granulosa (cellules lutéales) et va agir sur l’hypophyse pour inhiber la sécrétion de FSH. Elle agit aussi sur l’ovaire pour assurer une diminution de la production de progestérone.
C Contrôle hypothalamo-hypophysaire.
L’activité ovarienne est dépendante de l’activité hypophysaire (pour FSH et LH).
Le taux de FSH : il augmente pendant la phase folliculaire puis donne un pic synchrone avec la LH pendant l’ovulation.
Le taux de LH : le pic principal précède de 40 heures l’ovulation et permet la sécrétion de progestérone.
La FSH agit sur la croissance des follicules et sur la production d’œstradiol. Les hormones ovariennes exercent des rétrocontrôles négatifs sur la production de LH ou de FSH : la progestérone a un rétrocontrôle négatif sur la LH. Les œstrogènes ont deux types de rétrocontrôle : rétrocontrôle négatif sur la production de FSH ; au cours de la maturation, quand l’œstradiol dépasse la concentration de 200 pg/mL, le rétrocontrôle est inversé, donc positif sur FSH et essentiellement sur LH.
Le GnRH : elle est synthétisée au niveau du noyau arqué de l’hypothalamus. Sa sécrétion est pulsatile (2 ou 3 coups par heure) et elle est répercutée sur les hormones hypophysaires.La pulsabilité est constante pendant la phase folliculaire et diminue pendante la phase suivante
III Gestation.
A Fécondation.
Après expulsion du follicule, l’ovocyte II pénètre dans la trompe de Fallope, vers l’utérus. Lors de l’accouplement, il y a libération d’ocytocine qui favorise la progression de l’ovocyte en augmentant les contractions tubaires et utérines. Les contractions favorisent la progression des zoïdes. Seulement 1% de ces zoïdes franchit les glaires cervicales (mucus sécrété par le cervix). Ces glaires permettent de « décaper » les zoïdes et de leur faire acquérir leur pouvoir fécondant. Un zoïde va pénétrer dans l’ovule par lyse de la membrane pellucide, grâce à des sécrétions enzymatiques. Cette piqûre spermatique entraîne la réactivation de l’ovocyte qui sécrètera des enzymes empêchant la polyspermie. Il y a ensuite achèvement de la méiose.
B Implantation.
C’est à l’état de blastocyste que l’œuf parvient au contact, dans la cavité utérine. La période de vie libre est de sept jours. Cet œuf se fixera ensuite dans la paroi utérine.L’utérus est très réceptif.
Le corps jaune est au maximum de son développement. La muqueuse utérine est très développée et vascularisée. Le myomètre est inhibé par la progestérone. Grâce à des enzymes protéolytiques, le blastocyste érode la muqueuse utérine : c’est l’implantation interstitielle.
C Formation du placenta.
La paroi extra embryonnaire (trophoblaste) prend naissance au contact de la muqueuse utérine, du placenta.Les cellules prolifèrent : on a alors un syncitiotrophoblaste. Ce dernier s’enfonce dans la muqueuse et forme des villosités choriales qui parviennent au niveau des capillaires maternels. Ce syncitiotrophoblaste détruit la paroi. Il se forme alors de grandes lacunes de sang où ont lieu les échanges entre le fœtus et la mère. C’est un placenta hémochorial.
D La fonction du placenta.
Le placenta a deux grands rôles : nourricier et endocrine.
1 Fonction nourricière.
Deux types de circulation s’établissent dans le placenta : une circulation fœto-placentaire et utéro-placentaire. Ces deux circulations sont séparées par la barrière placentaire.
a Circulation fœto-placentaire.
Cette circulation passe par le cordon ombilical. Elle comprend deux artères et une veine. L’ensemble est relié par des capillaires. Le sang du fœtus passe par le placenta (renouvellement). Ce placenta constitue la seule interface entre la mère et le fœtus.
b Circulation utéro-placentaire.
Le sang arrive par la branche artérielle utérine. Il va se répandre dans les lacunes qui sont entre les villosités. Il est ensuite repris par la veine utérine. La surface choriale est divisée en lobules présentant eux-même des villosités plongeant dans les lacunes. C’est la surface choriale qui formera la barrière placentaire. Celle-ci s’amincie pendant les quatre premiers mois, pour atteindre et garder une épaisseur de quatre microns.
Cette barrière est imperméable mais sélective : échanges surtout d’O2 vers l’embryon (l’hémoglobine fœtale est plus affine pour l’oxygène que l’hémoglobine maternelle), de nutriments, de déchets, de médicaments, d’anticorps et d’hormones.
2 Fonction endocrine.
La placenta se comporte comme une usine hormonale qui relie l’hypophyse aux ovaires. Le placenta sécrète une hormone, l’HCG (hormone gonadotrophine chorionique), qui remplace la LH. Cette HCG maintiendra le corps jaune ovarien dès la cinquième semaine. C’est le placenta qui sécrète la progestérone jusqu’à la fin. Il sécrète aussi les oestrogènes.è Le placenta est une usine à hormones.
IV La parturition (accouchement).
Pendant la gestation, l’embryon a un mode de vie aquatique.L’élément le plus important : un « vieux » placenta entraîne l’arrêt fonctionnel du corps jaune de gestation : il y a alors diminution de sécrétion de progestérone (n’y a plus d’inhibition du myomètre) : l’activité utérine reprend. Les contractions engagent le fœtus dans le col utérin qui va se dilater. Un réflexe se met en place et entraîne la sécrétion, par la post-hypophyse, de l’ocytocine qui intensifiera les contractions utérines. L’utérus sécrète en même temps de la prostaglandine qui augmente l’histolyse du placenta et du corps jaune résiduel.
En même, il y a production de relaxine qui dilatera les ligaments de la ceinture pelvienne et ramollira les muscles utérins. L’accouchement a lieu en deux temps. Cinq minutes entre les contractions : c’est le moment.
La poche des eaux se rompt et le col de l’utérus s’efface ; le fœtus s’engage, aidé par les contractions volontaires de la mère. L’expulsion est rapide, on coupe le cordon ombilical.
V Lactation.
A Les glandes mammaires.
Les glandes mammaires sont formées par les ascini et des tissus adipeux. Les ascini sont des glandes qui aboutissent dans les canaux galactophores. Ces derniers sont entourés de capillaires sanguins et par des cellules musculaires qui permettent l’extrusion du lait.
B Composition du lait.
Les trois premiers jours, c’est le colostrum qui est riche en anticorps. Le lait est riche en protides (15g), en lipides (34g), et en glucides (67g). On y trouve aussi des sels minéraux (2 g/L), des anticorps et des vitamines.
C Mécanismes de sécrétion.
Pendant la gestation, le corps jaune et la placenta produisent de la progestérone. Cette hormone va agir au niveau des seins en inhibant la sécrétion de lait. Le placenta produit l’HCG et l’HCP qui vont entraîner une multiplication des ascini et donc, augmenter la production de lait. Ce lait ne sortira pas car il y a inhibition par la progestérone. Au moment de la parturition, la quantité de progestérone diminue brusquement et l’inhibition de sécrétion est levée.
L’hypophyse produit la prolactine (PRL) qui stimule la synthèse de lait. La succion entraîne un réflexe qui agit sur l’hypophyse postérieure : il y a sécrétion d’ocytocine qui agira sur les cellules musculaires des seins : il y a alors extrusion.
D Maintient de la lactation.
La lactation peut durer des années (si l’enfant continue à téter, il y a production de lait) : c’est un réflexe tacto-hypothalamohypophysaire qui entraîne l’inhibition des neurones à GnRH et le maintient en aménorrhée (pas de règle). Ce réflexe entretient une hyperprolactidémie qui maintient l’aménorrhée par inhibition de LH.
TD : Le problème hypothalamo-hypophysaire et L'absorption digestive.
Le problème Hypothalamo-Hypophysaire.
L’hypothalamus contrôle le système endocrinien par l’hypophyse (glande pituitaire). Ces deux structures constituent l’axe hypothalamo-hypophysaire.
I Organisation anatomique de l’axe hypothalamo-hypophysaire.
A L’hypophyse.
C’est une petite glande de 0,6 gramme chez l’Homme. Elle est suspendue à l’hypothalamus par la tige pituitaire. Elle se situe dans une petite cavité osseuse (selle tercique) de l’os sphénoïde (à la base du crâne).
Cette hypophyse comporte deux parties d’origine embryologique différente :
- L’adénohypophyse ( ou antéhypophyse) : elle est en position antérieure de l’hypophyse. Son origine embryologique est ectodermique ; elle provient d’un ectoderme non différencié.
- La neurohypophyse (ou posthypophyse) : elle est d’origine neurodermique.
1 L’adénohypophyse.
Elle est constituée de différents types cellulaires sécréteurs. Chaque type sécrète des hormones différentes : c’est une glande pluri-endocrinienne). L’activité sécrétrice est contrôlée par les neurones hypothalamiques.
2 La neurohypophyse.
Elle ne contient aucune cellule glandulaire. Elle contient des faisceaux d’axones dont les terminaisons libèrent des neurosécrétions.
B L’hypothalamus.
Il est constitué par de nombreux noyaux.
Au niveau de l’hypothalamus antérieur, on trouve les noyaux : para-ventriculaire, supra-optique, pré-optique et supra-chiasmatique.
Au niveau de l’hypothalamus médian, on trouve le noyau arqué et le noyau tubéro-latéral.
Le contrôle est direct au niveau de la neurohypophyse où les neurones qui sont issus de l’hypothalamus libèrent des neurosécrétions dans la circulation générale (grâce à la vascularisation) : on parle alors de neuro-hormones.
Le contrôle indirect a lieu au niveau de l’adénohypophyse où d’autres neurones hypothalamiques libèrent des sécrétions régulatrices mais dans le système porte adénohypophysaire.
à RH : releasing hormone (=libérine)
à IN : inhibiting hormone (=inhibine).
Ces neurosécrétions libérées dans ce système contrôlent la synthèse et la libération de véritables hormones sécrétées par les cellules glandulaires de l’adénohypophyse.
 C’est un système neuroendocrinien.
C’est un système neuroendocrinien.
C Notions importantes en neuroendocrinologie.
Neurosécrétions : certaines cellules fonctionnent soit comme un neurone, soit comme des cellules endocriniennes (ex : neurones hypothalamiques). L’information électrique est transformée en information hormonale.
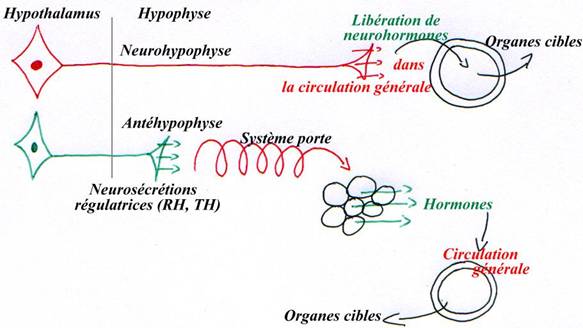
Système porte : un système porte est une liaison vasculaire particulière, constituée de vaisseaux situés entre deux systèmes capillaires. Dans l’adénohypophyse, il permet aux neurosécrétions d’atteindre rapidement les cellules glandulaires sans être dilués.
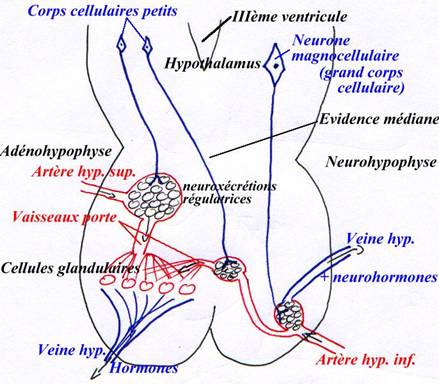
II La neurohypophyse.
A Les neurohormones neurohypophysaires.
Il existe deux types de neurohormones neurohypophysaires :
- ADH : Hormone AntiDiurétique.
- L’OT : Ocytocine.
Ces deux hormones sont très proches chimiquement ; elles contiennent neuf acides aminés et diffèrent par deux d’entre eux.
Les précurseurs de ces hormones sont synthétisés dans des gros neurones, au niveau des noyaux para-ventriculaire et supra-optique.
Le précurseur de l’ADH est la propressophysine.
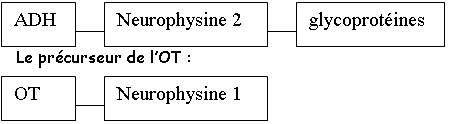
Le clivage s’effectue dans les axones et les hormones sont libérées dans les terminaisons axoniques.
1 Rôle de l’ADH.
L’ADH a deux organes cibles :
- Le rein : elle la réabsorption en eau en augmentant la perméabilité à l’eau au niveau des tubes collecteurs.
- Les vaisseaux : elle entraîne une vasoconstriction (resserrement des vaisseaux).
2 Rôle de l’OT.
Elle a deux organes cibles :
- Les glandes mammaires où elle permet l’éjection du lait en autorisant la contraction des cellules myo-épithéliales de ces glandes.
- L’utérus : pendant l’accouchement, elle agit sur la contraction du muscle lisse de l’utérus (myomètre) pour expulser le bébé.
B Contrôle des sécrétions.
1 L’ADH..
Le contrôle de l’ADH se fait directement sur l’hypothalamus grâce aux osmorécepteurs (sensibles à la pression osmotique) où une baisse de la pression osmotique entraîne une diminution de la sécrétion d’ADH pour compenser une diminution de cette pression osmotique. Le contrôle est aussi assuré par l’intermédiaire du système cardiovasculaire, où, des volorécepteurs (récepteurs à la volémie) enregistrent les changements de pression. Ils se situent au niveau des oreillettes et des gros troncs veineux.
Une hausse de la volémie entraîne un diminution d’ADH. Une diminution de volémie entraîne, elle, une augmentation de sécrétion d’ADH.
D’autres facteurs comme, la chaleur, les émotions, la nicotine, peuvent accroître le sécrétion d’ADH. Le froid et l’alcool entraînent, eux, une réduction de la libération d’ADH.
2 L’ocytocine.
La régulation de l’ocytocine est prise en charge par deux réflexes :
- R éflexe d’éjection du lait : pendant la tétée, des mécanorécepteurs sont stimulés par afférence sensorielle (système nerveux central) à hypothalamus à ocytocine à circulation générale à glandes mammaires à éjection du lait.
- Réflexe de contraction de l’utérus : la dilatation du col utérin (stimulus) est enregistrée par des mécanorécepteurs à système nerveux central à hypothalamus à ocytocine à circulation générale à myomètre à augmentation des contractions utérines à expulsion du bébé.
III L’adénohypophyse.
Les hormones sont libérées par les cellules glandulaires de l’hypophyse. Ces hormones sont de type peptidique.
Ces neurohormones sont sécrétées au niveau des neurones parvo-cellulaires, dans les noyaux arqué, pré-optique, tubérolatéral, supracchiasmatique et para-ventriculaire (sert aux deux hypophyses).
Les neuropeptides régulent la sécrétion d’hormones.
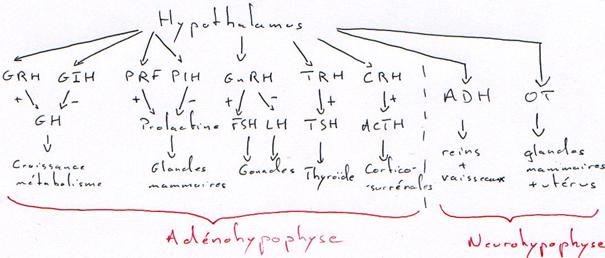
A L’hormone de croissance.
L’hormone de croissance (GH ou somatotrope STH) est une protéine. Elle agit sur la croissance, avant la soudure des cartilages de conjugaison. Elle accroît le nombre de mitoses osseuses et cartilagineuses. Un déficit en cette hormone provoque le nanisme. Un excès entraîne une acromégalie.
Cette hormone a une action sur le métabolisme glucidique : elle est hyperglycémiante. Elle a aussi une action lipolytique, et un effet anabolisant avec les protéines.
Les contrôles :
- inhibiteur : GIH (somatostatine et SRIF)
- activateur : GRH (somatocrinine ou somatolibérine)
Les glucocorticoïdes, les hormones thyroïdiennes, les hypoglycémie et une augmentation du taux d’acides aminés vont avoir un effet régulateur sur cette hormone.

Les traumatismes (douleurs, froid, sommeil, exercice et jeune) vont avoir un effet de contrôle.
B La prolactine (P ou PRL).
C’est une protéine qui a pour organe cible les glandes mammaires. Elle agit sur les cellules sécrétrices du lait en permettant leur multiplication.
Elle favorise la synthèse des substances nutritives du lait :
- Activateurs (stimulants) : PRF, TRH, OT et deux réflexes (tétée et stimulation du col utérin).
- Inhibiteurs : PIH et dopamine.
C Les hormones gonadotrophes.
FSH, LH. Comme stimulant, on trouve le GnRH.
D La TSH (glycoprotéine).
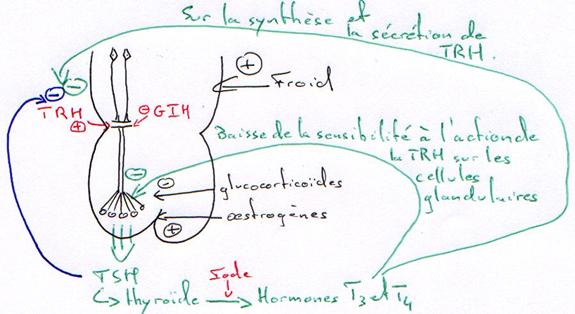
Les hormones T 3 et 4 agissent sur les organes et tissus (sur le métabolisme cellulaire). Ces hormones augmentent la glycogénolyse (hépatique et musculaire), la lipolyse. Elles ont un effet anabolisant vis-à-vis des protéines. Elles permettent aussi une augmentation de la thermogenèse.
E L’ACTH (fonction corticotrope).
L’ACTH provoque la libération d’une substance hormonale (le cortisol) par les corticosurrénales, pendant le stress.
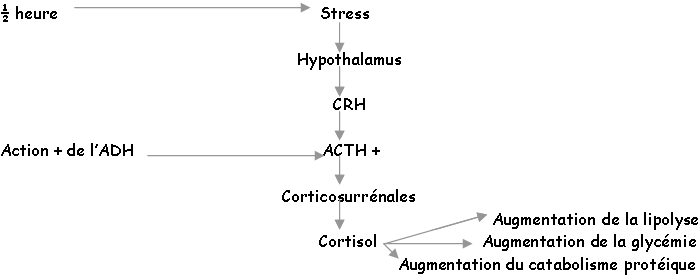
Pendant le stress, le système orthosympathique mis en place de suite, innerve la glande médullosurrénale qui va synthétiser de la noradrénaline et de l’adrénaline.
Le système limbique (qui régit les émotions) de certaines fonctions endocrines est bloqué par les émotions.
Absorption digestive.
I Introduction.
A Généralités.
· L’absorption a lieu tout au long du tube digestif.
· Au niveau de la bouche, on a l’absorption perlinguale.
· L’alcool passe dès l’estomac.
· Au niveau de l’anus, il y a aussi absorption (suppositoires).
 L’absorption est faible : autour de 100 mg.
L’absorption est faible : autour de 100 mg.
Au niveau intestinal, la quantité d’absorption digestive est de 1 kg. La digestion n’a de sens que si les nutriments peuvent être mis à la disposition des cellules de l’organisme grâce à un système d’absorption : la cellule intestinale. Le système de transport est composé par le sang et la lymphe.
B Dispositif absorbant.
L’intestin grêle a une longueur de 3 mètres et un diamètre de 4 cm. Ces dimensions donnent une surface de 0,35 m² (surface faible). Les valvules conniventes permettent de tripler la surface (1 m²). Les villosités permettent de passer à 10 m² (x10) et les microvillosités font passer cette surface à 200 m² (x20).  Finalement, la surface d’échange est multipliée par 600.
Finalement, la surface d’échange est multipliée par 600.
Le sang chargé de nutriments remonte vers le foie (pour les glucides et protides) par les capillaires puis les veinules et enfin par les veines : c’est un système porte (1L/min). Après un repas, le débit passe à deux litres par minute.
Les chylifères permettent le transport des lipides. Ils se jettent dans le canal thoracique, dans la sous-clavière puis dans la veine cave (sang). Le débit est de 2 à 3 mL par minute.
II Les glucides.
A Introduction.
Les glucides représentent entre 55 et 60% de notre apport énergétique quotidien.
- Amidon : 50% des apports.
- Saccharose : 30%.
- Lactose et fructose : 20%.
Les polysaccharides complexes seront digérés par la cellulose.
B Digestion.
1 Digestion intraluminale.
Cette partie de la digestion a lieu dans la lumière du tube digestif et permet l’hydrolyse des polyosides (amidons).
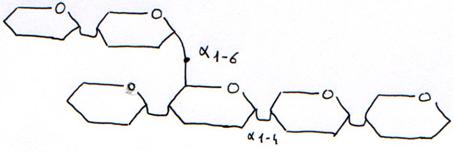
L’amylase est d’origine pancréatique et salivaire. Cette enzyme coupe les liaisons  1
1 4.
4.
La digestion par l’amylase donne :
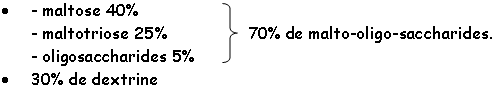
2 Digestion des oligo et disaccharides.
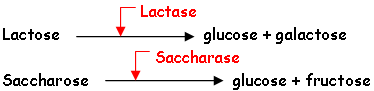
Ces enzymes sont sur les bordures des cellules épithéliales.
L’ -glucosidase donne la glucoamylase et l’
-glucosidase donne la glucoamylase et l’ -dextrinase sucrase.
-dextrinase sucrase.
3 Absorption.
On a deux systèmes de transport : transport transcellulaire (glucose galactose) et diffusion paracellulaire.
L’absorption du glucose et du galactose est réalisée par l’intermédiaire d’une combinaison ternaire ; monosaccharide, transporteur Na+, avec nécessité de fournir de l’énergie.
L’affinité du transporteur pour le sucre augmente avec la concentration en Na+. Quand cette concentration est grande (ce qui est le cas dans la lumière du tube digestif), le transporteur fixe intensément le sucre. Le complexe ternaire passe sur la phase cytosolique. Le milieu étant faible Na+, il y a libération de sodium. Le milieu en est ensuite appauvri grâce à une ATPase NaK qui consomme de l’énergie.
Le glucose intracellulaire sort de la cellule par diffusion facilitée grâce à un second transporteur (Glut 2).
Le cas du fructose.
Le transport facilité est indépendant de la concentration en sodium. Le transporteur sur la face apicale est le Glut 5, celui de la face basale est le Glut 2.
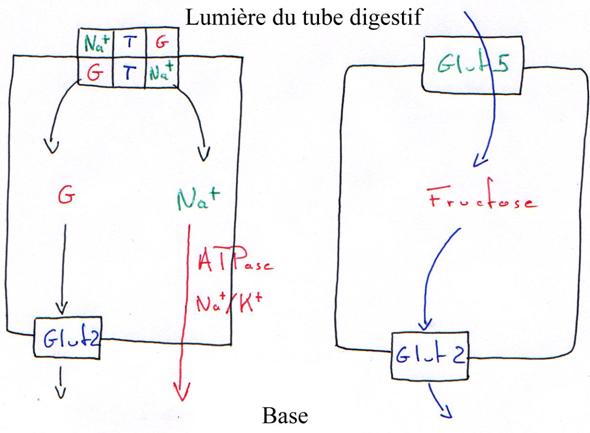
La diffusion paracellulaire prend en charge 20% des sucres. C’est une diffusion passive sans apport d’énergie. Le passage se fait selon le gradient de concentration.
D Le devenir des sucres.

Les sucres qui n’auront pas été absorbés serviront de source d’énergie aux bactéries qui produisent des acides gras volatils et des gaz (H2, CO2, CH4).
III Les protides.
A Introduction.
On trouve deux types de protides : les protides d’origine exogène et les protides d’origine endogène.
1 Les protéines exogènes.
Elles représentent 10 à 15% de notre apport énergétique quotidien. On ingère 1g de protide par kg (de masse corporelle) et par jour.
Les protéines végétales sont moins bien digestibles que les protéines animales, du fait qu’elles sont engagées dans des polymères ligneux qui les protègent.
La cuisson des aliments entraîne une modification de leur structure.
2 Les protéines endogènes.
Ce sont les glycoprotéines enzymatiques (salivaire, gastrique, …). On en absorbe 20 à 30g par jour. Les protéines de la bile représentent 10 g par jour et les cellules desquamées apportent 30g par jour de protides.
Avec un apport de 60g de protéines exogènes et 60g de protéines endogènes, un sujet de 60kg excrète entre 6 et 12g de protides. On a alors une absorption comprise entre 90 et 95%.
B Digestion.
1 Digestion intraluminale.
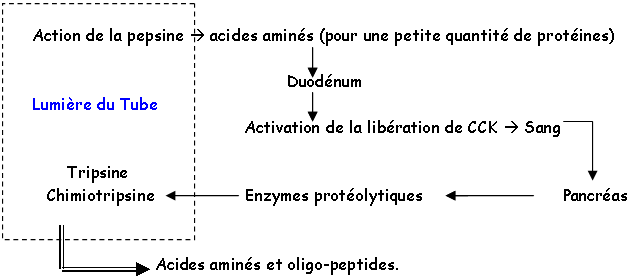
2 Digestion entérocytaire (au niveau des cellules intestinales).
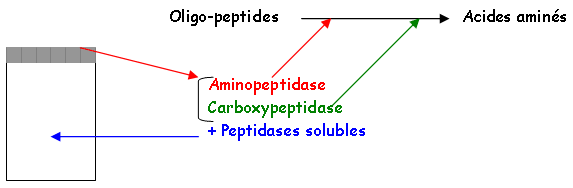
C Absorption.
1 Absorption des acides aminés.
Le transport des acides aminés se fait grâce à des transporteurs. Certains seront Na-dépendants, d’autres seront indépendants.
2 Les oligo-peptides.
Les dipeptides et les tripeptides sont transportés à travers la membrane par mécanisme Na+ indépendant mais H+ dépendant, ce qui coûte de l’énergie (avec la pompe Na/K).
D Le devenir des acides aminés.
Ils passent au niveau du sang et vont au foie pour servir à la synthèse protéique ou pour être dirigé vers d’autres organes comme les muscles.
IV Les lipides.
A Introduction.
Il existe des lipides exogènes (30% de l’apport énergétique quotidien). 80 à 90% sont des triglycérides, 10 à 20% sont des phospholipides ou du cholestérol. On trouve aussi des vitamines liposolubles. Parmi les acides gras essentiels, on trouve l’acide linolénique et l’acide arachidonique.
Parmi les lipides endogènes, on trouve les lipides biliaires, les lipides provenant des cellules desquamées et des bactéries détruites.
Il n’y a pas de limite à l’absorption des glucides et des protides. Les lipides, eux, en ont une. Quand la dose de lipides est supérieure à 300g/j, ils provoquent des stéatorrhées (diarrhées).
B Digestion.
1 Généralités.
L’agitation mécanique et les sels biliaires réduisent la taille des grosses gouttelettes lipidiques. Cette première action permet une meilleure attaque de la lipase pancréatique. Les résidus de l’action de cette dernière enzyme sont des acides gras, des monoglycérides, des diglycérides et du glycérol.
>Ensuite, les sels biliaires, les acides gras, les monoglycérides et les diglycérides forment des particules hydrosolubles : les micelles qui permettent de passer dans la phase aqueuse.
Les sels biliaires sont formés d’une molécule de cholestérol (non polaire), de plusieurs radicaux hydroxyles et d’une chaîne carbonée avec un radical carboxyle terminal. Le côté non-polaire du cycle stéroïde se dissout à la surface de la gouttelette lipidique non plaire et laisse la face polaire exposée à la surface. Comme les radicaux ionisés sont en surface, les petites gouttelettes ne peuvent pas se reformer en grosses gouttelettes.
2 Digestion gastrique.
L’action de la lipase linguale permet la digestion lipidique en milieu acide, en l’absence de sels biliaires : elle permet l’hydrolyse de 10 à 30% des lipides au niveau stomacal.
3 Digestion intestinale.
T6  lipase.
lipase.
PL  phospholipase A2.
phospholipase A2.
Cholestérol  cholestérol estérase.
cholestérol estérase.
Même schéma que pour les protéines.
Dans le duodénum et le jéjunum, les sels biliaires sont ionisés car le pH est supérieur au pKa : l’absorption est impossible.
Dans l’iléon, le milieu est de moins en moins alcalin (le pH diminue) : les sels biliaires ne sont plus ionisés et pourront être absorbés.  C’est le cycle entéro-hépatique des sels biliaires (95% d’entre eux sont réabsorbés).
C’est le cycle entéro-hépatique des sels biliaires (95% d’entre eux sont réabsorbés).
Master:
Chapitre 1 :
La Circulation.
I Introduction et Rappels.
A Le rôle de la circulation sanguine.
La circulation permet entre autre le transport de l’oxygène qui est devenu nécessaire suite à l’accroissement de taille des organismes. La diffusion ne se fait que pour des surfaces de quelques microns d’épaisseur.
Le sang transporte :
- Les nutriments (produits de la digestion).
- L’oxygène.
- Les déchets (du métabolisme, comme le CO2).
- Les hormones (molécules servant de signaux).
- Des cellules (les globules rouges et cellules du système immunitaire).
- Les anticorps.
- La chaleur pour les animaux endothermes (transport de calories).
B Les compartiments liquidiens d’un organisme.
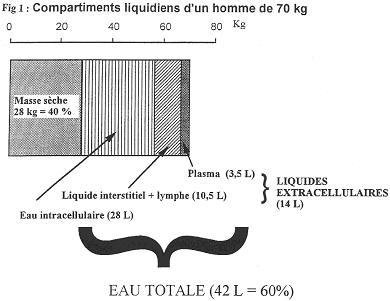
1 Définition des compartiments liquidiens.
On distingue l’eau dans le compartiment intracellulaire et l’eau du compartiment extracellulaire (la moitié).
Le liquide interstitiel, qui baigne les cellules, est composé de 10,5 litres. Il joue un rôle dans l’homéostasie.
Le plasma sanguin ne comprend que 3,5 litres.
La circulation sanguine ne représente qu’une faible proportion des liquides corporels. Pour être efficace, elle a une vitesse importante. Le débit cardiaque est de 5 litres par minute.
2 Méthode de détermination.
Pour effectuer le calcul d’un volume, on dilue une substance dans le nouveau volume. Il faut tout de même trouver une substance qui reste dans le compartiment étudié.
· Pour l’eau totale, on utilise de l’eau. Cette eau est marquée au tritium (3H2O). Cette eau va se diluer et on regardera le facteur de dilution.
· Pour le plasma, on utilise l’albumine. Cette dernière ne quitte pas la circulation sanguine (en réalité, elle ne quitte que très peu ce compartiment). L’albumine utilisée sera marquée radioactivement par de l’iode (radioactif). On peut aussi utiliser le bleu Hevans (ou T18-24) à la place de l’albumine.
Au début de l’expérience, on observe l’effet de dilution, puis une phase de plateau (ceci est valable pour toutes les molécules).
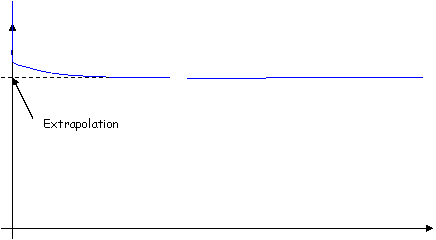
· Pour l’eau extracellulaire, on utilise du Bromure (Brome).
· Pour le volume interstitiel on fait la différence entre « l’espace brome » (eau extracellulaire) et le volume plasmatique (« espace albumine »).
· Pour l’eau cellulaire, on fait la différence entre l’eau totale et l’eau extracellulaire (espace brome).
Il y a toujours des mouvements d’eau d’une espace à un autre.
La circulation est en relation avec l’eau extracellulaire. Chez les mammifères, l’appareil circulatoire est clos mais pas étanche. Les échanges se font du plasma vers le milieu extracellulaire (grâce à la pression osmotique) : c’est la filtration capillaire.
La pression sanguine fait passer le liquide vers le milieu extracellulaire (sens hydrostatique). La pression oncotique fait entrer le liquide (vers le sang).
|
|
Plasma
|
Liquide extracellulaire et interstitiel
|
Liquide intracellulaire
|
|
Cations
|
Na+
|
Na+
|
K+
|
|
Lipides
|
Peu de différence
|
|
Protéines
|
+++
|
+
|
++++++
|
|
Phosphates
|
|
Très peu
|
++++
|
La barrière épithéliale bloque les grosses molécules mais laisse passer les petites.
C Les méthodes d’étude de l’appareil cardiovasculaire.
1 Les variables mesurables.
On peut mesurer :
- Des pressions : la pression artérielle (en mm de Hg). Une pression n’est pas une force.
- Des débits : par exemple, le débit cardiaque (5 litres par minute chez l’Homme).
- Des volumes : par exemple, le volume du ventricule (120mL en moyenne chez l’Homme).
2 Mesures de Pressions.
a Les méthodes indirectes.
- La méthode auscultatoire : pour cette méthode, on a besoin d’un brassard et d’un stéthoscope. On va mesurer la pression artérielle diastolique et systolique (pressions moyennes)
- Par Finapres : dans ce cas, on va mesurer la pression artérielle en continue. On place un « brassard » sur le doigt. L’intérêt de cette méthode est qu’elle donne la pression à chaque battement cardiaque (on voit alors les différences de pression).
b Les mesures directes (méthodes sanglantes).
Pour les méthodes sanglantes, on a deux voies d’entrée :
- La voie veineuse par cathétérisme droit (jambe ou bras). Dans ce cas, on peut atteindre jusqu’à l’oreillette. Grâce au cathétérisme on peut mesurer la pression, récupérer du sang, faire des injections… On peut même pousser jusque dans le ventricule droit et même jusqu’au tronc pulmonaire.
- La voie artérielle par cathétérisme gauche. Ce cathétérisme est plus difficile. Les artères étant profondes et la pression forte. Dans ce cas, on peut aller à l’entrée de l’aorte puis dans le ventricule (pas dans l’oreillette).
3 Mesure des débits.
a Chez l’animal, à « usage unique ».
On peut utiliser un débitmètre électromagnétique mais c’est un cas relativement rare.
On peut aussi utiliser des microsphères (méthode très utilisée mais définitive pour l’animal). Ces billes (ou microsphères) sont radioactives ou colorées. Elles ont un diamètre compris entre 10 et 15 micromètres et vont bloquer les capillaires.
Grâce à cette méthode, on n’a besoin que d’une petite partie du tissu étudié.
Avec les billes colorées, à t0, on utilise une première couleur, à t1, une seconde couleur, etc. … Finalement, on digère le tissu puis on passe ce qu’il reste au colorimètre.
Avec la méthode des billes radioactives, on n’a pas besoin de digérer le tissu.
b Chez l’Homme.
Doppler et Ecographie.
Chez l’Homme on mesure plus facilement la vitesse de la circulation sanguine que le débit.
La vitesse de circulation est obtenue grâce à l’effet Doppler.
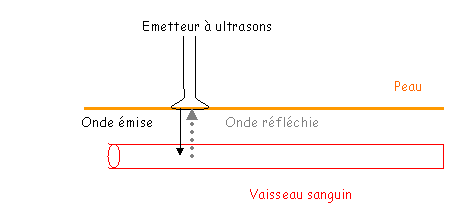
La variation de fréquence est proportionnelle à la vitesse de déplacement du sang dans les vaisseaux.
L’expérience donne une courbe à intégrer et peut donner la vitesse moyenne.
Après une écographie, on obtient la section des vaisseaux, puis le diamètre. On en déduit donc le débit grâce à l’écographie et au Doppler.
Méthode de Fick.
La méthode de Fick est un calcul permettant d’accéder au débit sanguin.
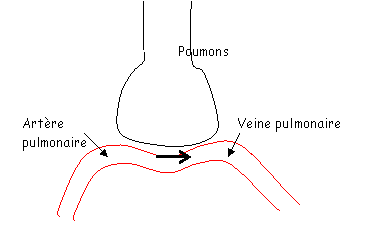
Pour faire ces calculs, il faut connaître la consommation d’O2 : VO2 = 250mL/min.
[O2] dans l’artère pulmonaire : 150mL d’O2/L (de sang)
[O2] dans la veine pulmonaire : 200mL d’O2/L (de sang).
Il y a 50mL de différence entre l’artère et la veine pour un litre de sang. Hors, 250mL d’O2 passent dans le sang chaque minute. On peut en déduire que 5 litres de sang passent dans les poumons par minute (c’est le débit).
La Pléthysmographie.
Le principe de cette technique est que l’on va mesurer la variation de volume d’un membre afin de déterminer le débit sanguin. Pour observer une variation de volume d’un membre (main…) on va bloquer le retour veineux, par exemple, par un garrot pour la main.
4 Mesures de volume.
La plupart du temps, les mesures de volume se font grâce à des techniques d’imagerie médicale (radiographie avec rayons X, écographie avec ultrasons, RMN [Résonance Magnétique Nucléaire] qui donne la meilleur définition, mais toujours en coupe).
5 Cas particulier de la fonction cardiaque.
a La fréquence cardiaque.
Pour la fréquence cardiaque, il faut distinguer la fréquence moyenne et la fréquence instantanée. La prise du pouls artériel se fait par l’arrivée de l’onde de pression et donne une fréquence moyenne. La mesure de la fréquence cardiaque par cardio-fréquence-mètre donne un enregistrement de l’activité électrique du cœur, ce qui permet d’obtenir une fréquence moyenne ou instantanée.
b Le volume d’éjection systolique (VES).
Le VES est le volume de sang quittant le cœur à chaque systole. La méthode par le calcul donne : Dc = Fc × VES ó 5L/min. ≈ 70 × 70mL
VES moyen = Dc/Fc
Une méthode instantanée est la radiologie qui permet la mesure de surfaces mais c’est une méthode peu fiable.
D Structure des appareils cardiovasculaires et relations avec l’appareil respiratoire.
1 Les poissons à respiration strictement branchiale.
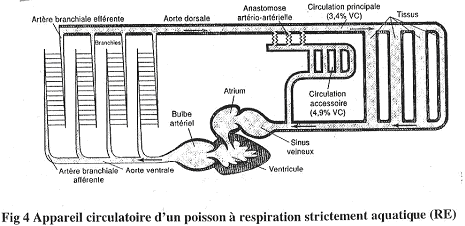
Le sang va du cœur aux branchies, puis aux organes et enfin, retourne au cœur.
Le cœur n’a que du sang désoxygéné.
Il ne faut pas oublier la présence d’une circulation accessoire. A partir de l’aorte dorsale se dérivent des anastomoses artério-artérielles qui détournent une partie du sang vers ce réseau secondaire.
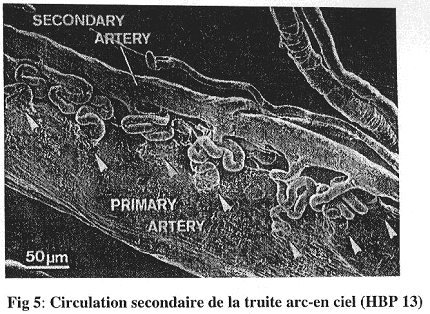
Cette circulation accessoire ne contient du plasma et a un rôle toujours inconnu.
2 Les poissons type Dipneuste.
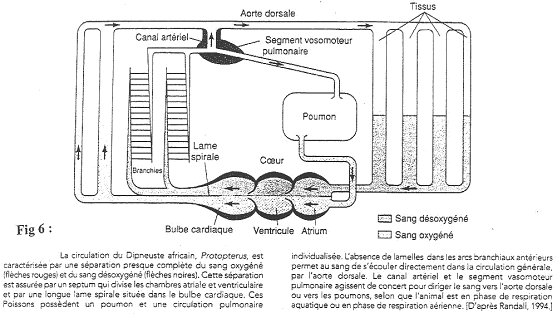
Certains poissons présentent l’apparition d’un poumon.
Ils respirent à la surface (quand l’eau comporte très peu d’oxygène). Au niveau du cœur, il va y avoir séparation des deux types de circulation.
Le sang des organes ne se mélange pas au sang arrivant des poumons. La séparation du sang désoxygéné et du sang oxygéné se fait grâce à l’action de la lame spirale qui est un début de cloisonnement.
Les deux premiers arcs branchiaux perdent les branchies. Des sphincters vont orienter le sang vers l’aorte (quand le poisson est dans l’eau) ou vers les poumons (quand le poisson est dans l’air).
3 Les amphibiens.
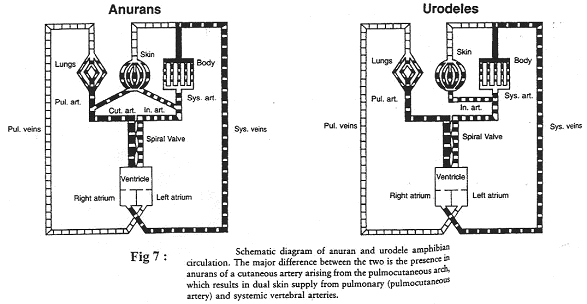
Les amphibiens peuvent avoir une respiration pulmonaire et/ou cutanée.
On observe une séparation anatomique avec les deux oreillettes et un ventricule. La lame spirale est le dispositif permettant de réduire le mélange des sangs.
a Les anoures.
Le sang venant des poumons s’enrichie en O2, arrive dans l’oreillette gauche et ne doit pas se mélanger au sang veineux arrivant dans le ventricule. Ce sang va partir vers les organes ou vers la peau. Dans ce dernier cas, il sera plus oxygéné.
Le sang veineux part préférentiellement vers le tronc pulmo-cutané.
b Les urodèles.
On ne trouve pas de tronc pulmo-cutané mais seulement une artère pulmonaire.
4 Les « reptiles ».
a Le cœur de tortue.
Le cœur de tortue présente deux oreillettes et un ventricule imparfaitement cloisonné.
On trouve le Cavum Pulmonale (CP), le Cavum Venosum (CV) et le Cavum Arteriosum (CA).
Le CP présente un début de cloisonnement.
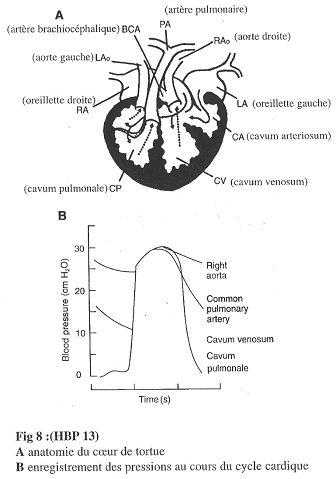
b Le cœur de Varan.
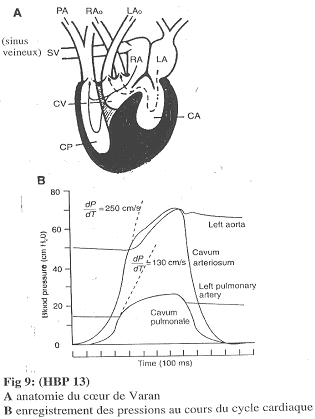
Le cœur de Varan présente deux oreillettes, un CP et un ensemble CV + CA.
Selon l’activité cardiaque, une cloison va bouger. En systole, cette cloison isole complètement le CP (la pression de part et d’autre de cette cloison devient alors différente). En diastole, il n’y a pas de cloison « parfaite ».
c Le cœur de Crocodile.
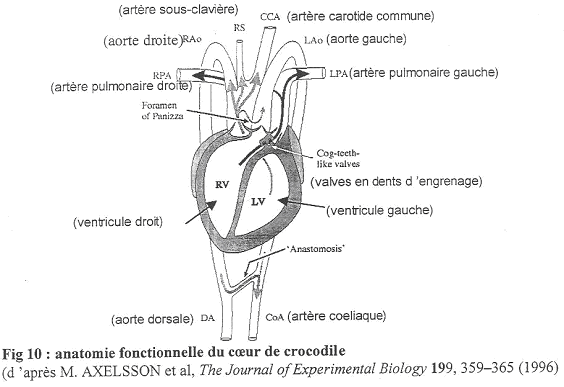
On distingue deux oreillettes ainsi que deux ventricules bien cloisonnés.
L’aorte gauche se fixe sur le ventricule droit alors que l’aorte droite prend son départ sur le ventricule gauche.
Remarques : Les reptiles ont toujours deux crosses aortiques. Ils présentent aussi plusieurs originalités :
- Le foramen de Panizza : il fait communiquer l’aorte droite et l’aorte gauche à leur départ des ventricules. Les mouvements de sang sont réalisés par la pression, ce qui fait que ce foramen peut être ouvert ou fermé. Le foramen de Panizza peut aussi être obturé par des valves artérielles.
- A la base de l’artère pulmonaire, on trouve une valve dentée qui peut être ouverte ou fermée, indépendamment des muscles (elle se ferme pendant une apnée). Cette valve permet le fonctionnement de l’aorte gauche.
5 Les oiseaux et mammifères.
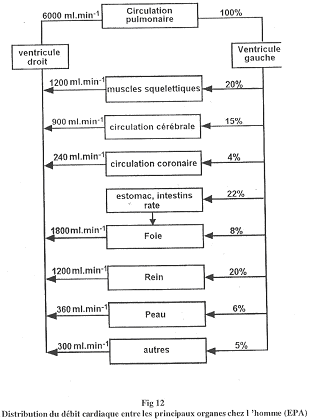
Les deux circulations (pulmonaire, du ventricule droit et systémique, du ventricule gauche) sont placées en série.
La mise en place de ces deux circulations permet d’avoir des pressions différentes selon le réseau.
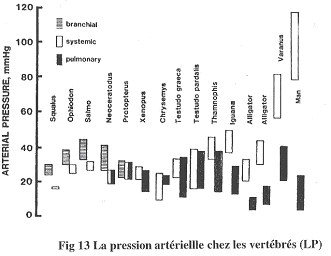
On étudie les pressions artérielles dans l’artère pulmonaire ou dans la branchie par rapport à la pression systémique.
Chez les poissons, la pression branchiale est supérieure à la pression systémique.
Chez les dipneustes et poissons associés, les pressions sont à peu près équivalentes.
Chez l’Homme, la pression systémique est largement supérieure à la pression pulmonaire. Le problème du poumon est qu’il est très vascularisé (environ 100m² chez l’Homme) et n’est une barrière de moins d’un micron d’épaisseur. Si la pression était trop forte, il y aurait un œdème pulmonaire qui pourrait être létal. Chez les crocodiliens et les varans, on trouve la même chose que chez l’Homme mais avec une moins forte amplitude.
Le cas particulier du fœtus :
Chez le fœtus, le poumon est non fonctionnel. Il existe deux dispositifs cardiaques permettant d’éviter d’envoyer du sang dans ces poumons.
- Le Foramen Ovale : Ce foramen est un trou entre les deux oreillettes. Le sang désoxygéné va rejoindre l’oreillette gauche, ce qui est tout simplement un court-circuit de la circulation pulmonaire.
- Le second dispositif prend en charge le sang qui est quand même passé dans l’artère pulmonaire. Ce dispositif va relier le tronc pulmonaire à l’aorte.
 Finalement, une faible quantité de sang arrivera à atteindre le poumon.
Finalement, une faible quantité de sang arrivera à atteindre le poumon.
A la naissance, le trou et le canal de dérivation se ferment.
II Physiologie Cardiaque.
A La pompe cardiaque.
1 Les Mammifères.
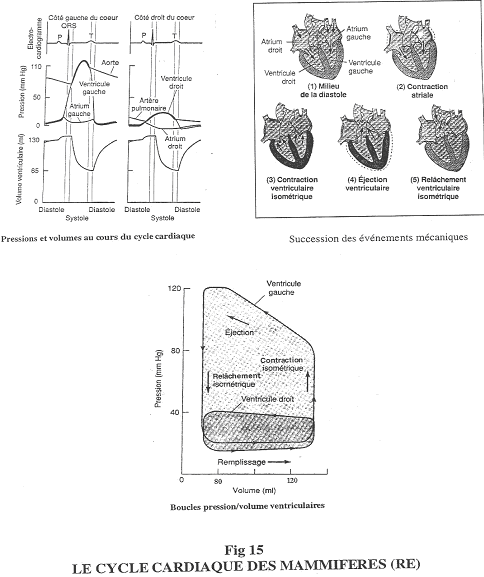
On étudie d’abord le volume ventriculaire, la pression. On réalise aussi un électrocardiogramme. Ces trois paramètres seront étudiés en fonction du temps.
La diastole montre une augmentation de volume. La systole montre, elle, une contraction avec diminution du volume ainsi qu’une augmentation de pression.
Au début, la contraction est iso volumétrique à fermeture des valves auriculo-ventriculaires.
Le ventricule se vide quand la pression ventriculaire devient supérieure à la pression aortique.
La systole est divisée en deux parties : une contraction iso volumétrique et l’éjection.
La pression va continuer à diminuer sans que le volume ne change à relâchement ventriculaire isoélectrique. Ensuite, le ventricule se remplie sous faible pression. A la fin du remplissage, il y a augmentation de la pression de l’oreillette gauche et une dernière augmentation du volume ventriculaire (grâce à la contraction de l’oreillette).
P : signal électrique pour la dépolarisation de l’oreillette.
Q, R, S : dépolarisation du ventricule.
T : repolarisation.
Du coté droit, on observe la même chose pour le ventricule. La pression est extrêmement faible dans l’artère pulmonaire.
Cf. figure 15, partie du bas :
Il n’y a pas de temps sur ce schéma.
2 Les poissons.
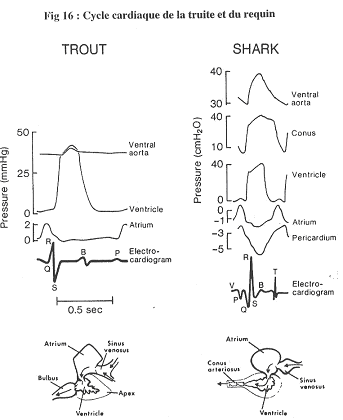
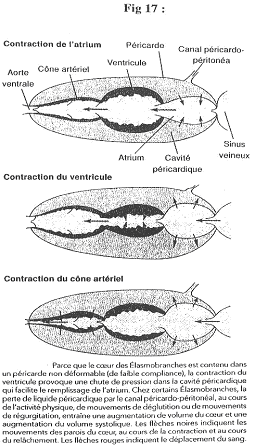
· La truite :
Pour ce poisson, on trouve le même type d’enregistrement que chez les mammifères. La contraction de l’oreillette précède celle de l’éjection ventriculaire.
· Le requin :
La contraction du cône artériel prolonge l’action du ventricule. La contraction de l’oreillette peut devenir négative (entre deux contractions). On dit négatif par rapport au milieu extérieur.
Dans ce cas, l’oreillette va donc aspirer le sang.
Dans le péricarde, la pression est toujours inférieure à zéro et inférieure à celle de l’oreillette.
La pression dans le ventricule diminue, ce qui entraîne une augmentation de la pression du péricarde. Hors, ce péricarde est rigide : quand le ventricule se contracte, il se crée donc une dépression à l’arrière qui aspire le sang et qui fait augmenter le volume de l’oreillette.
3 Les reptiles.
Revoir les figures 8 et 9.
· La Tortue.
Le ventricule est peu cloisonné. S’il ne l’est pas totalement, la pression dans le cavum pulomonale (CP) est égale à la pression dans le cavum venosum (CV) et dans le cavum arteriosum (CA).
Par conséquence, il y a aura une augmentation de pression identique dans l’aorte droite ou dans l’artère pulmonaire (même pression dans les deux cas). Ce phénomène est un problème pour le circuit ventilatoire qui demande une basse pression.
· Le Varan :
Chez le varan, il y a un cloisonnement étanche de temps en temps. En systole, le CP s’isole ce qui entraîne une augmentation de pression dans le CP qui est beaucoup plus faible que dans le CA. è La pression artérielle pulmonaire est inférieure à la pression aortique. On a alors une circulation à basse pression en série avec une circulation à haute pression.
· Le Crocodile :
On trouve deux aortes (droite et gauche) mais l’aorte gauche ne va généralement pas recevoir de sang. De plus, au départ de cette aorte gauche, on va trouver une valve dentée. Entre ces deux aortes, il existe le foramen de Panizza qui laisse passer le sang de la haute pression vers la basse pression.
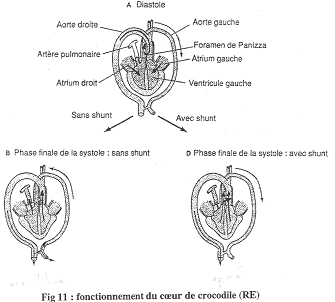
En A, on a la phase de diastole ; les figures B et D montre la systole avec un shunt en B et sans shunt en D. La pression est différente dans le ventricule droit et dans le gauche : elle est supérieure dans le ventricule gauche.
Le relâchement du cœur va permettre le remplissage par l’oreillette.
En A : Dans les aortes, le sang circule de l’aorte droite vers la gauche (la pression aortique droite est supérieure à la pression aortique gauche).
En B : Les ventricules doit et gauche se contractent. Le sang du ventricule droit passe dans l’artère pulmonaire mais la pression y est trop faible pour permettre le passage vers l’aorte gauche. Le sang du ventricule gauche part dans l’aorte droite. La valve sigmoïde vient se plaquer sur le foramen de Panizza et l’obstrue : il n’y pas de passage de sang.
En C : En plongée, il va y avoir fermeture de la valve dentée. La pression ventriculaire est inférieure à la pression aortique gauche. Ceci évite donc la circulation pulmonaire. Il y aura passage de sang (peu de pression dans le ventricule gauche) de l’aorte gauche vers l’aorte droite car le foramen de Panizza n’est pas fermé (avec shunt). On observe ainsi un court-circuit de la circulation pulmonaire.
B Le muscle cardiaque.
1 Structure d’un cardiomyocyte.
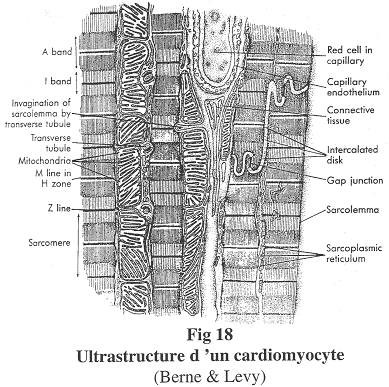
Les cardiomyocytes sont des cellules uni-nucléées. Elles sont dites striées car en microscopie optique, on observe des stries.
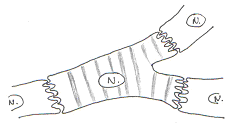
Ces cellules montrent des jonctions particulières : des jonctions pour la résistance et des desmosomes. On trouvera aussi des jonctions de type GAP qui jouent le rôle de synapse électrique ou de jonction communicante.
Bien que l’on ait plusieurs cellules différentes, la dépolarisation passe d’une cellule à l’autre sans intervention de neuromédiateurs (cela se passe comme si l’on n’avait qu’une seule cellule).
Les striations transversales montrent la présence de sarcomères qui sont des agencements particuliers d’actine et de myosine. Cet agencement est proche de l’agencement cristallin. De plus, tous les sarcomères sont alignés.
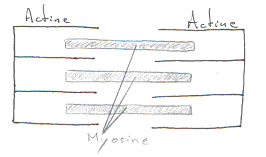
On trouvera dans ces cardiomyocytes de grandes quantités de mitochondries, des capillaires sanguins entre deux fibres, des disques intercalaires ou stries scalariformes (ancien terme) qui sont des jonctions entre deux cardiomyocytes. Les parois des cardiomyocytes sont proches mais ne se touchent pas. On a aussi un réticulum sarcoplasmique abondant qui permet le stockage de Ca2+, la libération de ce calcium pour l’action sur des protéines contractiles.
2 Propriétés du muscle cardiaque.
a Couplage électromécanique.
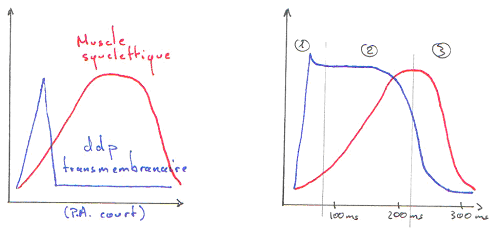
Le plateau du potentiel d’action dure aux alentours de 0,2 seconde.
La période réfractaire (PR) est la période pendant laquelle la structure ne réagit pas après avoir été stimulée.
La période réfractaire des muscles est de quelques millisecondes. Cette durée permet la fusion des contractions et la mise en place d’un tétanos ; ce qui est « normal » pour un muscle strié.
La période réfractaire du muscle cardiaque est longue. La période réfractaire absolue est d’environ 200 millisecondes : on ne peut donc pas tétaniser le muscle cardiaque.
Le potentiel d'action cardiaque est calcique alors que le potentiel d'action musculaire ou neuronal est sodique.
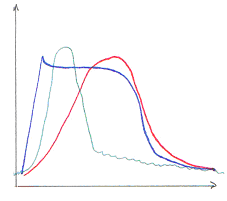
Pour mesurer la concentration en calcium dans la cellule, on va utiliser des sondes moléculaires comme l’Aequorine. Cette dernière devient fluorescente avec le Ca2+. La sortie de calcium (cardiaque) ressemble à celle du muscle strié squelettique.
Pendant la première phase, montée de potentiel, un canal électrosensible permet l’entrée de Na+ et s’ouvre quand la membrane se dépolarise : il va y avoir une boucle qui dépolarise la membrane.
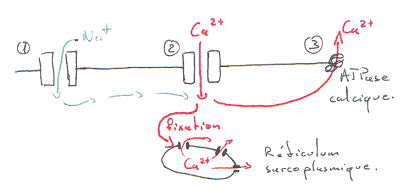
La phase de plateau est principalement due au calcium. Pendant la phase descendante, le calcium est pompé dans la cellule par une calcium-ATPase.
La différence de potentiel transmembranaire se passe de part et d’autre de la membrane. Les premiers ions calcium entrant (extracellulaires) vont aller stimuler la sortie de Ca2+ du réticulum sarcoplasmique. Ce canal à calcium est appelé RYR ou récepteur de la ryanodine (molécule végétale).
Le calcium cytoplasmique va aller agir sur les sarcomères, un peu comme dans le muscle strié squelettique. L’amplitude de la contraction va dépendre du niveau de Ca2+ du réticulum et de la sensibilité de l’appareil contractile, au Ca2+.
Le flash calcique est bref car ce calcium est re-pompé dans le réticulum par une calcium-ATPase (de type Serca).
Remarque : Dans le muscle strié, 50% de l’ATP est utilisé pour la contraction et l’autre moitié sert à faire rentrer le calcium dans le réticulum sarcoplasmique.
Les Serca peuvent être inhibées par le phospholamban (protéine complexe).
b Effets inotropes de la Noradrénaline.
L’action de la noradrénaline se fait sur la contraction du muscle cardiaque. Elle va augmenter cette force de contraction. La noradrénaline se lie sur un récepteur B2 adrénergique membranaire et entraîne la formation d’AMPc. Une PKa va être stimulée et va phosphoryler des cibles spécifiques :
- Canal calcium (qui voit son activité augmenter),
- Le PLB (phospholamban) qui est une protéine liée à la pompe Ca/ATPase, pompe qui fait entrer le Ca vers le réticulum endoplasmique.
Le calcium participe à l’augmentation de calcium dans le réticulum endoplasmique et permettant une plus forte vague calcique. Il agit aussi en stimulant la pompe, se qui fait rentrer le calcium dans le réticulum endoplasmique et ce qui raccourci ainsi la durée du flash (et un relâchement plus rapide). Dans ce cas, l’activité Serca augmente.
 Finalement, on peut dire que tous ces effets entraînent un meilleur remplissage du cœur.
Finalement, on peut dire que tous ces effets entraînent un meilleur remplissage du cœur.
- La phosophoryl-Troponine I diminue l’affinité du calcium pour la troponine C et qui entraîne donc une augmentation du relâchement de la fibre musculaire.
Remarque : Le cœur présente des récepteurs muscariniques pour l’acétylcholine. L’acétylcholine va diminuer la force de contraction. Ces récepteurs n’existent que dans l’oreillette.
Lors de stimulations par le système nerveux :
- Sur le ventricule, si la stimulation a pour origine le système nerveux orthosympathique, on observe des potentiels d’actions plus hauts et plus longs (la noradrénaline agit sur les canaux calcium).
- Sur le ventricule, le système nerveux parasympathique n’a aucun effet.
 Le système orthosympathique agit par un accroissement de la vitesse de contraction et de la force maximale. Il diminue la vitesse de décontraction (relâchement).
Le système orthosympathique agit par un accroissement de la vitesse de contraction et de la force maximale. Il diminue la vitesse de décontraction (relâchement).
- Sur l’oreillette, les effets du système nerveux parasympathique sont opposés é ceux du système nerveux orthosympathique.
c Effet de la longueur du muscle cardiaque sur sa contraction.
Courbes tension/longueur.
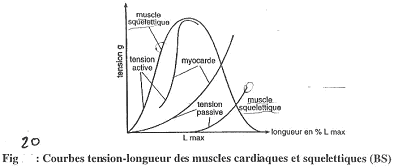
Une tension passive est une tension non provoquée par l’élément.
Une tension active est une tension réalisée par l’élément.
La relation entre tension et longueur est fonction de l’élasticité. Si les fibres sont peu élastiques, on aura beaucoup de tension alors que beaucoup d’élasticité entraîne l’existence d’une faible tension.
Tension active : courbes en cloches.
On a une longueur maximale pour le meilleure contraction : elle est liée à la longueur des sarcomères.
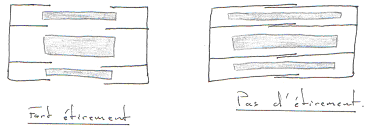
La force développée est fonction du nombre de liaisons actine/myosine.
Le muscle cardiaque développe une force passive tellement grande qu’il ne peut pas s’étirer plus (grâce aux fibres de collagène).
La notion de précharge : La précharge est la façon dont le muscle ventriculaire est étiré pendant la diastole è le remplissage conditionne la contraction.
C L’autonomie cardiaque et le contrôle de la fréquence cardiaque.
Notions de base : cf. DEUG.
L’origine de l’automatisme cardiaque est intrinsèque, comprise dans le tissu nodal (dans l’oreillette droite). Il y a stimulation de cellules en cellules dans le tissu auriculaire. Entre les oreillettes et les ventricules, on trouve du tissu isolant. La stimulation est relayée par le nœud auriculo-ventriculaire, puis le faisceau de Hiss et celui de Parkinje.
1 Origine et propagation de la stimulation.
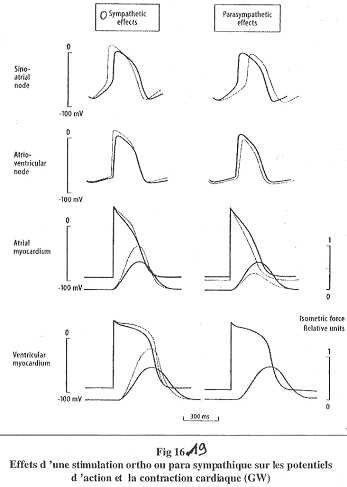
Dans la majorité des cellules, on a un potentiel de repos de l’ordre de -60mV. Dans les cellules du nœud sinusal, le potentiel de repos est instable, ce qui provoque des dépolarisations spontanées grâce à un canal responsable du courant entrant à IF (Na, K). IF s’ouvre à l’hyperpolarisation. Quand le seuil est atteint, la valeur atteinte permet l’ouverture de canaux voltage dépendants. Ici, ce sont des canaux calcium (voltage dépendants).
Il vient ensuite la phase de repolarisation par ouverture de canaux K. L’hyperpolarisation donne le début d’un nouveau cycle. La fréquence atteinte est d’environ 100 dépolarisations par minute.
Pour le nœud auriculo-ventriculaire, on trouve la même chose sauf que le fréquence spontanée est différente (environ 40 dépolarisation par minute).
 Finalement, on trouve deux endroits capables d’automatisme mais seul le nœud sinusal s’exprime.
Finalement, on trouve deux endroits capables d’automatisme mais seul le nœud sinusal s’exprime.
2 Effets des neuromédiateurs du système nerveux végétatif.
(Système nerveux parasympathique à NAd, Système nerveux orthosympathique à ACh).
Une stimulation du système nerveux orthosympathique entraîne une augmentation du courant de fuite alors que l’acétylcholine (ACh) provoque l’inverse.
Le système nerveux orthosympathique va augmenter la vitesse de dépolarisation et donc accélérer le cœur.
Le système nerveux parasympathique diminue cette vitesse de dépolarisation et donc, ralentit le cœur.
Les effets chronotropes s’expliquent principalement par cet effet sur le courant IF.
La PKA augmente l’activité du canal IF par phosphorylation. Selon l’état de phosphorylation des canaux, les potentiels d'action seront plus ou moins importants.
L’ACh entraîne la présence de potentiels plus faibles et des repolarisation plus tardives. L’ACh a un effet direct sur les canaux K+ par l’intermédiaire de protéines Gk.
D Le débit cardiaque.
Dc = Fc x Ves
Pour un humain, Dc de repos est d’environ 5 litres par minute.
1 Notion de précharge.
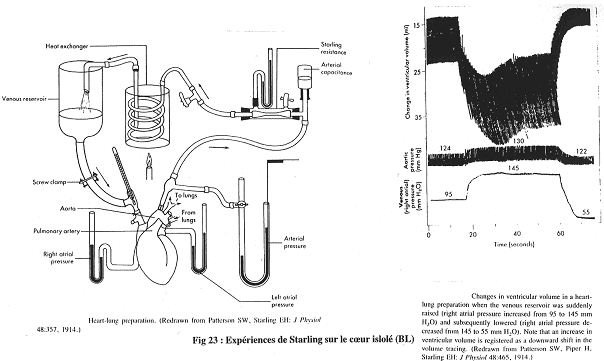
Sur cette expérience, on utilise un cœur isolé et perfusé de façon physiologique.
Le sang passe de l’oreillette droite au ventricule droit puis aux poumons ; il continue par l’oreillette gauche, puis le ventricule gauche et passe enfin dans l’aorte.
Sur le graphe, il manque le graphe du mécanisme de mesure du volume ventriculaire.
L’objectif de Starling est de voir si lorsque l’on augmente la pression de remplissage, le débit cardiaque (Dc) augmente.
Quand on monte le réservoir, la pression de l’oreillette droite augmente.
A 95, on a 1 hauteur.
Si la pression de remplissage augmente, l’étirement ventriculaire augmente, ce qui entraîne l’accroissement du volume d’éjection systolique (Ves).
Ves
Volume télé-diastolique
 Expérimentalement, pour augmenter le volume, on augmente la pression de remplissage (on peut trouver « Pression de remplissage » à la place du volume télé-diastolique).
Expérimentalement, pour augmenter le volume, on augmente la pression de remplissage (on peut trouver « Pression de remplissage » à la place du volume télé-diastolique).
Un effet de la précharge est que le temps de décharge est plus long : D – D’ à index de la contraction cardiaque.
Le Ves peut s’adapter par rapport au retour veineux (ce qui permet aux personnes âgées de pouvoir faire du « sport »).
2 Limitation du Ves par la postcharge : résistance.
La postcharge est tout ce qui s’oppose à l’éjection ventriculaire. Ici, on va jouer sur la pression de l’aorte.
La fonction d’éjection s’effectue quand la pression ventriculaire est supérieure à la pression aortique ; la pression artérielle diastolique agit constamment sur le ventricule.
Donc, si l’on augmente la pression artérielle, la valvule s’ouvrira plus tard, le ventricule se contractera donc aussi plus tard. La décharge devra également être plus rapide (car la pression artérielle est importante).
Les valves s’ouvrent plus tard et se ferment plus tôt : le phénomène d’éjection est plus court ; or, le travail cardiaque ne varie pas (l’aire ne change pas) mais c’est le système qui devient moins efficace. è Si l’on veut obtenir un même Ves, il faut augmenter la contractilité, donc, le travail cardiaque. C’est ce qui arrive dans les cas d’hypertension artérielle.
Remarque : La fonction de postcharge dépend aussi des propriétés extensives de l’aorte.
3 La contractilité.
LA force de contraction dépend de la précharge (durée d’étirement).
La contractilité est l’aptitude à se contracter quel que soit l’étirement ventriculaire.
Ici, Ves augmente mais dans chaque cas, D, D’ et D’’ ne définissent pas une droite. Quand on a une augmentation de la contractilité, on augmente le travail du cœur même si la précharge reste identique.
4 Conclusion et réaction in vivo.
L’exemple de la Noradrénaline.
Cette molécule augmente la force de contraction, la fréquence, le remplissage (volume), mais aussi augmente le retour veineux et la postcharge : tous ces facteurs ne sont donc pas indépendants.
|
|
Fréquence
|
Contractilité
|
Vitesse de conduction
|
Débit
|
|
Orthosympathique
|
+
|
+
|
+
|
+++
|
|
Parasympathique
|
-
|
0
|
0
|
---
|
Pour le système orthosympathique, l’effet le plus marqué est sur la fréquence : de plus, la vitesse et la fréquence sont étroitement liées (propriétés voisines sues au tissu nodal).
Quand la fréquence est lente, la durée du cycle est grande et inversement.
Quand la fréquence augmente, la diastole est moins importante (moins de temps pour remplir le ventricule), donc, ici, l’effet relaxant de la noradrénaline est plus important.
En effet, si l’on se trouve à de hautes fréquences, c’est la diastole qui sera le plus affectée : la durée d’une systole diminue aussi mais bien moins, à cause de la vitesse et de la force de contraction.
La fréquence et la contractilité sont liées sur un cœur entier et la seule manière de les dissocier expérimentalement est faite par logiciel (Cf. TP).
E Métabolisme cardiaque et circulation coronaire.
1 Les endothermes.
a Le métabolisme du cœur.
Le métabolisme du cœur correspond à ses besoins.
C’est un métabolisme très aérobie où va se dérouler l’oxydation des nutriments, ce qui explique son fort taux de mitochondries (le plus fort du corps).
En période de repos, les substrats préférentiels de l’oxydation sont les acides gras libres (70%) avec 30% de glucides. Durant l’exercice, c’est un autre substrat qui va être oxydé : ce sont les lactates. Ces derniers proviennent des muscles squelettiques (environ 60%).
Le pourcentage de glucose dépend de la glycémie selon chaque individu.
Le métabolisme anaérobie est très peu développé dans la fonction cardiaque : le cœur se nécrose très vite, donc, si un problème a lieu dans la circulation coronaire, cela est très grave (infarctus).
b La circulation coronaire.
Il existe une circulation par ventricule.
La capacité d’anastomose est peu importante : en effet, un territoire de tissu cardiaque est irrigué par une seule voie ; donc, si une artère se bouche, tout un secteur ne sera plus irrigué (problème d’autant plus important que le barrage est en amont de la circulation).
L’artère coronaire pénètre dans la paroi des ventricules et lors d’une contraction systolique du ventricule, l’artère coronaire s’écrase (diminution du débit).
On assiste donc à une fonction paradoxale : lors de la systole, le débit est faible alors qu’en diastole, ce débit est plus fort. Quand la fréquence augmente, , la diastole diminue, donc, le temps d’irrigation coronaire diminue également. Toutefois, ce système fonctionne. Au repos, le débit de cette circulation est de 0,25L/minute. Durant l’exercice, ce débit passe à environ 1,3 litre/minute. è Le débit coronarien s’adapte donc.
Si l’on prélève du sang dans l’artère et dans la veine pulmonaire, et que l’on mesure la PAV : le taux d’oxygénation du débit artério-veineux est toujours maximal, c'est-à-dire que le myocarde est un grand extracteur d’O2 et s’il doit consommer plus d’O2, sa seule solution est d’augmenter les débits coronariens. C’est une différence par rapport aux cellules classique qui ont toujours des réserves (le DAV n’est pas maximal).
2 Les ectothermes (reptiles, amphibiens).
a Le métabolisme du cœur.
Le problème chez les ectothermes est que le tissu cardiaque est en hypothermie : on assiste à des problèmes de fibrillations qui sont asynchrones au niveau de la contraction.
Ici, le cœur fonctionne en anaérobie, ce qui lui confère une résistance à l’anoxie et aussi, un affranchissement vis-à-vis de la température.
b La circulation coronaire.
Le cœur, en général, es poissons, n’a pas de circulation coronaire. Il possède des travées, ce qui lui confère des propriétés spongieuses : il s’imprègne de sang qui provient de la cavité péricardique. Le problème est que ce sang est pauvre en O2.
Au cours de l’évolution, certains poissons voient un système coronaire apparaître mais celui-ci est limité seulement à l’épicarde (juste la couche externe).
On peut donc considérer que a circulation pulmonaire a été sélectionnée chez les poissons car cela permet un avantage : il y a un apport de sang oxygéné dans la cavité péricardique et il ya donc augmentation de l’oxygénation cardiaque.
F Fonction endocrine du cœur.
L’hormone principale produite par le cœur est l’ANF (Atrium Natriurétique Factor ; vieux terme) ; c’est une hormone qui augmente la natriurèse (diminution urinaire de Na+). L’oreillette sécrète l’ANP (nouveau terme) quand elle est distendue. Cette distension est directement la conséquence de la volémie.
On trouve une boucle de régulation. Au niveau de l’oreillette, on a des volorécepteurs qui mesurent la volémie. Si cette dernière est excessive, il y aura sécrétion d’ANP (et natriurèse + diurèse juste après). La volémie reprendra ensuite une valeur normale.
Rappel : Les stimuli pour la synthèse d’ADH (hormone anti-diurétique).
On trouve comme stimuli efficaces : la pression osmotique hypothalamique et la diminution du volume des oreillettes. è Récepteurs et organes sécréteurs vont participer à la synthèse et à la régulation hydrominérale.
III Physiologie vasculaire.
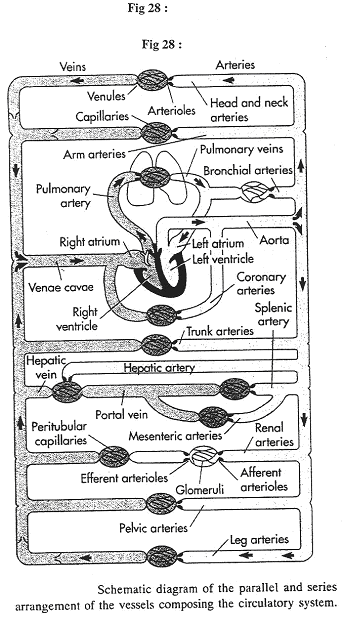
Revoir la figure 6.
Ce document montre les cotés gauche et droit égaux car parallèles.
Sur le document 28, on observe le système porte hépatique : on trouve une succession de deux réseaux de capillaires, ce qui est rare.
Au niveau du rein, on trouve des artérioles afférentes et efférentes séparées par des glomérules.
Au niveau du cœur, on va trouver un petit mélange de sang oxygéné avec du sang venant des veines bronchiques : les veines et capillaires bronchiques se déversent dans les veines pulmonaires : on peut différemment avoir 100% de saturation en O2 dans le sang.
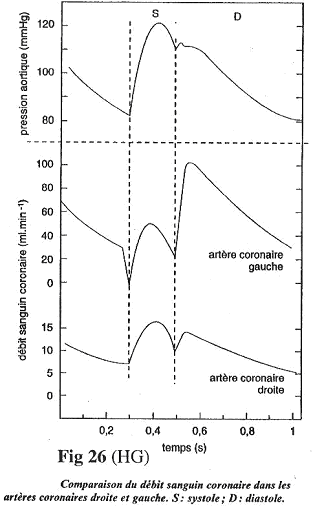
La circulation coronaire a la particularité, lorsque le cœur se contracte, de comprimer les artères coronaires (normal). Si on étudie le débit dans les artères coronaires gauches, on observe deux phases : une où la circulation est faible et une où la circulation remonte
 L’irrigation du myocarde est essentiellement diastolique.
L’irrigation du myocarde est essentiellement diastolique.
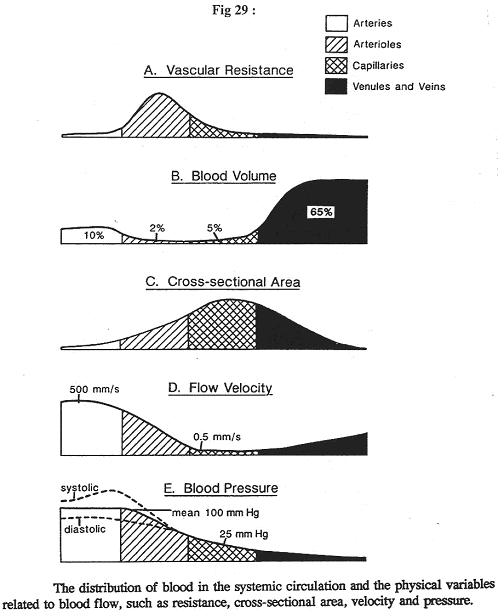
Dans cette figure, le sang circule de la gauche vers la droite.
En A, on étudie la pression moyenne. Elle diminue tout le temps, de l’entrée à la sortie : c’est ce qui fait avancer le sang. La diminution de pression est plus élevée à l’entrée qu’à la sortie. Elle ne remonte jamais.
Si l’on rajoute l’anatomie du système, on aura une surface de sections cumulées (surface de coté X nombre de vaisseaux) :
- Au niveau de l’aorte, la surface est multipliée par 1 (1 vaisseau).
- Au niveau des veines caves, on multiplie par 2
- Pour les capillaires, il faut multiplier par des milliards, ce qui montre une très grande surface de capillaires. Cette surface a une conséquence immédiate sur la vitesse du flux.
En D, le débit à l’entrée des capillaires est égal au débit au milieu et au débit de sortie. Or, si le débit est constant, la vitesse est très différente. è La vitesse capillaire est 1000 fois plus faible que la vitesse dans l’aorte. Après les capillaires, il y a une ré-augmentation de la vitesse du flux sanguin.
A un moment donné, on se demande où est le sang. En fait, les 2/3 de la masse sanguine se trouvent dans le compartiment veineux où la pression est plus faible. è Le système circulatoire n’est pas homogène.
Le sang artériel ne représente que 10% de la masse sanguine. De plus, il y est en mouvement à vitesse très rapide.
A Structure des vaisseaux.
1 Structure de base.
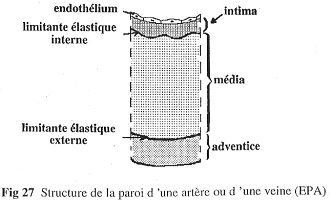
Les vaisseaux sont pratiquement tous sur ce modèle : trois parties (intima, média et adventice).
· L’intima :
Cette partie est toujours présente. Elle est formée d’un endothélium très fin et très plat. On pourra trouver une couche sous-endothéliale qui se développe surtout avec l’âge. L’intima a la même structure embryologique que l’endocarde.
· La média :
Cette partie est formée de cellules musculaires lisses et/ou de fibres élastiques.
· L’adventice :
Dans cette partie, on trouve peu de cellules. On a surtout du collagène. C’est un « emballage » un peu rigide qui permet d’éviter les déchirements.
2 Comparaison des différents vaisseaux.
Pour comparer les vaisseaux, on a deux niveaux distincts : niveau fonctionnel et niveau histologique.
Au niveau histologique, on peut comparer une veine et une artère de même calibre (même débit) : l’artère a une paroi plus épaisse. Ceci est facile à voir car les veines et artères ont des structures voisines.
Si l’on regarde des sections de veines et d’artères, on s’aperçoit que dans les veines, l’adventice représente environ la moitié de la paroi, ce qui n’est jamais le cas dans les artères.
3 Evolution de ces structures.
Les grandes artères sont des artères élastiques car la média contient quasi uniquement des fibres élastiques.
Les artères de plus petits calibres sont dites musculaires car la média contient plus de cellules musculaires lisses que de fibres élastiques.
Les artérioles sont particulières car il n’y a plus d’adventice. On ne trouve plus que des cellules musculaires lisses et l’intima, cette dernière étant exclusivement formée de l’endothélium et de sa lame basale.
Entre les artérioles et les veinules, il existe un réseau de capillaires uniquement formés d’un endothélium (et de sa lame basale). Inégalement répartis, on trouve aussi des péricytes dont le rôle est peu connu (contraction, etc. …).
 Il faut bien comprendre que ce réseau peut être constitué par anastomose ; tout dépend de l’ouverture et de la fermeture des sphincters. à Tous ces réseaux capillaires ne sont pas ouverts en même temps. Ils sont ouverts en fonction des besoins.
Il faut bien comprendre que ce réseau peut être constitué par anastomose ; tout dépend de l’ouverture et de la fermeture des sphincters. à Tous ces réseaux capillaires ne sont pas ouverts en même temps. Ils sont ouverts en fonction des besoins.
Les veinules sont assez différentes des artérioles : l’adventice revient mais pas la média.
Dans les veines, la média revient mais elle est plus fine que l’adventice. La conséquence est que la force de constriction des veines est plus faible que celle des artères.
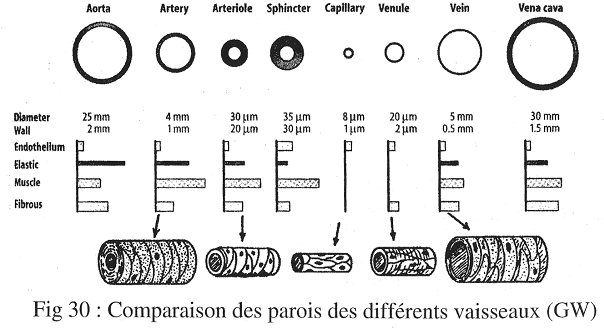
B Dynamique des fluides.
Les lois ont une limite dans leur utilisation car elle ne s’applique qu’aux fluides dont la viscosité est constante. Or, ici, les fluides ont des caractéristiques de différents paramètres : les lois de la dynamique des fluides ne s’appliquent pas partout mais elles permettent quand même d’expliquer certains phénomènes.
1 L’écoulement sanguin.
On distingue deux types d’écoulement : l’écoulement laminaire et l’écoulement turbulent.
L’écoulement laminaire se déroule comme si le liquide était divisé en strates glissant les unes sur les autres : on admet que ça peut être la réalité. Au contact du substrat, la vitesse devient quasiment nulle. Finalement, il se fait un gradient de vitesse (gradient laminaire). Dans un vaisseau sanguin, le profil d’écoulement est un peu différent : on a un profil parabolique.
Un intérêt de ce système est que la zone de frottements minimum est au niveau de la paroi car là, la vitesse est nulle (ou presque) et il n’y a pas (ou presque pas) de frottements. Un autre intérêt est la régularité de l’écoulement ainsi que l’absence de turbulences qui rompraient cet écoulement.
Dans le cas de turbulences, les profils de vitesse deviennent anarchiques et il y a aussi perte d’énergie par des chocs qui ne servent à rien. Les frottements obtenus par ses turbulences seraient la source de vibrations et de nombreux autres effets inutiles.
 Quand l’écoulement devient turbulent, cela s’entend au stéthoscope (à souffle au cœur).
Quand l’écoulement devient turbulent, cela s’entend au stéthoscope (à souffle au cœur).
Comment se fait le passage d’un type d’écoulement à l’autre ?
C’est le nombre de Reynolds (Re) qui permet d’expliquer le passage d’un courant à l’autre. Ce nombre dépend de la vitesse (V), du diamètre (D) et de la viscosité (µ) : Re = (V.D)/µ .
Moins un fluide est visqueux, plus le nombre de Reynolds est grand.
Pour un liquide donné, plus la vitesse d’écoulement est grande, plus il y a de risques d’y avoir des turbulences.
Pour une vitesse donnée et un liquide donné, plus le diamètre est grand, plus le risque d’avoir des turbulences est important.
Au niveau des artères on peut assister à la formation de sténoses, des pincements des artères. Comme le débit d’entrée est égal au débit de sortie et ceci, partout, les vitesses sont plus grandes au niveau des sténoses que de part d’autre de l’une d’elle.
Quand Re augmente, des turbulences sont créées et l’on peut donc entendre la circulation : on peut alors faire des mesures.
Les problèmes pathologiques liés à ces effets sont nombreux : on peut citer l’artériosclérose, surtout aux bifurcations.
2 La loi de Poiseuille.
Cette loi est similaire à la loi d’Ohm (U = R.I).
DP = R . débit è Débit = DP/r
En pratique : R = (8L*µ) / pR4 .
L est la longueur du vaisseau, r est le rayon de ce vaisseau.
Donc :
- Plus le tube est long, plus il y a de résistance.
- Pour m, plus le liquide est visqueux, plus il y a de résistance.
- Pour r, plus le rayon est petit, plus la résistance est grande.
 Il y a un fort impact du rayon sur la résistance de ces vaisseaux (puissance 4).
Il y a un fort impact du rayon sur la résistance de ces vaisseaux (puissance 4).
Si l’on s’intéresse à l’organisme en entier, globalement, la résistance ne varie pas qu’en fonction du rayon.
Revoir la figure 29.
On peut voir que les plus fortes résistances se trouvent dans les artérioles : c’est là où il y a une chute considérable du diamètre. Inversement, la chute de la pression sanguine, à ce niveau là, est due à l’augmentation de la résistance.
Au niveau des artères élastiques, il n’y a qu’une résistance extrêmement faible è la diminution de pression artérielle moyenne est donc quasiment nulle.
La tension :
Remarque : Quand on parle d’hypertension, en réalité, on parle d’hyper pression !
Les notions de pression et de tension ne sont pas identiques : la confusion des deux est un abus de langage.
T = P*r (T est la tension ; P la pression ; r le rayon).
Plus la pression augmente, plus la tension augmente. On a la même chose quand le rayon augmente. Dans le cas de fortes viscosités, il se développe une tension plus forte.
Par exemple, dans les artérioles, il se développe une pression élevée (le ¼ de la pression aortique) pour une paroi 100 fois plus fine. Cette paroi ne se déchire pas car ici r est petit et T est donc faible.
Dans le cas de l’aorte, on se trouve dans des conditions maximales : le diamètre est le plus grand possible et la pression, la plus forte possible. Il n’y a pas de déchirement car la paroi est très solide (composée de fibres élastiques).
C Hémodynamique (dynamique des fluides appliquée au sang et aux vaisseaux).
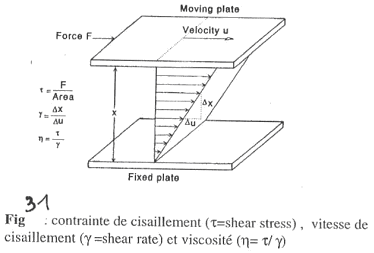
La plaque du dessus se déplace par rapport à celle du bas qui est fixée. On va ensuite définir la vélocité de la plaque supérieure en fonction de la surface et des forces développées.
t = F/Aire (S) à on obtient la dimension d’une pression. Mais il faut faire attention car F est tangentielle car c’est une force de cisaillement.
g est la « shear rate » ou vitesse de cisaillement. Du est la différence de vitesse alors que Dx est le gradient de vitesse.
 h = t/g . Cette valeur (h) diminue (donc les frottements) quand g augmente. à En pratique, plus le sang circule vite, moins celui-ci est visqueux (= comportement rhéo-fluidifiant). Par exemple, la peinture est de moins en moins visqueuse quand on la mélange de plus en plus.
h = t/g . Cette valeur (h) diminue (donc les frottements) quand g augmente. à En pratique, plus le sang circule vite, moins celui-ci est visqueux (= comportement rhéo-fluidifiant). Par exemple, la peinture est de moins en moins visqueuse quand on la mélange de plus en plus.
Quand la vitesse est faible, on obtient un empilement de globules rouges, ce qui rend le sang très visqueux. Au fur et à mesure que g augmente, les interactions entre globules rouges changent et il y a dissociation et donc, fluidification (h diminue).
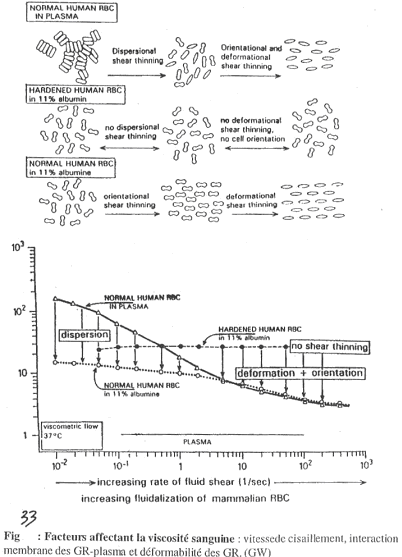
On observe sur ce graphe la viscosité relative par rapport à celle du plasma qui est donnée à une valeur de 1.
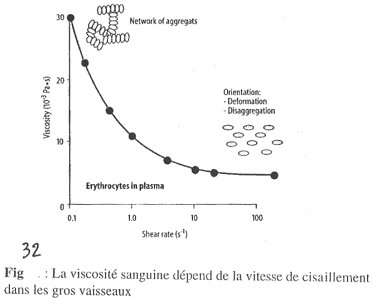
Sur ce graphe, on observe la viscosité réelle.
Sur la figure 33, les triangles blancs représentent la courbe normale, avec les globules rouges en suspension dans le plasma (à sang normal).
La courbe désignée par les ronds blancs représente des globules rouges humains normaux en suspension dans une solution d’albumine : 11% d’albumine représente 110g/L et donne une valeur de h égale à celle du plasma).
Avec de fortes valeurs de g, on ne voit pas de différence avec la courbe normale.
Pour de faibles valeurs de g, l’accroissement de h n’est pas très important car il n’y a pas d’agrégation des globules rouges car les protéines plasmatiques nécessaires à cette agrégation sont absentes.
Pour la courbe désignée par des ronds noires, on ne prend pas de globules rouges normaux mais des globules rouges durcis par le glutaraldéhyde. Ces globules ne sont pas déformables et les empilements sont maintenant impossibles. Ces globules rouges sont dans de l’albumine.
Pour de faibles valeurs de g, il n’y a pas d’augmentation de h.
Pour de forts g, il n’y a pas de diminution de h : aux fortes valeurs de g, le globule rouge passe d’une forme bicaténaire à une forme ovoïde è C’est une orientation de la circulation. Cette mise en forme ovoïde est inhibée dans ce cas par le glutaraldéhyde.
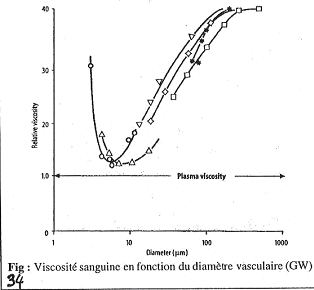
Ce document permet d’étudier l’influence du diamètre sur la viscosité sanguine. Il faut bien remarquer que la fluidité du plasma ne varie pas avec g.
Sur cette figure, quand un vaisseau a un diamètre de 1000mM, on a h qui est 40 fois plus grande que celle du sang.
S’il y a diminution du diamètre, h va diminuer. On a ceci jusqu’à 10mM où l’on trouve la valeur de h minimale.
Dans les petits vaisseaux, la viscosité du sang devient proche de celle du plasma (attention, 10mM n’est pas le plus petit diamètre existant).
Quand le diamètre diminue, on observe la chute de h ; cette chute est due à une séquence de phénomènes qui se déroule : les globules rouges se trouvent au milieu et le plasma autour.
Il y a un élément très important : l’hématocrite. Pour calculer cette hématocrite, on prélève une goutte de sang que l’on place dans un tube très fin de 7 à 8 centimètres de long pour un diamètre de 0.25 millimètre. On centrifuge et l’on mesure les hauteurs.
L’hématocrite (Ht) est égale à h/H. plus il y a de globules rouges, plus la viscosité sera grande.
L’hématocrite moyenne est de 0.45. Le maximum autorisé est de 0.5. Les problèmes liés à l’hématocrite sont surtout circulatoires : on peut trouver de graves thromboses arrivant à provoquer la mort.
Les parois des vaisseaux ont plus ou moins de couches et sont plus ou moins étirables. Ces vaisseaux sont des organes creux et ont donc une compliance : DV/DP.
Comparaison de la compliance des veines et des artères.
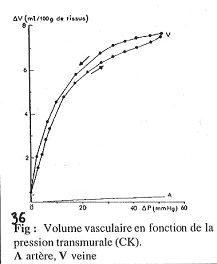
La compliance est la pente des courbes ; quand le maximum est atteint, la compliance est nulle. On observe que les veines ont toujours une compliance beaucoup plus élevée que les artères. Cette observation doit toutefois être nuancée.
En effet, on trouve des différences de pression entre les veines et les artères : Si l’on se met à pression élevée dans les deux systèmes, on observera que dans les veines, la compliance devient très faible, voir nulle.
Dans les veines, cette forte compliance permet une augmentation de volume dans le cas des fortes pressions (pressions restant d’ordre physiologique).
Les vaisseaux sanguins sont doués d’une certaines contractilité.
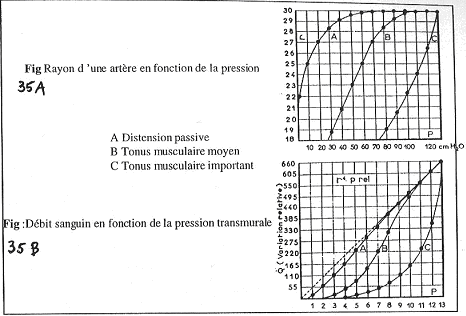
Dans le document A, sur la courbe A, on observe une distension passive. A l’atteinte de la valeur maximale, on se trouve au maximum d’étirement.
Sur la courbe B, Si le tonus musculaire augmente, le rayon va diminuer et faire obtenir une nouvelle compliance.
Sur la courbe C, le tonus musculaire est encore plus fort : on obtient une nouvelle courbe de compliance mais celle-ci ne devient jamais nulle !
Dans le document B, on mesure maintenant le débit, et non plus, le diamètre. Normalement, le débit est fonction du diamètre et de la pression. On s’attend donc à obtenir une droite. La pente dépend de R et donc, du rayon.
Or, ceci n’est vrai que pour de fortes pressions et pas pour les petites. En fait, on a une diminution de la pression, et du rayon, ce qui fait chuter le débit. Il y a fusion quand le diamètre ne dépend pas de la pression.
Si en plus, on a contraction, le diamètre diminue encore, ce qui fait encore diminuer le débit.
Tension et rayon : que ce passe-t-il lorsque l’on envoie dans un vaisseau, du sang sous pression croissante ?
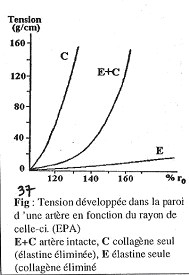
La compliance des vaisseaux fait que le volume augmente grâce à un étirement de la paroi qui subit certaines tensions.
Dans ce cas, la tension est fonction du rayon du vaisseau. La relation les unissant n’est toutefois pas linéaire. La courbe de résultats obtenus est relativement plate au début puis devient de plus en plus raide : on début, quand on tire sur la paroi la tension est faible, mais, plus on tire, plus la tension s’accroît. (Courbe E+C)
Si jamais on enlève le collagène du vaisseau, on obtient la courbe E : très peu de tension se développe.
Si l’on enlève l’élastine et que l’on garde uniquement le collagène, on obtient la courbe C montrant que le moindre étirement provoque une augmentation très importante de la tension.
En pratique, quand on a C+E (collagène et élastine), les éléments se mettent en jeu par l’action de l’élastine. Le collagène n’est pas étirable par lui-même : les mailles sont peu déformables sans tension. Il sert à protéger la paroi si la tension devient importante trop vite.
On peut faire une analogie entre le ballon de baudruche et le filet formé par le collagène et l’élastine :
- l’élastine développe peu de tension mais ne donne pas de rigidité au système ;
- le ballon est gonflé jusqu’à arriver à une position où il ne se déforme plus ; comme le filet.
L’action du tonus vasomoteur sur la tension.
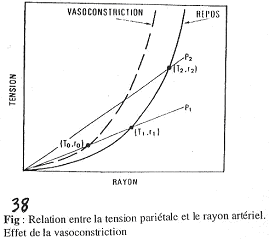
Quand les vaisseaux se contractent, on reste sur la droite de P2 ; on passe à un rayon plus faible mais la tension diminue : cela préserve des déchirures lors des grandes pressions.
 La vasoconstriction décale la courbe vers la gauche.
La vasoconstriction décale la courbe vers la gauche.
Il faut faire attention car, à rayon égal, la vasoconstriction augmente la tension !
(Les deux droites ont des pressions identiques).
Notion de contraintes pariétales (subit par la paroi).
Il y a des déchirements car les vaisseaux ne peuvent pas supporter de trop grandes pressions. L’épaisseur de la paroi est importante pour prévenir ces cassures : ce qui compte est le rapport entre T (que rapporte le vaisseau) et h (l’épaisseur) (T/h).
La tension est égale au rapport de la pression sur le rayon (T=P/r). Ce qui compte est la pression puis le rapport du rayon sur l’épaisseur de la paroi (r/h).
Lors d’une vasoconstriction, le rayon (r) va diminuer et comme l’on a la même quantité de matériaux, on va avoir l’épaisseur (h), qui augmente et fait ainsi diminuer la tension exercée sur la paroi : c’est un système de protection.
D La circulation artérielle.
Dans cette circulation, on distingue deux domaines : les artères élastiques (aortes et grosses artères) et les artères musculaires.
1 Les artères musculaire.
Ces artères sont riches en fibres élastiques et pauvres en cellules musculaires. Leur rôle est de régulariser le débit car le cœur est une pompe discontinue et les organes ont besoin d’un flux continu.
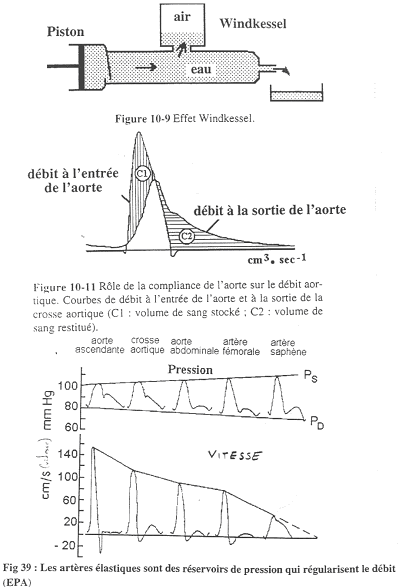
On suit le trajet des artères.
A la sortie du cœur, la vitesse atteint un maximum élevé mais ensuite, elle s’annule et arrive même à s’inverser. Dans les artères saphènes, le débit ne s’annule plus mais n’est pas régulier (toujours pas régulier). Si les artères étaient rigides, on n’aurait un écoulent sanguin uniquement pendant la systole.
Sur la figure du haut (10-9), quand on pousse le piston, tout ne sort pas en même temps : il y a un stockage par compression de l’air. Quand le piston recule, il y a écoulement car l’air comprimé pousse le liquide. Il faut bien faire attention au fait qu’il n’y ait pas d’air dans l’aorte ! Le rôle de l’air est joué par l’élasticité de la paroi de l’aorte.
Sur la figure 10-11, on voit que les débits ne sont pas superposés : la moitié du sang est stockée alors que l’autre moitié s’écoule.
Sur la figure du as, on observe l’enregistrement de la pression dans les artères élastiques.
 Plus on s’éloigne du cœur, plus la pression systolique augmente, alors que la pression diastolique diminue. Finalement, on a alors la pression artérielle moyenne qui diminue très lentement (très peu).
Plus on s’éloigne du cœur, plus la pression systolique augmente, alors que la pression diastolique diminue. Finalement, on a alors la pression artérielle moyenne qui diminue très lentement (très peu).
La pression systolique augmente par une sorte d’artefact.
Quand le cœur met le sang sous pression, l’onde de pression se déplace plus vite que le sang. Cette onde de pression va être réfléchie et il va y avoir des croisements qui vont donner des interférences représentées soit par des soustractions, soit par des additions d’ondes.
L’aire sous la courbe de chaque période est inférieure ou égale à la précédente.
2 Les artères musculaires.
(Vrai aussi pour les artérioles).
Ces artères sont douées de vasomotricité. Elles sont aussi appelées « artères de distribution ». La vasomotricité intervient pour la régulation de la pression artérielle.
Pa=Dc*RPT
RPT dépend du diamètre des vaisseaux.
Le contrôle des muscles lisses vasculaires dépend du système nerveux orthosympathique. Parfois on a des terminaisons nerveuses cholinergiques, mais seulement pour quelques rares organes. Le système nerveux orthosympathique entraîne la vasoconstriction.
Cette vasoconstriction sert aussi à la thermorégulation.
Pendant une réaction inflammatoire, il va y avoir vasodilatation.
a Vasodilatation débit-dépendante.
(Vasodilatation induite par le flux sanguin).
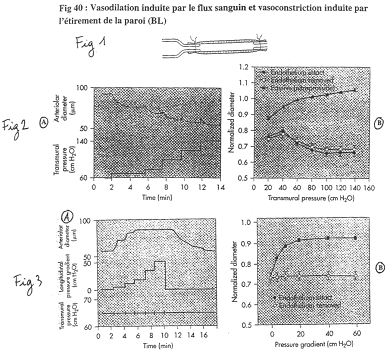
On prend une artère où le débit sanguin augmente graduellement (par palier).
Sur la figure 3, on fait varier le débit sans modifier la pression transmurale.
Pour le diamètre de l’artère : quand il y a augmentation de circulation, on observe une vasodilatation. Sans endothélium, la vasodilatation débit-dépendante est supprimée : on a donc besoin de la totalité de l’endothélium (besoin de son intégrité).
L’endothélium sécrète du NO qui est vasodilatateur
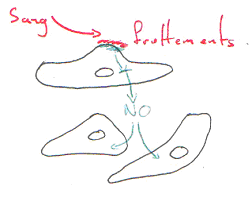
Si l’on remplace le sang par un liquide de plus en plus visqueux, on va faire augmenter la vasodilatation. Si l’on rigidifie les cellules endothéliales, on observe qu’il n’y a plus de vasodilatation débit-dépendante.
 C’est le « Stear Stress ».
C’est le « Stear Stress ».
 C’est la déformation de la cellule qui est perçue et qui déclenche la libération de NO.
C’est la déformation de la cellule qui est perçue et qui déclenche la libération de NO.
Si les vaisseaux ont un débit qui augmente, la vitesse va augmenter, comme les frottements. à Le diamètre augmente, ce qui fait diminuer la vitesse.  C’est une boucle de régulation (c’est le rôle fondamental de l’endothélium).
C’est une boucle de régulation (c’est le rôle fondamental de l’endothélium).
b La vasoconstriction myogénique.
Revoir la figure 40.
Dans cette expérience, le sang ne circule pas, le débit est donc de 0.
On augmente la pression transmurale par paliers. A chaque palier, les artères vont avoir une petite dilatation, puis une réduction du diamètre. Plus l’artère reçoit de pression, plus le diamètre diminue. Si l’on empêche le muscle de se contracter, le diamètre augmente.
Sans endothélium, on observe les mêmes phénomènes.
Quand on étire les cellules musculaires lisses, il y a contraction. Dans la paroi, on a des canaux sensibles à l’étirement : ils permettent l’entrée de calcium, dépolarisation et contraction.
Le principal intérêt et le tonus vasomoteur : contraction un peu permanente. Ce tonus permet d’augmenter l’épaisseur et le diamètre et ce qui diminue les contraintes.
 Ce tonus protège du déchirement.
Ce tonus protège du déchirement.
Le passage de la position couchée à debout.
Une trop forte pression dans les capillaires entraîne la formation des œdème. Il y a une limite entre vasodilatation et vasoconstriction réflexe en aval.
E Vasodilatation métabolique.
L’irrigation d’un tissu s’adapte aux besoins de ce tissu. Le phénomène est assez général mais difficile à étudier saut sur les muscles.
1 L’hyperhémie réactionnelle.
On provoque une occlusion et l’on mesure le flux sanguin dans le vaisseau.
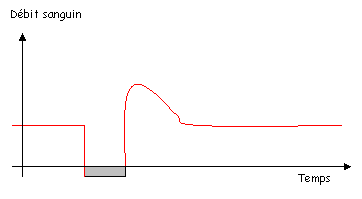
Ce mécanisme est peu connu.
Pendant l’occlusion, on aura une hypoxie et une hypercapnie (trop de CO2), le pH chute. Ce sont tous des stimuli vasodilatateurs, avec des mécanismes d’action différents.
2 L’hyperhémie fonctionnelle.
Cette hyperhémie est mise en évidence facilement dans un muscle.
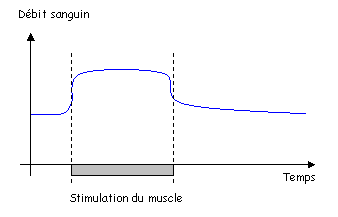
Très rapidement, la vasodilatation se produit mais trop vite pour les facteurs cités précédemment. On ne sait pas très bien ce qu’il se passe.
Ce mécanisme a été étudié là où le muscle et l’artère sont collés.
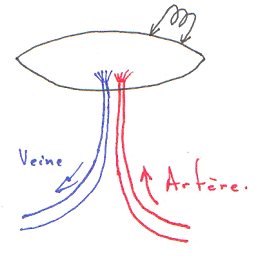
Souvent, on voit que les artères et les veines sont collées.
Si l’on détruit l’endothélium de la veine, on aura une hyperhémie bien moindre.
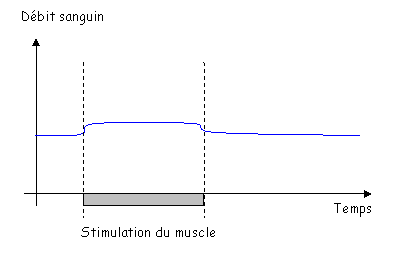
L’endothélium de la veine peut produire du NO et le faire diffuser dans l’artère. L’endothélium est un « capteur ». è L’endothélium de la veine, par son endothélium, produit du NO qui va agir sur l’artère associée.
Ce phénomène n’existe pas dans tous les cas.
On trouve aussi une régulation métabolique à la place de mécanisme dans les petits vaisseaux, voir même dans des organes.
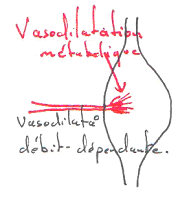
L’intérêt de ce mécanisme est d’éviter le collapsus artériel. Cela regroupe plusieurs nécessités.
Si l’on augmente la pression en amont, on va augmenter le débit.
Selon les organes et la situation, on a soit une vasoconstriction soit une vasodilatation.
F Le muscle lisse vasculaire.
Le muscle lisse vasculaire présente des différences avec les muscles striés :
- Il n’y a pas de sarcomères.
- Il y a présence d’actine et de myosine, mais sans organisation géométrique : les filaments sont dispersés. Cette position présente un avantage : la fibre musculaire lisse est moins dépendante de sa longueur que la fibre musculaire striée.
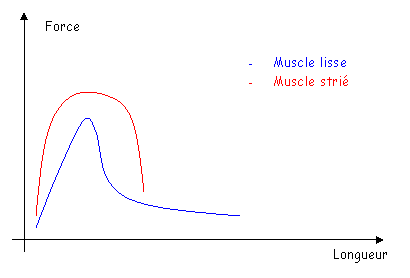
Comme dans le muscle cardiaque, les cellules sont reliées entre elles par des jonctions GAP : elles se stimulent les unes les autres (il n’y a pas de plaque motrice dans le muscle lisse). Les terminaisons du système nerveux orthosympathique forment des varicosités (des vésicules) et ne stimulent que quelques cellules qui vont stimuler leurs voisines…
La force développée par le muscle lisse peut être aussi forte que celle développée par le muscle strié mais cette contraction sera beaucoup plus lente.
Le muscle strié est relâché ou contracté. Le muscle lisse a des états intermédiaires : des états verrouillés. Dans ces états verrouillés, le muscle se maintien dans l’état intermédiaire choisi sans consommer d’énergie.
Le muscle strié et le muscle cardiaque se contractent toujours grâce à un potentiel d'action : le muscle lisse non ! Il peut se contracter grâce à un potentiel d'action ou non.
Dans les muscles lisses, le Ca2+ joue un rôle dans la contraction. Dans ce cas, l’intervention du calcium se fait grâce à un couplage avec la calmoduline.
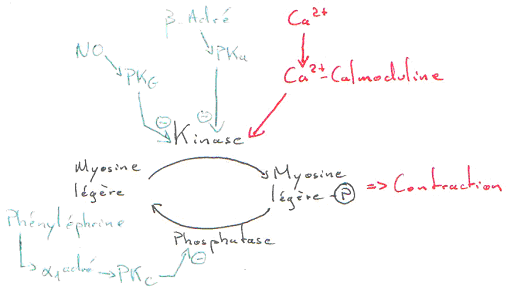
La concentration en calcium est modulable par un ensemble d’enzymes qui interviennent à divers niveaux.
Le NO (vasodilatateur) permet l’accumulation de GMPc (qui active la PKg). Cette PKg phosphoryle la kinase et l’inhibe.
La phényléphrine est un agoniste des récepteurs a1-adrénergiques : ils sont couplés à la PLC et donnent de l’IP3 et du DAG. Ce DAG va activer la PKc. La contraction est favorisée.
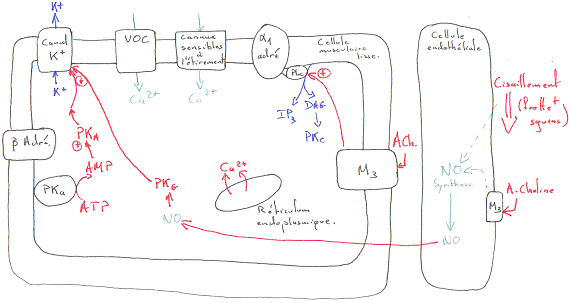
Remarque : il y a le problème de l’existence de M3 car l’acétylcholine n’est pas une hormone ; c’est un neuromédiateur, mais cela fonctionne…
L’acétylcholine, sur l’endothélium va entraîner une vasodilatation alors que sur les cellules musculaires lisses, elle entraîne une vasoconstriction.
Les vaisseaux sanguins sont innervés par le système nerveux orthosympathique alors que l’acétylcholine est libérée par le système nerveux parasympathique.
La noradrénaline a une action différente selon le récepteur sur lequel elle se fixe : elle donne une vasoconstriction en se fixant sur le récepteur a1 et une vasodilatation en se fixant sur le récepteur b.
 Dans la plupart des artères, l’activité a1 est prédominante, mais ce n’est pas le cas partout (surtout dans les artères des muscles striés). è Les artérioles ont principalement des récepteurs a alors que les artères des muscles striés ont plutôt des récepteurs b.
Dans la plupart des artères, l’activité a1 est prédominante, mais ce n’est pas le cas partout (surtout dans les artères des muscles striés). è Les artérioles ont principalement des récepteurs a alors que les artères des muscles striés ont plutôt des récepteurs b.
G La microcirculation (ou circulation capillaire).
1 Organisation d’un réseau capillaire.
Beaucoup d’études ont été faites en 2 dimensions alors que la majorité des réseaux est en trois dimensions.
Les artérioles donnent des métartérioles et des boucles capillaires sont branchées sur ces métartérioles. A la base de chaque départ, on trouve un sphincter pré capillaire.
On a aussi des anastomoses veineuses qui permettent de détourner le sang. La vitesse dans les capillaires est lente, 1000 fois plus lente que dans l’aorte. Les échanges sont surtout des échanges nutritifs.
2 Structure des capillaires.
En a, on voit des capillaires continus, comme dans les muscles. L’O2 et le CO2 diffusent. On a des fentes minces pour quelques échanges. Il existe aussi le transport transendothélial (pinocytose).
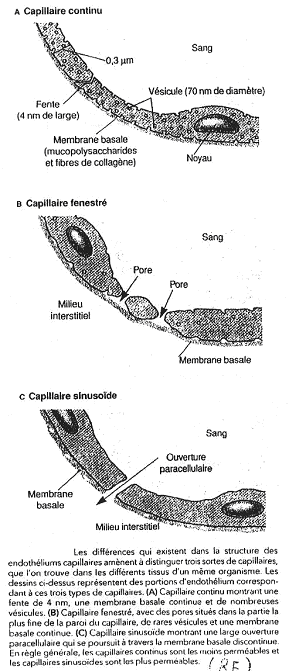
Sur la figure b, on a le cas des capillaires fenestrés des reins. Il existe un fort débit dans les trous ainsi qu’une sélectivité de la lame basale.
La figure c représente des sinusoïdes, trouvés dans le foie et dans les os. Il y a une erreur sur ce document : il n’y a pas de lame basale dans les sinusoïdes.
Les capillaires font une filtration permanente des liquides, ce qui est la conséquence de la nutrition. Le liquide va sortir du capillaire (par les protéines) et avec ce liquide, sort tout ce qui peut passer au travers de la paroi.
La plupart du temps, c’est du plasma sans protéines qui sort.
La pression oncotique du plasma (ou pression plasmatique des protéines) s’oppose à la filtration.
Au début, la pression sanguine est supérieure à) la pression oncotique mais au fur et à mesure, la pression sanguine devient inférieure à la pression oncotique, ce qui entraîne la réabsorption.
La filtration dans les capillaires représente un volume de 20 litres par jour. La réabsorption représente, elle, 18 litres par jour. On a finalement une différence de 2 litres par jour.
Ces deux litres restant sont drainés par les capillaires lymphatiques et donnent la lymphe.
 C’est la conséquence de la pression élevée et de la perméabilité du capillaire.
C’est la conséquence de la pression élevée et de la perméabilité du capillaire.
H La circulation veineuse.
Les veines ont une compliance élevée aux basses pressions.
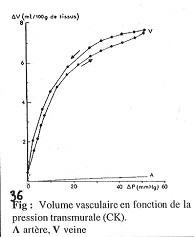 .
.
Cette compliance entraîne le remplissage. Quand elles se vident, les veines s’aplatissent : le volume du compartiment veineux est donc variable.
Les veines ont une possibilité de veino-constriction, qui compte beaucoup pour le retour veineux. Elles ont aussi de nombreuses valvules anti-reflux.
Le retour veineux au cœur dépend de la différence de pression entre les veines et l’oreillette. Le problème existant est qu’il y a très peu d’énergie participant au retour veineux. L’énergie vient de la contraction du cœur qui fait un appel de sang. Une autre source d’énergie est la constriction des veines (structures qui aident au retour) ; les muscles striés squelettiques et les mouvements respiratoires aident fortement à faire remonter le sang au cœur.
Les veines sont des structures où règnent de basses pressions : les contractions font écraser les veines. L’augmentation de pression obtenue par l’écrasement, en arrière de la veine entraîne la fermeture de la valvule et en avant, il y a ouverture de la valvule.
Les mouvements respiratoires aident à la remontée du sang (l’inspiration).
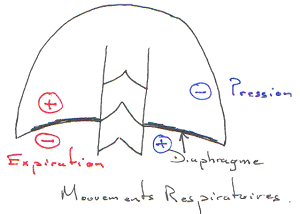
IV Physiologie cardio-vasculaire intégrée.
A Le couplage cœur/vaisseaux.
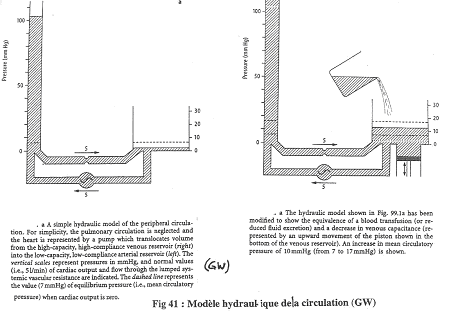
On considère que l’appareil cardio-vasculaire est représenté par le montage.
Si le cœur s’arrête, on obtient la même pression dans les artères que dans les veines. Le niveau atteint est la pression de remplissage : cette pression ne dépend que du volume sanguin (de la volémie). Chez l’Homme, cette pression de remplissage est de l’ordre de 7 millimètres de mercure (7mm Hg).
Si le débit de la pompe augmente, la pression dans le compartiment artériel augmente mais diminue dans le compartiment veineux : on atteint la débit cardiaque maximal où le sang dans le compartiment veineux est absent.
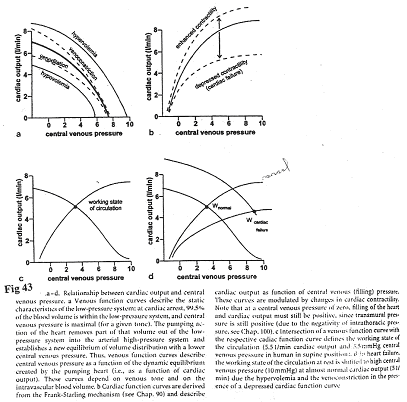
En a, on observe les effets du débit cardiaque sur la pression veineuse.
Sur le document 41, à droite, on a un compartiment veineux à capacité variable. La veino-constriction est représentée par une montée du piston et la veino-dilatation est mimée par l’abaissement du piston.
- La veino-constriction entraîne une montée du niveau de liquide qui fait augmenter la pression veineuse qui elle –même accroît le débit cardiaque.
- Dans le cas des transfusions, la pression moyenne de remplissage augmente, ce qui fait augmenter le débit cardiaque.
Plus la pression veineuse augmente, plus le volume télé-diastolique augmente et donc, le débit cardiaque augmente.
Sur le document 43, en c, le point d’intersections des deux courbes montre un état d’équilibre de la circulation.
Sur ce même document, en d, si la contractilité ventriculaire diminue, on aura un débit faible mais avec une pression veineuse élevée.
Si l’on a contraction veineuse et hypervolémie, cela permet de remonter le débit cardiaque.
Ce phénomène est typique des personnes ayant une insuffisance cardiaque.
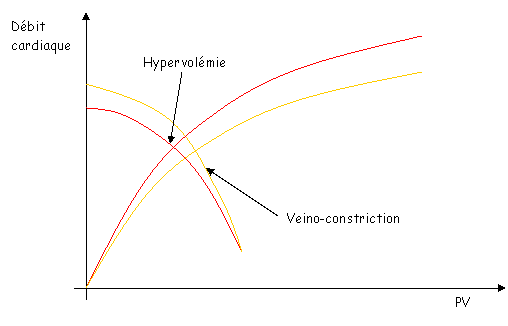
Ces courbes permettent de comprendre les fonctions cardiaque et veineuse.
La volémie est essentielle pour le contrôle de la fonction cardiaque. On a des volorécepteurs auriculaires (oreillette droite) qui contrôle la sécrétion d’ADH.
L’oreillette, quand il y a surpression, synthèse de l’ANP qui, sur le rein, fera excrété du sodium et donc de l’eau.
B Régulation de la pression artérielle moyenne.
On trouve une boucle de régulation de cette pression. On a des capteurs de pression (barorécepteurs artériels dans l’aorte ou les carotides). Les informations fournies par ces récepteurs sont traitées par le système nerveux central.
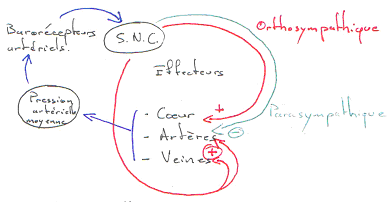
Dc = Fc * Ves.
Ves est fonction de la contractilité ventriculaire (par le système nerveux orthosympathique) mais aussi du retour veineux, lui même fonction de la volémie, des pompes accessoires et de la vasoconstriction.
· Les barorécepteurs.
Ces récepteurs sont des fibres nerveuses, sensibles à l’étirement.
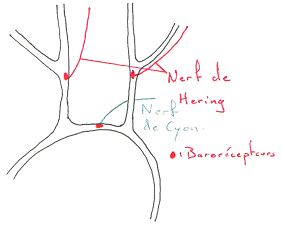
Si la pression est constante, on aura une moins bonne réponse que si l’on a une pression pulsatile. La décharge carotidienne a une phase ascendante où les potentiels d'action augmentent. Elle montre aussi les variations de pression.
Ces nerfs convergent vers le bulbe (noyau trichus solitaire).
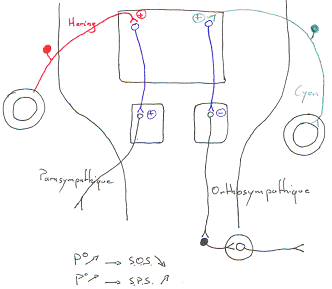
Quand la pression augmente, l’activité du système nerveux orthosympathique diminue alors qu’avec cette même augmentation de pression, l’activité du système nerveux parasympathique s’accroît.
 C’est le baroréflexe.
C’est le baroréflexe.
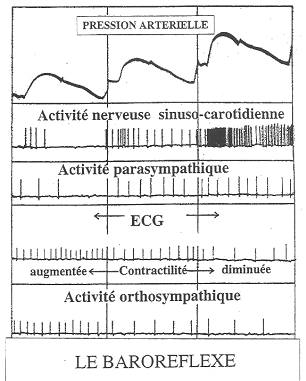
Ce baroréflexe fonctionne tout le temps, d’un battement de cœur à l’autre.
Un autre système dans le rein complète cet effet : c’est le système rénine-angiotensine-aldostérone. à C’est une régulation hormonale de la pression artérielle.
Les cellules sécrétant la rénine sont dans l’artériole afférente. Les cellules du tube contourné distal forment la macula densa qui communique avec les cellules à rénine.
Si la pression diminue dans l’artériole afférente, il va y avoir sécrétion de rénine. Cette dernière, dans le sang, hydrolyse l’angiotensine (produite par le foie) en angiotensine 1. Ce produit est transformé en angiotensine 2 par l’action d’enzyme de conversion.
Les effets de l’angiotensine 2 sont une augmentation de la vasoconstriction (qui fait augmenter la pression), une activation du cortex surrénalien qui va produire de l’aldostérone et une sensation de soif. L’aldostérone va entraîner une augmentation de la réabsorption de sodium (et de l’eau qui lui est associée).
Les cellules à rénine mesure la pression par leur propre étirement. Ces cellules sont innervées par le système nerveux orthosympathique et quand elles sont stimulées, elles vont sécréter de la rénine. La diminution de la concentration en sodium du tube contourné distal entraîne, par les cellules de la macula densa, une stimulation des cellules à rénine.
C La posture.
Quand le sujet est couché, il n’y a pas de différence de hauteur entre la tête, le cœur et les pieds La pression artérielle moyenne dans l’aorte est de 100mm Hg. Elle est de 95mm Hg dans les pieds et la tête.
La pression veineuse est de 2mm Hg dans le cœur, de 5mm Hg dans les pieds et la tête.
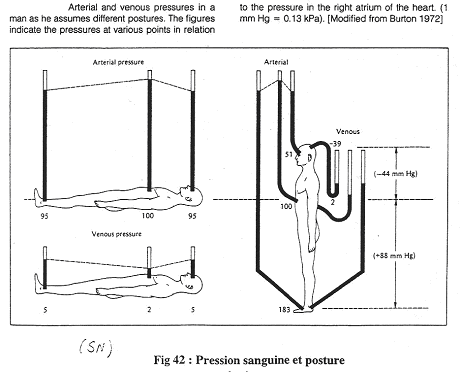
Au levé, au niveau du cœur, rien ne change.
En dessous du cœur, dans les pieds, la pression est de 95mm Hg + la pression hydrostatique (88mm Hg), soit 183mm Hg.
Au dessus du cœur, dans le crâne, on a une pression de 54mm Hg, soit 95mm Hg – 44mm Hg.
Une des conséquences est qu’au niveau des pieds, la pression augmente fortement et brutalement.
Les capillaires.
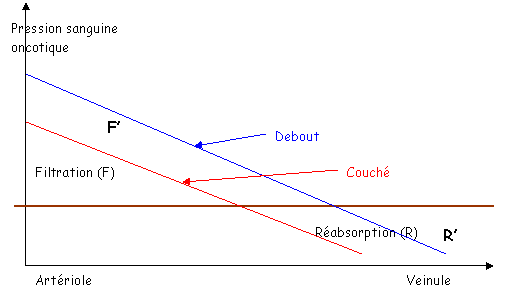
L’augmentation de la pression due au levé va entraîner l’accumulation d’eau, ce qui peut provoquer des oedèmes.
Il existe toutefois des phénomènes qui luttent contre cet effet de la pesanteur :
- La vasoconstriction myogénique. Moins de sang arrive dans les capillaires.
- Il y a constriction veineuse de temps en temps sur le retour, ce qui fait diminuer la pression mais aussi augmenter le retour veineux.
On peut citer le problème capillaire, mais le principal problème est le retour veineux.
Les vaisseaux sanguins forment un réseau continu où le liquide qui descend attire celui qui monte.
D Exercices physiques.
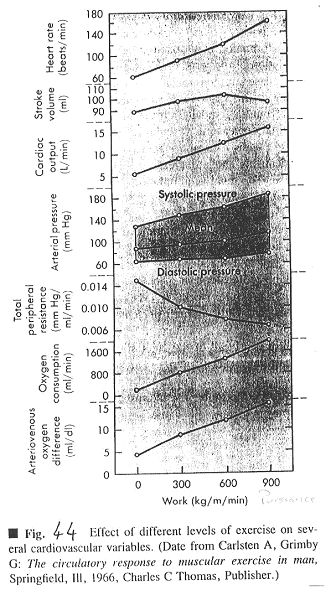
Ce document est un rassemblement de mesures de différents facteurs.
On voit que Fc monte régulièrement. Ves, à puissance élevée donne soit un plateau, soit une petite baisse.
Ves augmente car il y a augmentation du retour veineux, de la ventilation pulmonaire et stimulation du système nerveux orthosympathique.
Le débit cardiaque (Dc) augmente, ce qui est normal, car Dc=Fc*Ves.
La pression artérielle augmente à peine, c’est donc la résistance périphérique qui diminue. Cette diminution de résistance périphérique est due à la vasodilatation des artérioles des muscles. En premier, la vasodilatation est due au métabolisme. Ensuite, elle est due aux fibres musculaires lisses artérielles qui ont des récepteurs b (et donc vasodilatateurs) alors que les autres artères ont des récepteurs a1 (qui donneraient une contraction).
Le débit cardiaque est multiplié par 5 et toute l’augmentation est dirigée vers les muscles (dont le cœur) : on a donc une très importante vasodilatation des vaisseaux musculaires.
La pression diastolique est à peu près constante mais la pression systolique, elle, augmente. Ceci est expliqué par le Ves qui augmente (au début) et par la diminution de la durée de la phase d’éjection ventriculaire.
Chapitre 2 :
La Fonction Digestive.
La fonction digestive fait parti d’un ensemble de quatre fonctions de nutrition : respiration, digestion, excrétion et circulation.
D’autres fonctions sont par exemple : la locomotion, la marche, le travail, la stature, la posture, l’aguets, l’affût, etc…
I Introduction, généralités.
A Présentation de la fonction digestive.
Le tube digestif peut être séparé en différents segments (parties) :
- partie sus diaphragme : de la bouche à l’œsophage ;
- partie sous diaphragme : estomac, intestin grêle, gros intestin (ou colon), mais aussi pancréas et foie.
Les aspects de la digestion sont vastes :
- les besoins (adultes, au repos, …)
- la prise alimentaire
- digestion des aliments
- absorption des nutriments
- métabolisme (devenir des nutriments dans l’organisme).
B Quelques rappels.
On distingue classiquement :
1_ Le besoin d’énergie ou de calories, et sont concernés les glucides et les lipides (composés ternaires C-O-H). Ils servent à l’oxydation cellulaire. Ils vont aussi permettre les contractions musculaires, la régulation thermique, le transport actif, la réduction de synthèse ou l’anabolisme.
2_ Le besoin de matière ou besoin plastique : glucides, lipides, protides (pour l’azote). Ces produits servent à « l’entretien », au renouvellement cellulaire, à l’énergie et à la synthèse de nombreuses hormones, à la croissance, à la gestation, à la lactation, aux exercices.
L’énergie chimique des nutriments est convertie en ATP avec un rendement d’environ 25%.

Les valeurs à connaître :
· Calorie (cal) : quantité de chaleur nécessaire pour élever la température d’un gramme d’eau de 14,5°C à 15,5°C. En nutrition, on parle de Kcal. Kcal = Cal.
· Joule (J) : unité d’énergie mécanique. 1Cal = 4,184 J (ou 4,18J) ó 1J = 0,239 Cal
C Mesure des dépenses énergétiques.
1 La calorimétrie directe.
La calorimétrie mesure l’énergie thermique perdue par un sujet placé dans une enceinte close, isolée de l’extérieure.
2 La calorimétrie indirecte ou thermochimie.
La thermochimie évalue l’énergie chimique des nutriments ou l’énergie théoriquement libérable par l’oxydation de substrats alimentaires en présence d’oxygène.
a La thermochimie alimentaire.
On utilise une bombe calorimétrique et on détermine ainsi la chaleur de combustion métabolique. Il faut tout de même corriger les valeurs obtenues ; par exemple, pour une protéine qui ne s’est pas complètement oxydée, il reste de l’urée qui renferme une énergie potentielle.
Il faut également tenir compte du rendement du tube digestif, mesuré par le coefficient d’utilisation digestive (CUD).
|
Constituants
|
CUD (en %)
|
Vol. Calorique (en KJ)
|
Kcal/gramme
|
|
Glucides
|
99
|
17
|
4
|
|
Lipides
|
95
|
38
|
9
|
|
Protides
|
85
|
17
|
4
|
|
Ethanol
|
99
|
30
|
7
|
b Thermochimie respiratoire.
Principe : L’organisme tire son énergie de l’oxydation des nutriments et la quantité d’énergie libérée dépend donc du volume d’O2 utilisé.
Les méthodes de thermochimie respiratoire mesure la dépense énergétique d’un sujet à partir de sa consommation d’O2.
c Coefficient thermique de l’O2 : Kx.
Le coefficient thermique de l’O2 est la quantité d’énergie libérée par litre d’O2 consommé à partir de l’équation suivante : métabolites + O2 à CO2 + H2O + Energie.
Energie = Kx * VO2
Kx varie selon les nutriments et l’on choisit un Kx moyen qui environ 5 Kcal/Litre d’O2 (soit 20KJ/L d’O2).
Comme le coefficient thermique de l’O2 dépend du substrat transformé, il faut préciser la nature de celui-ci grâce au quotient respiratoire.
d Coefficient respiratoire (QR).
QR = VCO2(expiré)/VO2(consommé) unité : Litre par unité de temps.
On détermine ce QR à partir d’une équation générale de l’oxydation des nutriments : QRglucides = 1 ; QGprotéines = 0.83 ; QRLipides = 0.70.
3 Evaluation du besoin énergétique.
a Définition du besoin énergétique.
« Besoins énergétiques d’un individu correspondant à la valeur de l’apport énergétique alimentaire qui équilibre la dépense d’énergie chez un sujet dont la corpulence, la composition de la masse corporelle et le degré d’activité physique sont compatibles avec le maintien durable d’une bonne santé et permettent l’exercice de l’activité physique nécessaire. » (OMS, 1986).
« Chez l’enfant et la femme enceinte ou allaitante, les besoins énergétiques inclus les besoins associés à la croissance tissulaire ou à la sécrétion lactée à un rythme comparable avec une bonne santé ».
Les apports énergétiques alimentaires correspondant à une moyenne des apports « habituels » assurés durant une durée déterminée, modérée et non aux apports effectifs d’une journée.
D’une façon conventionnelle, les apports sont exprimés sous forme d’apports journaliers.
A partir des besoins énergétiques d’une personne (homme de 60 à 70kg ou femme de 50 à 60kg) de référence, on procède à des corrections en prenant en compte, la taille, le poids, certaines modifications physiologiques (grossesse, allaitement, vieillissement) et les facteurs environnementaux (comme l’activité physique et le climat) pour déterminer les besoins de chaque sujet.
b Détermination du poids idéal en fonction de la taille.
Pour trouver le poids correspondant à la taille, il existe différentes formules.
· Indice de la masse corporelle (IMC) ou Indice de Quételet ou BMI en anglais (pour l’OMS).
IMC = P (en kg)/T² (taille en cm)
Ce rapport est de 22 pour un homme et de 20,8 pour une femme.
Pour un homme de 1m70, le poids idéal est de 63,6kg.
Pour une femme de 1m60, le poids idéal est de 51,7kg.
Un indice de 30 pour un homme et de 28,6 pour une femme sont des révélateurs d’obésité.
· La formule de Lorens, pour l’homme.
P = T-100 – [(T-150)/4] ; T est en centimètre et P en kg.
Pour 1m70, le poids idéal est de 65kg.
· La formule de Lorens pour la femme.
P = T – 100 – [(T-150]/2,5] ; T est en centimètre et P en kg.
Pour 1m60, le poids idéal est de 56kg
La formule de Lorens permet un intervalle de +/- 10% mais si cet intervalle atteint 20%, on se trouve dans un cas d’anormalité.
Ces estimations de poids se font en tenant compte du squelette.
c Composantes du besoin énergétique.
Le besoin énergétique est la résultante d’un ensemble de dépenses :
- liées au métabolisme de base (pour les femmes enceintes et allaitantes, les besoins de production sont inclus dans ce métabolisme ; même chose pour la croissance d’un enfant) ;
- liées au travail digestif et à l’utilisation des nutriments par l’organisme ;
- liées à la thermorégulation ;
- liées au travail musculaire.
α Le métabolisme de base.
Ce métabolisme est dépense énergétique mesurée dans des conditions standards et qui exprime les dépenses nécessaires de la vie d’un sujet au repos, à la neutralité thermique (entre 20° et 25°C), mesurée par thermochimie respiratoire (repos, couché, au calme, à jeun depuis 14h et à sa neutralité thermique).
On réalise la mesure toujours à la même heure (environ 10h) pour éviter l’impact circadien sur la dépense énergétique de repos pendant les 24 heures.
Le métabolisme de base est proche du métabolisme lors du sommeil (le pouls est plus faible pendant le sommeil). On observe :
- diminution du tonus musculaire,
- relâchement des muscles lisses,
- diminution des fonctions de l’organisme.
Ces méthodes sont utilisées pour déterminer le disfonctionnement de la thyroïde.
Pour des sujets de même âge, de même sexe, le poids corporel est le facteur essentiel du métabolisme de base.
Pour un homme adulte de 70kg, avec une activité légère, on trouve une valeur de 70kcal/h.
Pour une femme adulte de 55kg, avec une activité légère, on trouve une valeur de 55kcal/h.
Les facteurs de variation du métabolisme de base : le poids, la taille, le sexe, l’âge (il y a évolution de 5% par an de 3 à 10 ans ; diminution de 2% par décennie après 20 ans), l’état physiologie.
Le métabolisme de basse augmente de 20% en fin de grossesse. Celui-ci varie avec les conditions de l’environnement : la pratique régulière d’un exercice physique important provoque son accroissement. Une température élevée va faire diminuer ce métabolisme alors qu’une température basse le fait remonter.
Certaines « conditions de vie » provoquent des changements : le caféisme et le tabagisme accroissent le métabolisme de base.
Un homme d’un mètre 70 et de 65kg a un métabolisme de base de 110kJ/kg/jr (26,3kcal).
Une femme d’un mètre 60 et de 55kg a un métabolisme de base de 100kJ/kg/jr (23,9kcal).
β Dépenses liées au travail digestif.
Il y a augmentation du métabolisme de base. La méthode de détermination consiste chez des sujets vivants, placés dans les conditions standard de mesure du métabolisme de base et recevant un repas de composition définie, on mesure la dépense supplémentaire au métabolisme de base et on la compare à l’énergie ingérée.
La dépense d’énergie liée à la prise alimentaire se décompose en deux facteurs :
- les dépenses liées au travail du tube digestif (commune à tous les nutriments) qui constituent une faible d’accroissement de la dépense (3% de l’apport énergétique ingéré).
- Les dépenses spécifiques liées à l’utilisation cellulaire de chaque catégorie de nutriments, aussi appelé : Action Dynamique Spécifique des nutriments (ADS). ADS = 0 pour les glucides, 7% pour les lipides et entre 25 et 30% pour les protides.
L’ingestion de 100kJ (5,88g de protéine) entraîne l’apparition de 130kJ dans l’organisme et 107 kJ quand le nutriment est un lipidique.
L’ADS est aussi appelé « Extra Chaleur Post Prandiale », soit ECPP (perte de chaleur après la prise alimentaire).
Quand on crée un apport énergétique au niveau du métabolisme de base, l’accroissement de la dépense énergétique lors de la prise alimentaire est d’environ 10% du métabolisme de base. Chez un sujet dans des conditions standards, sans activité physique, à 25°C, pour maintenir l’équilibre de l’état physiologie, il faut des apports énergétiques supérieurs de 10% au métabolisme de base.
γ Dépenses liées à la thermorégulation.
Homéothermie : la température centrale du corps (80%) doit être maintenue dans des limites étroites malgré les variations de la température ambiante è nécessité » d’un système de régulation (pour le froid ou le chaud).
Il existe chez l’Homme une température dite « de neutralité thermique », ou « température de confort »qui correspond aux conditions de mesure du métabolisme de base (20 à 25°C). C’est la température qui chez un sujet n’entraîne aucune dépense énergétique engagée dans la lutte contre le chaud ou le froid.
Dans le maintien de l’homéothermie, on trouve un rôle essentiel du sang.
· Thermogenèse :
C’est la lutte contre le froid, une lutte sans protection.
Il va y avoir mise en place des frissons thermiques (contractions musculaires sans mouvement) qui dégagent de la chaleur et mettent en œuvre un métabolisme de sommet, 2 à 5 fois supérieur au métabolisme de base.
· Thermolyse :
Il y a mise en jeu du système vasculaire par vasodilatation ; il y a évacuation thermique par la peau et/ou par l’eau (visible ou non). Dans les conditions du métabolisme de base, la perte journalière d’eau est de 0,7 à 0,8 litre, en distinguant environ 2/3 perdus par les poumons et 1/32 par la peau.
Si la température augmente, il va y avoir des pertes d’eau visibles par le mécanisme de sudation. La sueur d’une journée peut représenter jusqu’à 10 litres.
La thermolyse est efficace car la perte de chaleur d’un gramme d’eau vaporisée, élimine 2,45kJ.
Si les conditions de chaud ou de froid sont trop fortes, l’organisme s’épuise rapidement.
On admet actuellement que l’Homme est moins armé pour lutter contre le chaud que contre le froid.
δ Dépenses liées au travail musculaire.
La contraction musculaire est essentielle. Le rendement de mécanique de celle-ci n’est que de 20% : 75% de l’énergie est dépensée sous forme de chaleur. Ces efforts musculaires sont relativement difficiles par de fortes températures car il y a augmentation de la quantité supplémentaire de chaleur à éliminer.
Les dépenses liées au travail musculaire sont d’origines diverses : professionnelles, ludiques, sociales.
|
Activités
|
Homme
|
Femme
|
|
Sommeil
|
1
|
1
|
|
Position couchée et assise au calme
|
1,2
|
1,2
|
|
Debout
|
1,4
|
1,4
|
|
Promenade lente
|
2,5
|
2,5
|
|
Marche soutenue
|
3,2
|
3,2
|
|
Position assise
|
1,3 à 1,5
|
1,3 à 1,5
|
Le poids du sujet est un facteur essentiel de la dépense énergétique liée à l’activité physique.
ε Les bésoins énergétiques.
1 Chez l’adulte.
Chez l’homme adulte moyen, les besoins énergétiques sont d’environ 2600kcal/jour, et chez la femme, ils sont de 2000kcal/jour.
Pour un homme, un travail physique pénible va faire monter les besoins énergétiques jusqu’à 3500kcal/jour.
Apports énergétiques conseillés par le CNERNA (1992)
Chez l’homme, activité physique réduite à 2100 kcal
Chez l’homme, activité physique moyenne à 2700kcal
Chez l’homme, activité physique forte à 3000 kcal
Chez la femme, activité physique réduite à 1800 kcal
Chez la femme, activité physique moyenne à 2000kcal
Chez la femme, activité physique forte à 2200 kcal
2 Evolution des besoins énergétiques lors du vieillissement.
Avec l’âge, ces besoins vont diminuer :
- Changement du poids corporel et de la composition de l’organisme (diminution de la masse musculaire et accroissement de la masse grasse).
- Diminution de l’activité physique : incidence des maladies ou des infirmités qui font régresser l’activité physique.
L’apport énergétique total doit subir une diminution en fonction de l’âge.
|
|
20 à 39ans
|
40 à 49 ans
|
50 à 59 ans
|
60 à 69 ans
|
70 à 79 ans
|
|
AET
|
100%
|
95
|
90
|
80
|
70
|
3 Au cours de la grossesse.
Au cours de la grossesse, le métabolisme de base s’élève. De façon moyenne, le gain de poids est d’environ 12,5kg et les besoins supplémentaires sont de l’ordre de 400kJ/jour durant le second trimestre et entre 900 et 1000kj/jour pendant le troisième trimestre, soit 633 en moyenne.
4 Au cours de l’allaitement.
Les apports énergétiques supplémentaires sont d’environ 2100kJ/jour.
5 Chez les enfants (croissance).
Chez les enfants en croissance, on va distinguer deux facteurs : la valeur énergétique des tissus formés et le coût énergétique des biosynthèses.
On trouve une augmentation de 23kJ/gramme pour le coût énergétique de la croissance d’un nourrisson. Chez le jeune enfant, cette valeur est de 21kJ/gramme.
6 Rations équilibrées.
L’arachide et les olives ont des acides gras saturés alors que le maïs, le tournesol ont des acides gras insaturés.
Pour les aliments, il faut regarder la qualité organoleptique.
II Glucides et digestion.
A Les sources.
Les glucides sont présents dans les aliments sous deux formes : les sucres de goût sucré (sucre simple comme le glucose, le fructose et le galactose ; ou sucre double comme le lactose, le saccharose et le maltose) et les sucres sans goût sucré (exemple : amidon).
Classiquement, les aliments sont divisés en 6 groupes :
1_groupe bleu : lait et dérivés.
2_groupe rouge : viandes, poissons, œufs (richesse en protéines).
3_groupe jaune : les corps gras
4_groupe marron : céréales et dérivés mais aussi les produits sucrés (les cuirités).
5_groupe vert : fruits et légumes.
6_groupe violet : les boissons.
1 Groupe 1, lait et dérivés.
On trouve du lactose (glucose + galactose). Le taux est faible mais existe. L’aspect nutritionnel est intéressant car le lactose facilite l’absorption de Calcium, l’implantation de la flore lactique dans le tube digestif.
Les bactéries lactiques servent à la fabrication des produits laitiers.
Il existe parfois une intolérance au lactose s’il y a déficience en lactase intestinale.
2 Groupe 2, viandes, poissons et œufs.
Les viandes rouges comptent 0,5% de glycogène (en poids frais ou parties comestibles).
Les huîtres contiennent 6% de glucides qui évoluent en glycogène au moment de la reproduction. Les moules contiennent 2% de glucides.
3 Groupe 3, corps gras.
Le beurre contient 0,6% de glucides et la crème 4%.
4 Groupe 4, céréales et dérivés – produits sucrés.
Le blé (en grains) montre 68% de glucides, avec 2% de sucres simples ; 64% d’amidon et 2% de cellulose.
Le riz présente 70% de glucides avec essentiellement de l’amidon et 1% de sucres simples.
Le maïs contient également 70% de glucides avec 2% de cellulose.
Le sucre pur comme le sucre de canne, et la betterave à sucre contiennent 100% de glucides.
Le miel contient 70% de glucose + fructose et 6% de saccharose.
On trouve ensuite les produits de confiserie, le chocolat (poudre de cacao 40% de glucides, chocolat à croquer 64% de glucides), les confitures 60% et les glaces entre 20 et 25% de glucides.
5 Groupe 5, Plantes potagères (ou « légumes ») et Fruits.
Les plantes potagères (en lieu et place des « légumes ») comprennent :
- les « légumes » (en général 7% sauf la tomate 4%)
- les tubercules : pomme de terre 19% ; topinambour 17% ; manioc 37%
- les graines de légumineuses (vrais légumes) : haricots, lentilles, pois, fèves : 55 à 65% avec essentiellement de l’amidon
- les champignons : 4%
Les fruits :
- les fruits frais aqueux : 5 à 10%
- les oléagineux (olive, noix de coco, avocat) : environ 10%
- les graines d’oléagineux (noix, noisettes, amandes) : 17% dont 3% de cellulose
- les fruits amylacés (riches en amidon, comme les châtaignes) : 40%
- les fruits secs : 70%
- les fruits exotiques : bananes 20% ; ananas 12% ; dattes 73%
6 Groupe 6, les boissons.
Pour les boissons à base de fruits, on trouve 10 à 15% de glucides.
B Les besoins et apports en glucides.
Les sucres devraient représenter au moins 40% de l’AET (Apport Energétique Total).
L’amidon devrait couvrir 2/3 des besoins et les oses et diholosides 1/3.
Les besoins sont de 5 g/kg/jour.
C La digestion des glucides.
1 La bouche.
La salive, avec α-amylase (salivaire) (aussi appelée ptyaline) dont le pH optimum est de 6,5 est une enzyme activée par les ions Cl-.
L’action de cette enzyme est limitée à cause du court temps buccal. Elle devient inactive quand le pH passe en dessous de 4 (elle garde toutefois une certaine action dans l’estomac).
De nombreuses espèces animales n’ont pas d’amylase salivaire.
2 L’estomac.
En plus de la continuité de l’action relative de la ptyaline, il y a l’action chimique de l’HCl (acide chlorhydrique). Le suc gastrique pur a un pH de 1.
3 L’intestin grêle.
α Action prépondérante de l’α-amylase pancréatique.
L’action de cette enzyme est similaire à celle de l’α-amylase salivaire, avec des coupures de l’amidon et du glycogène. On obtient des éléments maltoses, maltotrioses, soit, des oligosaccharides ramifiés en 1-6 et non ramifiés plus un peu de glucose.
β Le suc intestinal.
Ce suc est sécrété par les glandes de Brunner et de Lieberkühn.
On trouve des oligosaccharidases et des disaccharidases spécifiques ; par exemple, la maltase qui agit à pH compris entre 5,4 et 6 et une lactase qui agit de 5,6 à 6. On peut aussi citer une saccharase dont le pH optimum est compris entre 5,8 et 6,2.
Ces hydrolases restent attachées à la bordure en brosse des entérocytes.
Il existe un complexe saccharase/Isomaltase qui hydrolyse le saccharose et la liaison α1à6 des dextrines. La saccharase a aussi le nom d’invertase car le saccharose est dit « sucre inverti » ou bien encore de sucrase (saccharose se dit sucrose en anglais).
D Absorption des glucides.
1 Le glucose.
L’absorption du glucose est complexe et a surtout lieu dans le jéjunum (la partie haute de l’intestin grêle). L’absorption se fait par un transport actif secondaire : cotransport (ou symport) avec Na+ au pole apical de l’entérocyte. La concentration en glucose de l’entérocyte est supérieure à celle de l’intestin grêle. Cette absorption nécessite donc de l’énergie. L’énergie utilisée est associée au gradient de sodium assuré par les pompes Na/K ‘sur les faces baso-latérales). è On obtient alors un gradient électrochimique de sodium entre la lumière intestinale et l’intérieur des entérocytes qui va dans le sens de l’entrée du sodium dans l’entérocyte.
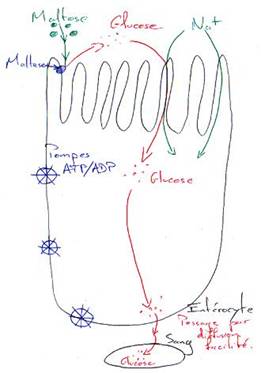
Il y a entrée du glucose et du sodium au pôle apical de l’entérocyte. Le glucose passe dans le sang au pôle basal par diffusion facilitée.
Le glucose est le nutriment glucidique principal (≈80%).
Le transport du glucose est actif, pour preuve, celui-ci est inhibé lorsque l’on ajoute de la ouabaïne (glucoside caryotonique qui inhibe les pompes à sodium).
2 Le galactose.
On trouve le même système que pour le glucose mais le galactose est présent en moindre quantité.
Toutefois, le galactose est un inhibiteur compétitif du transport de glucose dans l’intestin grêle.
3 Le fructose.
Le fructose est absorbé par diffusion facilitée selon un gradient de concentration via un système indépendant du Na.
L’absorption de ce composé est lente par rapport à celle du glucose ou celle du galactose.
L’hydrolyse des polysaccharides est rapide, en effet, on observe que les mécanismes d’absorption du glucose et du fructose sont rapidement saturés.
On trouve une exception à ceci, l’hydrolyse du lactose qui a une vitesse deux fois moindre à celle du saccharose.
E Annexes.
Les fibres alimentaires.
a Définition.
Les fibres sont des polymères végétaux qui présentent dans leurs parois de la cellulose et des pectines végétales.
Les fruits et légumes sont surtout riches en cellulose et pectine. Le son contient de la cellulose, de l’hémicellulose, de la lignine et de l’acide phytique.
|
Fibres végétales…
|
Biochimie
|
Distribution
|
|
Fibres glucidiques, fibreuses, cellulose
|
Eléments glucanes
|
Dans les parois des cellules végétales (indigestibles, rôle de ballast)
|
|
Fibres glucidiques, fibreuses, hémicellulose
|
Xylane, arabane, galactane
|
Dans le son et les légumineuses.
Propriétés : hygroscopiques + ballast
|
|
Fibres glucidiques, non fibreuses
|
Pectines (peau de pomme), gommes, mucilage, alginates
|
Peaux et pépins de fruits,
Algues
|
|
Fibres non glucidiques, Lignine
|
|
Dans les tiges et enveloppes de graines et des légumes secs
|
|
Fibres non glucidiques, Acide phytique
|
|
Dans le son
|
b Intérêt des fibres dans l’alimentation.
Les fibres ont un fort pouvoir de rétention d’eau et des substances hydrosolubles (glucides, minéraux, oligo-éléments) : elles jouent le rôle d’éponges. On peut trouver quelques fibres qui sont lipophiles.
Le son retient 8 fois son poids d’eau.
Les fibres de légumes et de fruits retiennent jusqu’à 10 fois leur poids d’eau, et les gommes arrivent jusqu’à 20 fois.
Cette capacité de rétention entraîne une augmentation du volume du bol alimentaire qui devient alors un lest ou un ballast, ce qui stimule alors la motricité (ou tonus) intestinale.
Remarque :
Les sucs intestinaux, la flore intestinale et les entérocytes desquamés forment les matières fécales minimales (liquides). Les fibres ont un rôle de tampon qui protège les muqueuses de l’action trop forte des sucs.
c Digestibilité des fibres.
On trouve un premier groupe de fibres indigestibles : lignine, mucilage, alginate. Des complexes vont ainsi se former (comme avec le son) et échapper ainsi à l’action enzymatique.
Le deuxième groupe de fibres est digestible. On y retrouve la cellulose, l’hémicellulose et les pectines ; ces dernières étant digérées à 90% par les enzymes bactériennes. Cellulose et hémicellulose sont digérées à 50% par les enzymes bactériennes.
Les produits de digestion des fibres sont des acides gras à courtes chaînes (C1, C2, C3, C4) qui seront absorbés ou éliminés voir même réutilisés par la flore. Il peut également y avoir production de gaz tels que le méthane, l’H2, le CO2 et des traces d’autres gaz éliminés par voie respiratoire ou intestinale, voir même cutanée.
d Fibres et transit.
Les fibres végétales sont hygroscopiques et difficiles à digérer. Elles maintiennent les selles humides et augmente leur volume, ce qui provoque une augmentation de la vitesse du transit.
A dose préconisée, les fibres entraînent une accélération des transits lents (>3 jours) et un ralentissement des transits rapides (<1jour).
e Effets des fibres.
· Digestion et absorption des lipides.
On observe trois effets majeurs :
- Prévention de l’athérome (en liaison avec le métabolisme du cholestérol) ;
- Prévention des choléithiases (cristaux dans les canaux biliaires) ;
- Prévention du cancer du colon par effet sur la flore intestinale.
En fait, toutes ces indications sont empiriques car les mécanismes réels sont encore hypothétiques.
Une augmentation du transit entraînerait une diminution de l’absorption de cholestérol en le piégeant dans les sels biliaires.
Il y a un effet écran produit par les substances hydrocolloïdales qui forment un film de protection au contact des entérocytes par rapport au milieu de la lumière intestinale.
· Effet sur le métabolisme des glucides.
Les fibres végétales améliorent la tolérance aux glucides et pendant les épreuves d’hyperglycémie provoquée (voie orale) permettent de faire diminuer le pic.
· Effet sur le métabolisme minéral.
Les fibres, par des phénomènes de chélation vont retenir les minéraux tels que Fe, Cu, Zn, Mg, Ca … Ces ions seront donc mal absorbés.
F Glycémie et index glycémique.
On réalise les mesures au réveil et deux heures après la fin du repas. En général, on va trouver une valeur comprise entre 0,8 et 1,4g/L.
L’index glycémique permet de différencier les sucres « lents » et les « rapides ». Les sucres « lents » sont des sucres qui pénètrent lentement dans le sang.
Les sucres rapides sont de petite taille et élèvent rapidement la glycémie. Ils sont à éviter dans les cas de diabète ou d’obésité.
L’index glycémique est le fait que la glycémie augmente plus ou moins vite et atteint un pic, puis, redescend, ce qui forme un triangle. Le pic maximal est obtenu entre 20 minutes et 25 minutes.
La classification entre sucres lents rapides est supplantée par la notion bons ou mauvais glucides.
Le classement de cet index, ou glycémie, à une valeur de 100% ; les raisins 85%, les patates 80%, riz blanc 72%, riz brun 66%, pâtes 60%, saccharose 60%, pois 50%, pommes 39%, lait écrémé 32%, lentilles 29%, soja 15%.
G Les boissons alcoolisées.
1 La fermentation alcoolique.
Il y a apparition d’éthanol à partir de glucose. Tous les fruits sucrés donneront de l’éthanol.
Par exemple, un vin à 12% indique que l’on a 12mL d’éthanol dans 100mL de ce vin ; c’est la même chose pour les bières et les autres alcools…
2 La distillation
On part d’un besoin alcoolisé : on a besoin d’une boisson plus alcoolisée que la boisson de base.
A partir de vin, on va former le cognac et l’armagnac ; le cidre est la base du calvados ; la canne à sucre va permettre la fabrication du rhum.
Les origines de l’alcool sont différentes pour le whisky et la vodka.
Le métabolisme de l’alcool est toujours un sujet d’études.
1g d’éthanol libère 7kcal (soit 29,3J).
L’alcool ingéré doit être métabolisé par l’organisme avec une priorité absolue ; d’où le danger de prises multiples et rapides d’alcool en un temps restreint.
On distingue trois voies métaboliques pour la dégradation de l’alcool :
- Voie normale : « l’Alcool Déshydrogénase ».
Le NAD est un co-enzyme qui intervient dans tous les métabolismes glucidiques. L’absorption trop importante d’alcool fait dériver le NAD.
- Système microsomal oxydant l’éthanol,
- Système péroxydasique.
 Ces deux dernières voies sont dangereuses car elles interviennent quand la voie normale est saturée. Elles nécessitent le NADPH2, des enzymes des microsomes, des acides nucléiques et des acides aminés cellulaires.
Ces deux dernières voies sont dangereuses car elles interviennent quand la voie normale est saturée. Elles nécessitent le NADPH2, des enzymes des microsomes, des acides nucléiques et des acides aminés cellulaires.
La courbe de Widmark (avec flèche d’alcoolémie).

A partir d’une alcoolémie donnée, à un temps 0, et à condition de cesser les prises alcooliques, l’éthanolémie diminue d’environ 0,2g/L/h.
III La digestion des lipides.
A Sources.
1 Groupe 1, lait et dérivés.
Le lait contient 3,9% de lipides (39g/L).
A l’état naturel, les lipides sont sous forme de globules gras, maintenus dispersés et stables, à 37°C et sous l’action émulsifiante des lécithines.
Au froid, les globules montent à la surface et forment la crème.
Les fromages ont un taux moyen de lipides de 25%, mais ces lipides sont exprimés par rapport à l’extrait sec.
2 Groupe 2, viandes, poissons et œufs.
Les viandes rouges possèdent 20% de lipides, le porc 25%, l’agneau 24%, le mouton 19%, le veau 10%, le cheval 2% et la charcuterie 30 à 40%.
Les volailles maigres (poulets, pintades) et les lapins (cuniculture) possèdent environ 10% de lipides. Les volailles grasses comme les canards 18%, les oies 33% et les dindes 22%.
Les poissons ont en moyenne 7% de lipides.
Les poissons maigres montrent moins de 5% de lipides (limande, sole), les demis gras ont entre 5 et 10% (sardine, saumon) et les gras (anguille, thon) ont plus de 10% de lipides.
Les œufs comprennent environ 11% se répartissant e, 0,2% dans le blanc et 92% dans le jaune.
3 Groupe 3, corps gras.
Dans ce groupe, on va trouver les graisses animales (lard, saindoux) et les lipides végétaux (huile d’olive, d’arachide) qui comprennent 100% de lipides.
Le beurre ne contient que 83% de lipides et la crème autour de 30%.
On attribue aux lipides, le goût différentiel des viandes (en fonction des concentrations, et de la nature des lipides).
4 Groupe 4, céréales et dérivés – produits sucrés.
On trouve très peu de lipides dans ce groupe. Par exemple, le grain de blé contient 1,5% de lipides et le cacao est l’exception de ce groupe, avec 29% de lipides.
5 Groupe 5, Plantes potagères (ou « légumes ») et Fruits.
Ce groupe montre aussi très peu de lipides avec en général moins de 1% de lipides.
On trouve cependant une exception : les oléagineux. Ces plantes montrent un taux très importants de lipides : 50 à 60%.
Les châtaignes ont seulement 2,6% de lipides.
6 Groupe 6, les boissons.
Le taux moyen de lipides est de 0% dans ce groupe.
B Besoins.
L’AET en lipides est compris entre 30 et 35%.
Les lipides de constitution sont retrouvés dans les viandes.
C La digestion (des triglycérides).
Les acides gras sont généralement des C16, C18 ou C20.
Parmi les lipides, on trouve les triglycérides, le cholestérol, les vitamines liposolubles (A : vision de nuit par le carotène ; D : ossification ; E : impliquée dans le vieillissement mais aussi la gestation ; K : impliquée dans la coagulation).
La digestion des lipides met en jeu la salive. Il existe une lipase linguale, sécrétée par la face dorsale de la langue, par les glandes de Ebner. C’est une enzyme peu importante chez l’Homme, mais importante chez le rat, la souris.
Dans l’estomac, il y a des effets chimiques par l’HCl ainsi que l’action de la chaleur et du péristaltisme. Les lipides vont ainsi commencer à s’émulsionner.
Dans le suc gastrique, on cite l’existence d’une lipase gastrique « pré duodénale ».
 Finalement, on obtient l’hydrolyse des triglycérides qui aboutit à la formation d’acides gras à chaîne courte et d’acides gras insaturés à chaîne longue. Au final, on obtient des acides gras libres et des 1,2diglycérides.
Finalement, on obtient l’hydrolyse des triglycérides qui aboutit à la formation d’acides gras à chaîne courte et d’acides gras insaturés à chaîne longue. Au final, on obtient des acides gras libres et des 1,2diglycérides.
Dans la période néonatale, l’activité de la lipase pancréatique est faible ; les lipides du lait doivent être digérés ; 30% des triglycérides ingérés du lait seraient digérés dès l’estomac ; dans les triglycérides du lait, on retrouve beaucoup d’acides gras à chaînes courtes et moyennent hydrophiles qui sont absorbés par voie sanguine directe, par la muqueuse gastrique, comme l’alcool.
Le duodénum (longueur, 50 cm).
Dans les phases prandiales, la vésicule biliaire se contracte et fait passer la bile dans le duodénum, par le canal cholédoque. La bile (sans enzyme) contient des acides et des sels (Na) biliaires.
On va trouver l’acide glycocholique, l’acide taurocholique, l’acide désoxycholique l’acide lithocholique et l’acide chénodésoxycholique.
Les sels biliaires ont un rôle majeur.
Grâce à l’émulsion des graisses dès le duodénum. Ils ont des propriétés leur faisant diminuer la tension superficielle.
Leur action est indispensable :
- pour que les lipides se transforment en globules de 0,5 à 1µm de diamètre (indispensable à l’action de la lipase pancréatique),
- pour l’absorption des vitamines liposolubles,
- pour la digestion des autres aliments car si les lipides ne sont pas digérés, ils entourent les aliments, ce qui empêche les enzymes d’agir. Il y aurait dans ce cas une prolifération de bactéries intestinales avec un phénomène de putréfaction et un surplus de gaz (aussi appelé, météorisation).
La lipase pancréatique.
Cette lipase a un rôle majeur et déterminant car elle agit à l’interface huile/eau des gouttelettes lipidiques finement émulsifiées.
La co-lipase. C’est une protéine qui est sécrétée en pro-enzyme. Elle est présente dans le suc pancréatique et a une action synergique à la lipase.
La phospholipase, également sécrétée en pro-enzyme, va former des phospholipides.
Ces deux enzymes passent du stade pro-enzyme au stade enzyme par coupure d’un pentapeptide, ce qui les active.
La lipase pancréatique agit en surface, sur les globules émulsionnés, en libérant un mélange de diglycérides, de monoglycérides, de glycérol libre et des acides gras libres. Dans ce processus, les sels biliaires interviennent en plus en favorisant la formation de particules hydrosolubles (les micelles).
La structure des micelles est analogue à celle de l’émulsion lipidique mais plus petite. Les groupements non polaires (acides gras, monoglycérides et sels biliaires) sont orientés vers le centre. Les groupements polaires, hydrophiles, sont en surface.
Les micelles ont un diamètre de 3 à 00nm. Il s’agit de quelques milliers de molécules (solution claire).
La solution lipidique a des particules de diamètre de 0,5 à 10µm qui forment une solution sombre.
Après la digestion intraluminale des lipides, il y a au contact de la membrane des entérocytes, trois fractions différentes :
- gouttelettes d’émulsion lipidiques insolubles,
- micelles solubles,
- molécules libres (acides gras, monoglycérides, glycérol et stérols).
D L’absorption.
L’absorption des lipides est complexe. Les micelles sont au contact de la membrane apicale des entérocytes, dans le feutrage de glycoprotéines. Les acides gras libres surtout, et les monoglycérides, passent dans l’entérocyte par diffusion passive.
Les micelles libèrent leurs composés pour en accepter d’autres, au fur et à mesure de l’action de la lipase pancréatique.
Dans l’entérocyte, les acides gras libres sont activés en AcylCoA. Ils se combinent ensuite à des monoglycérides et reconstituent des triglycérides, lesquels s’unissent à des protéines et forment de fines gouttelettes : les chilomicrons, de diamètre compris entre 0,1 et 0,5µm. Ces chilomicrons sont le mélange de lipoprotéines, de triglycérides, de cholestérol et de vitamines liposolubles.
Les chilomicrons sont expulsé de l’entérocyte au pôle basal par exocytose. Ils passent ensuite dans les vaisseaux chylifères. Ils ne peuvent pas passer par les capillaires sanguins car ils sont recouverts d’un réseau de polysaccharides qui s’y oppose ; mais aussi, le diamètre est trop faible pour pouvoir les accepter. Le glycérol et les acides gras à courte chaîne (inférieur aux C12) sont absorbés par voie sanguine (voie portale).
Le cholestérol non estérifié prend la même voie que les acides gras libres, ré-estérifiés dans les entérocytes.
IV Protéines et digestion.
A Les sources.
1 Groupe 1, lait et dérivés.
Ce groupe montre une richesse en protéines. Le lait alimentaire (lait de vache) montre un taux moyen de 3,5% de protéines.
On trouve des variations selon l’animal mais aussi selon des variations naturelles : alimentation, saison, cycle de lactation.
Les protéines du lait sont représentées par les caséines (α, β, γ et K). Les caséines sont soumises à l’action de la présure, extraite de la caillette de jeunes veaux. Fonctionnement avec du Ca2+, un pH acide et une température proche de 40°C. Cette présure va attaquer la caséine K et former un précipité qui évoluera en caillé. Ce dernier donne le fromage par expulsion de lactosérum (mécanisme de synergie). On trouve le même processus dans la coagulation naturelle du sang.
Le sérum est un ensemble plasma – fibrinogène.
En plus, on trouve de la lactalbumine et de la lactoglobuline. Le caillé est un concentré de lipides et de protéines. Le lactosérum contient les produits hydrosolubles.
2 Groupe 2, viandes, poissons et œufs.
Les viandes comprennent environ 18% de protéines. La charcuterie, 25 à 26% ; les volailles et lapins, environ 20% ; les poissons entre 18 et 22% ; les œufs, 13% dont 11% dans le blanc et 16% dans le jaune.
3 Groupe 3, corps gras.
On ne trouve pas de protéines dans ce groupe.
4 Groupe 4, céréales et dérivés – produits sucrés.
Pour les céréales et dérivés, on retrouve 10 à 11% de protéines sans les grains de blé, riz, maïs…
Les produits sucrés, comme le cacao, contiennent 21% de protéines.
5 Groupe 5, Plantes potagères (ou « légumes ») et Fruits.
Les plantes potagères :
- légumes et tubercules : 1 à 2%
- graines de légumineuses : 18 à 24% en moyenne (soja, 35%)
Champignons : 2,4%
Fruits :
- frais (aqueux) : moins de 1% de protéines
- graines d’oléagineux : entre 14 et 21% de protéines
- fruits amylacés, environ 4%
6 Groupe 6, les boissons.
Pas de protéines.
B Les besoins.
Les besoins en protéines ont des particularités. Les protéines ont un aspect « plastique » ou « constitutionnel ». Le corps possède des protéines à renouveler, par exemple :
- les protéines des muqueuses,
- les protéines musculaires,
- les hormones (très nombreuses),
- les enzymes,
- les anticorps.
Il y a aussi les pertes minimales d’azote (qui sont obligatoires). Pour un homme adulte, il y a perte de 54mg d’azote par jour et par kilo de poids. Les pertes sont représentées par les urines, les matières fécales, la sueur, les menstruations (chez la femme) et par les cheveux et ongles (les phanères).
Les protéines peuvent être apportées selon deux sources (animales ou végétales). Les protéines animales sont les meilleures à cause du problème des acides aminés indispensables. Elles devraient représenter ½ à 2/3 des protéines alimentaires.
De nombreux travaux ont été faits pour optimiser les protéines et l’alimentation. Trois facteurs ressortent :
- la quantité protéique, 12 à 14% de l’AET ;
- le taux de digestibilité protéique, qui s’étudie par de multiples facteurs ;
- l’aspect de qualité protéique, tenant compte de la composition en acide aminés essentiels pouvant être absorbés et donc, utilisés par l’organisme.
Ces trois facteurs ont donné lieu à l’expérimentation ancienne de « nutrition » qui a permis de classer les protéines végétales.
On va s’intéresser à trois « phénomènes » : l’azote ingéré (Ni), l’azote urinaire (Nu), l’azote fécal (Nf).
Le dosage de l’azote est très sur et comporte deux étapes : la minéralisation sulfurique (une masse organique est soumise pendant 24 heures à l’action de H2SO4 [pur] à 900°C) qui permet de mettre toutes les formes d’azote en la forme (NH4)2SO4 ; le dosage par la méthode de Kjeldahl. [P] = [N] x 6,25.
On peut faire ces mesures sur l’Homme, les animaux, en utilisant des « cages à métabolisme ».
Ni – Nf = Nobservé
Ni (ingesta) – (Nu + Nf) (excreta) = Nretenu
Le Coefficient d’Efficacité Protéique (CEP).
CEP = ΔP (g ou kg)/N
Le Coefficient d’Utilisation Digestive (CUD).
CUD = [(Ni - Nf)/Nf]-[Nabsorbé/Ningéré]
La Valeur Biologique (VB).
VB = [Ni – (Ni + Nf)]/[Ni – Nf] = Nretenu / Nabsorbé
L’Utilisation Protéique Nette.
UPN = Nretenu / Ningéré
La plupart des protéines alimentaires contiennent environ 16% d’azote.
Les besoins protéiques moyens.
Ce besoin moyen est de l’ordre de 1 gramme de protéine par kilogramme par jour (chez un adulte). Cette valeur passe à 6 grammes par kilogramme et par 24 heures pour une femme enceinte et à 16 gramme pour une femme allaitante.
On retrouve 9 acides aminés essentiels ; ils doivent absolument être apportés en même temps et en quantité optimale.
Pour le classement des protéines, on utilise divers facteurs nutritionnels et si l’on prend l’UPN, chez les rats, on obtient le classement suivant :
- œufs 94%
- lait de vache 82%
- poisson 80%
- riz en grain 70% après cuisson
- soja 61% après cuisson
- blé 40% après cuisson.
Le facteur limitant en protéines est l’acide aminé essentiel de la protéine par rapport à celle de l’œuf.
La référence aux préférences de l’œuf est remplacée par des données de la FAOMS en mg d’acides aminés essentiels par gramme de protéine.
Comme facteur limitant, on trouve la zéine : lysine + tryptophane. Dans les céréales, c’est la lysine qui est limitante.
Les protéines végétales sont d’un sont d’un coût inférieur aux protéines animales. De plus, on peut suppléer ces protéines végétales, soit en ajoutant les acides aminés manquant, soit en pratiquant des mélanges de diverses sources végétales.
Quelques exemples empiriques :
- En Chine, il y a le mélange riz + soja
- En Amérique du Sud, mélange maïs + haricots rouges
- En Afrique du Nord, mélange semoule + pois chiche ou bien semoule + lait caillé.
- En Inde, mélange, riz + lentilles
- En France, mélange flocon de céréales + lait du yaourt ou bien, pain + fromage, ou bien, riz + fromage, ou lait + patates (mais pauvres en leucine).
C Digestion.
1 La bouche.
Au niveau de la bouche, la mastication permet un début de clivage dans les aliments.
2 L’estomac.
Dans l’estomac, la présence d’HCl va entraîner la dénaturation (chimique) partielle de protéines. Grâce à l’HCl, le pepsinogène va former la pepsine par hydrolyse d’un peptide. On trouve des endopeptidases à pH optimum de 1,6 à 2,4 et de poids moyen de 35 000Da.
L’hydrolyse est préférentielle entre les acides aminés aromatiques (tryptophane, phénylalanine, tyrosine) et les acides dicarbolxyliques (glu). Celle-ci s’en gage par le NH2.
On voit également que le pouvoir de digestion est contenu dans les sécrétions pancréatiques. En effet, on supporte une ablation de l’estomac, bien qu’il faille des prises alimentaires fragmentées et que l’on observe l’absence de sécrétion du facteur intrinsèque, indispensable pour l’absorption de vitamine B12 dans l’iléon. Cette absence de sécrétion est appelée anémie de Biermer ou anémie pernicieuse. Il y a donc apport supplétif obligatoire.
· La présure ou « rénine » ou « chymosine ».
Cette enzyme est présente seulement chez les nourrissons. Elle attaque les caséines en présence de Ca2+. Elle est absente chez l’adulte où là, il y aura action de la pepsine. On trouve de la présure car le nourrisson a un estomac peu acide.
3 Le duodénum.
Le duodénum est le lieu majeur de l’hydrolyse des protéines grâce au déversement du suc pancréatique (nombreuses protéases et peptidases) avec deux points communs :
- sécrétion sous forme de précurseurs inactifs (grains de zymogène),
- pH optimum de 7 à 8 ; le pH est remonté par les ions HCO3- de la bile et du suc pancréatique.
Le Endopeptidases.
Il y a également sécrétion d’endopeptidases. Par exemple, l’entérokinase duodénale (émise par certaines cellules du duodénum) va cliver le trypsinogène en trypsine (T) plus un heptapeptide. La trypsine est activée par des ions Ca2+ et va hydrolyser préférentiellement des liaisons peptidiques proche des acides aminés basiques, engagés par leur COOH.
Il existe également des facteurs dits « anti-trypsiques », contenus dans certains aliments : le blanc d’œuf qui donne une glycoprotéine ou ovomucoïde ainsi que légumineuses (de la plus faible inhibition provoquée à la plus forte inhibition provoquée) haricot cru, soja, lentilles, petits pois.
Le chymotrypsinogène est clivé en chymotrypsine par l’action de la trypsine. La chymotrypsine va préférentiellement cliver les acides aminés aromatiques, engagés par leur COOH.
La proélastase est clivée en élastase par la trypsine. Elle va hydrolyser des petits acides aminés (glycine, alanine)
La collagénase : elle hydrolyse quelques liaisons peptidiques du collagène.
Il faut noter que l’on trouve un système d’autorégulation de la trypsine selon la prise alimentaire et la quantité de protéines.
Les Exopeptidases.
On trouve la procarboxypeptidase qui est activée en carboxypeptidase sous l’action de la trypsine. Elle va hydrolyser la liaison peptidique côté COOH et libérer un acide aminé à la fois.
On peut également trouver des ribonucléases pour l’ARN et des désoxyribonucléases pour l’ADN.
Le suc intestinal.
Ce suc est sécrété par les glandes de Bruner et de Lieberkühn. On retrouve dedans, des aminopeptidases qui hydrolysent des liaisons peptidiques où sont engagés les acides aminés à NH2 terminal ; mais aussi des tri-oligopeptides et oligopeptides qui vont former des acides aminés libres.
D L’absorption.
Il y a similitude d’absorption par les entérocytes du glucose et des acides aminés.
La concentration en acides aminés dans l’entérocyte est plus forte que dans la lumière intestinale. On retrouve le même schéma d’absorption que le glucose.
On admettra qu’il existe plusieurs types de transporteurs dépendant du Na+ et spécifiques (neutres, basiques, dicarboxyliques) ou de tel ou tel acide aminé (exemple : phénylalanine, leucine, lysine).
Quelques protéines peuvent être absorbées par les entérocytes sans transformation majeure. C’est le cas classique des Anticorps du lait maternel qui vont faire bénéficier l’enfant de la protection immunologique de la mère.
Chez l’adulte, il peut y avoir absorption de di ou tripeptides par des transporteurs.
Dans tous les cas, les molécules en question seront absorbés par voie sanguine, donc portale.
V Mammifères, oiseaux et digestion.
A Présentation.
Il y a beaucoup de données, essentiellement pour deux types d’animaux :
- Animaux à intérêt zootechnique
- Animaux de compagnie (en général monogastriques).
Parmi les herbivores, on retrouve le cheval et les lapins ; parmi les omnivore, on a les porcs et les volatiles chez les granivores.
Parmi les animaux de laboratoire, on cite : la souris, le rat, le chien, le cobaye, le lapin, le singe.
Il y a ressemblance du TD de l’Homme avec celui du rat mais surtout du porc. La peau et les yeux humains ressemblent à ceux des lapins et cobayes. Notre système nerveux est comparable à celui des singes.
Les travaux de toxicologie sont principalement réalisés sur des rats singes et rats.
B Anatomie.
1 Bouche et dents.
a Le cheval.
La formule dentaire du cheval est connue. Les lèvres sont mobiles. Les chevaux peuvent pâturer l’herbe plus ras que les bovins.
b Les porcs.
Ces animaux ont une dentition d’omnivore. Il possède un groin qui leur permet de fouir.
2 L’estomac.
a Le cheval.
L’estomac est en cornemuse, dans la partie droite de l’abdomen. Sa taille réduite (15 à 18 litres). La muqueuse interne a deux aspects :
- cul-de-sac à gauche où arrivent les aliments sont dans la partie blanche et plissée (sans glande digestive)
- cul-de-sac à droite : la muqueuse est rose et violacée, avec des glandes gastriques. Le cardia est très serré et interdit tout retour en arrière des aliments (vomissement impossible). Le pylore est largement ouvert. Les aliments restent peu de temps dans l’estomac qui va se vider dès qu’il se rempli. Il n’a qu’une capacité d’un volume.
b Les oiseaux.
Ils ont un estomac avec trois poches :
- Le jabot : simple réservoir où ramollissent les graines ; pas de glandes digestives.
- Le ventricule succenturié : élargissement du tube digestif, peu développé, la muqueuse interne a des glandes gastriques. Les aliments ne font que passer mais s’imprègnent de sucs gastriques.
- Le gésier : on y trouve une membrane coriace, entourée de muscles puissants où les aliments comme les graines vont être broyés. Le broyage est favorisé par les graviers ingérés avec les graines par les oiseaux.
3 L’intestin.
a L’intestin grêle.
Le développement de l’intestin grêle dépend de l’alimentation de l’espèce. Court et gros calibre chez les carnivores ; étroit et long chez les herbivores.
En moyenne, deux fois plus long chez le bœuf que chez le cheval ; mais l’intestin grêle de cheval a un diamètre deux fois plus gros. C’est la surface d’absorption qui compte.
b Le gros intestin.
Le développement de cette partie de l’intestin est en rapport avec le régime alimentaire : court chez les carnivores et long et compliqué chez les herbivores. Le cheval a un développement exceptionnel de 130 à 140 litres !!! Les ¾ de sa capacité digestive. En comparaison, le bœuf n’a une capacité digestive que de 40 litres.
Cet intestin est divisé en trois parties :
- le caecum : poche en cul-de-sac, bosselé chez le cheval, lisse chez le bœuf ;
- le colon : partie la plus longue ; celle du cheval est spéciale : elle fait 3 mètres de long, 80 centimètres de diamètre et divisée en deux parties (colon repli et colon flottant dont le dernier qui est beaucoup plus petit) ; Remarque : chez l’Homme, le colon est ascendant, transverse, descendant, et sigmoïde ;
- le rectum : c’est la partie terminale, reliée à l’anus. Remarque : chez les oiseaux, la différence avec l’intestin grêle n’existe pas.
Chez la poule, on a deux caecums de 8 centimètres débouchant dans la partie terminale de l’intestin, débouchant dans le cloaque.
On va distinguer les ruminants qui ont une digestion stomacale et les non ruminants qui ont une digestion intestinale et qui peuvent avoir des pathologies d’ordre cholique et des colites.
C Quelques éléments de physiologie.
1 Le cheval.
La mastication du cheval est plus complète que chez les ruminants et les carnivores car il ne fait pas de rumination.
La sécrétion salivaire est intermittente (se fait lors des repas) et représente 5 à 50 litres par jour. Cette sécrétion est fonction de la richesse en eau des aliments.
Le brassage stomacal est insignifiant : en effet l’estomac se vide 2 ou 3 fois durant un repas. On va trouver un brassage intestinal prolongé, surtout au niveau des caecums.
Au niveau des rations, on va trouver un fractionnement de l’alimentation en 8 repas journaliers. Les aliments sont concentrés ne sont à donner qu’après le fourrage.
2 Le porc.
La mastication est intermédiaire entre celle des carnivores et celle des herbivores. Le porc a une salivation moyenne de l’ordre de 15 litres par jour.
3 La volaille.
On a un ramollissement des aliments dans le jabot qui est dépourvu de glandes salivaires. L’hydratation se fait par l’eau de boisson qui humidifie les aliments. LA salivation est insignifiante : 10 à 15mL/jour.
Le broyage a lieu après le ventricule succenturié et le malaxage se fait dans le gésier, avec l’aide de petits graviers.
VI Symbiose et digestion.
(Ou apports symbiotiques des aliments).
A Introduction.
Le tube digestif des eucaryotes abrite des microorganismes participant plus ou moins, par leurs activités métaboliques, à la fourniture de nutriments directement utilisables (par les cellules hôtes). On peut citer des symbiotes intracellulaires et coelomiques.
B Les symbiotes du tube digestif.
1 Les symbiotes intracellulaires.
On trouve diverses espèces d’invertébrés allant des coelentérés aux mollusques. Ces animaux peuvent héberger dans certaines cellules, des algues vertes (des zoochlorelles) ou brunes (des zooxanthelles). A la lumière, les algues vont synthétiser des sucres simples mis à la disposition de l’hôte.
2 Les symbiotes coelomiques.
On trouve par exemple certains invertébrés vivant près des cassures tectoniques.
Les bactéries impliquées sont capables d’utiliser un certain type d’énergie, fournie par l’oxydation du H2S et des sulfates qui abondent dans les sources d’eaux chaudes et au niveau de ces cassures
Par exemple, on peut citer un pogonophore (Riftia pachyphila) qui peut mesurer jusqu’à un mètre. Sa cavité coelomique est largement occupée par de grandes poches appelées des trophosomes qui sont remplies de bactéries, qui, dans ce milieu, synthétisent de l’ATP et fixent du CO2.
a Digestion de la cire d’abeilles (cire de nids).
Cette cire est essentiellement composée de lipides. Des oiseaux se nourrissant de cette cire vont posséder des microorganismes dans leur intestin (bactéries comme Micrococcus cerolipicus et des levures comme Candida albicans).
b Digestion de la cellulose.
La cellulose est le polysaccharide de structure majeur de la paroi végétale, l’alimentation de base des herbivores et des xylophages.
On trouvera principalement des microorganismes anaérobies qui digèrent la cellulose et qui fournissent ainsi des acides venant du métabolisme oxydatif anaérobie du glucose, ainsi que du CO2 et du méthane.
Beaucoup d’invertébrés se nourrissent de cellulose par le biais de microorganismes symbiotiques. On trouve dans ce cas les termites inférieurs qui sont xylophages et qui peuvent compter jusqu’à 45 espèces de flagellés symbiotiques (les termites supérieurs sont herbivores). La vie de ces animaux est OBLIGATOIREMENT symbiotique.
Chez les vertébrés, on v trouver des bactéries et des protozoaires symbiotiques qui peuvent attaquer la cellulose par action de la cellulase (enzyme). Ceci est optimisé chez les herbivores et particulièrement les ruminants. On note aussi la présence d’un système différent, qui consiste à recycler les fécès : la coprophagie.
L’ingestion de fécès est importante pour de nombreuses espèces, cela allant des poissons jusqu’aux mammifères.
L’auto coprophagie existe est assez rare. Dans la plupart des cas, les animaux mangent les fécès d’autres espèces. Il y a ainsi apports de nutriments particuliers.
Par exemple, les chiens, chats et chevaux ont un régime alimentaire déséquilibré. En général, les herbivores mangent les fécès des carnivores. Les espèces auto coprophages sont par exemple les rongeurs : castor, écureuil, chinchilla, lapin ainsi que certains lémuriens comme l’opossum et le koala.
La digestion de la cellulose a lieu dans l’intestin. Il y a ré ingestion immédiate des fécès particulièrement appelés caecotrophes (fécès ayant la même composition que le bol alimentaire mais avec des microorganismes qui sont expulsés et qui les différencient des autres fécès) Ces fécès sont également riches en eau et avalés sans mastication, puis, stockés dans une poche antérieure de l’estomac, non acide.
Ici, l’action des microorganismes continue jusqu’à une nette amélioration du rendement de la cellulose plus des gains en composés azotés et en nutriments essentiels, procurés par les microorganismes qui sont eux-mêmes digérés.
C Les ruminants.
Mérycisme est un synonyme de rumination.
L’estomac des ruminants forme deux compartiments principaux, séparés par des constrictions transversales. L’estomac antérieur va former les chambres d’origine oesophagiennes alors que l’estomac postérieur, glandulaire, est comparable a un estomac classique de mammifères.
a Rumen ou Panse.
Cette poche est la plus volumineuse. Elle représente 80% du volume stomacal (250 litres chez la vache).
b Réticulum ou Bonnet (ou réseau également).
C’est la poche la plus antérieure et la plus petite. Elle représente environ 5% du volume gastrique (15 litres chez la vache).
c Omasum ou Feuillet.
C’est la troisième poche représentant autour de 8% du volume total (20 litres chez la vache).
d L’Abomasum ou Caillette.
C’est cette partie qui représente l’estomac classique des mammifères. Il fait environ 8% du volume total. Il assure la sécrétion de HCl et de pepsinogène.
La panse et le bonnet renferment une culture de microorganismes anaérobies avec de nombreuses bactéries et des champignons inférieurs et des protozoaires ciliés appartenant à deux familles (Isotrichidae et Orphyoscocelidae). On a entre 105 et 1010 individus par mL de ce « bouillon de culture ».
Le métabolisme de cette flore donne des acides gras volatils mais aussi du méthane et du CO2 en proportions variables selon le type de nourriture ingérée et le type de microorganismes dominants. L’essentiel du méthane et du CO2 est éliminé par éructation, ce qui est indispensable la rumination.
La grande partie des acides gras volatils est absorbée au niveau des trois 1ères poches. Le pH est à peu près neutre. On trouve une grande production salivaire, continue, estimée à 200 litres par jour pour la vache.
Le reste passe dans la caillette avec une attaque des protéines, puis passe dans l’intestin avec un système de digestion proche des autres mammifères.
La rumination a été très étudiée, et surtout les systèmes réflexes qui la commandent.
Chez la vache, 2 à 4 kg de microorganisme sont digérés par l’hôte, ce qui lui apporte une grande quantité de produits azotés. Une part des l’azote est recyclée car la vache récupère sous forme d’urée une bonne partie des groupements NH2 venant de son métabolisme protéique.
Il y a récupération d’ammoniac venant de l’activité bactérienne et ainsi, les ruminants assurent une certaine balance azotée alors que leur régime alimentaire en est pauvre.
La température centrale de ces animaux est environ supérieure de 1 à 2°C par rapport à l’Homme. La rumination prend entre 4 et 10 heures par jour. La glycémie est de l’ordre de 0,6g/L.
Chapitre 3 :
Physiologie de la respiration.
I Principes généraux.
A Le milieu de respiratoire.
L’air et l’eau ont des propriétés différentes et particulièrement la solubilité des gaz (O2 et CO2).
1 Solubilité des gaz respiratoires.
La solubilité est l’aptitude d’un gaz se dissoudre.
A l’équilibre, la concentration en O2 est différente selon le milieu où l’on se situe. Ceci est du à la solubilité de l’O2 qui est différente entre l’eau et l’air.
Pour ce qui concerne le CO2, les résultats ne sont pas du même genre, les concentrations à l’équilibre sont quasiment les mêmes, que l’on soit dans l’eau ou dans l’air. Le CO2 a une solubilité 30 fois supérieure à celle de l’O2.
Dans l’air, la quantité d’O2 disponible ne dépend pas de la température alors que dans l’eau la concentration en O2 est dépendante de la température :
- Plus l’eau est froide, plus l’O2 se dissout.
- Plus l’eau est chaude, moins l’O2 se dissout.
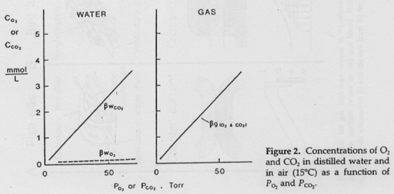
La courbe de la concentration du gaz est fonction de la pression partielle du gaz.
 Un animal respirant dans l’eau a peu d’O2 à sa disposition : en milieu aquatique, les consommations d’O2 doivent être faibles.
Un animal respirant dans l’eau a peu d’O2 à sa disposition : en milieu aquatique, les consommations d’O2 doivent être faibles.
2 Densité et viscosité.
La densité de l’eau est 800 fois supérieure à celle de l’air.
La viscosité de l’eau est 50 fois plus importante que celle de l’air.
 La mécanique ventilatoire est beaucoup plus difficile dans l’eau que dans l’air.
La mécanique ventilatoire est beaucoup plus difficile dans l’eau que dans l’air.
Dans l’eau, à 15°C, on trouve 7mL (environ 10mg) d’O2 par litre d’eau (1kg).
Pour avoir un gramme d’O2, il faut remuer 100kg d’eau.
Un litre d’air contient 210mL d’O2 et 790mL de N2.
Conséquence : La plupart des animaux à respiration aérienne ont des mouvements respiratoires bidirectionnels. Les animaux aquatique ne peuvent pas se permettre de faire cette double circulation : ils effectuent uniquement des mouvements unidirectionnels, ce qui limite le travail ventilatoire.
Le fait que le CO2 soit très soluble et que les poissons soient obligés de brasser beaucoup d’eau pour peu d’O2 donne un sang artériel très pauvre en CO2 ; la régulation du pH plasmatique est donc différente de celle des animaux à respiration aérienne.
B Les différents types d’appareils ventilatoires.
La branchie est une évagination tégumentaire. Le poumon est une invagination tégumentaire. Le poumon a un avantage énorme : il est protégé car il est interne.
1 La respiration tégumentaire.
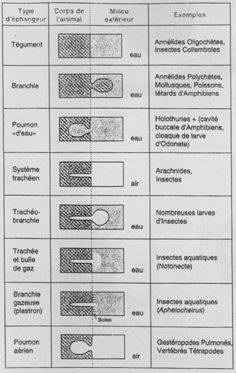
Les animaux pratiquant cette respiration sont assez simples. La surface de diffusion est faible : les échanges sont donc peu importants. De plus, le tégument sert aussi à la protection et rend la diffusion de l’O2 assez difficile (système peu efficace).
Sur le document, il manque le rôle de la circulation :
- Chez les lombrics, l’appareil circulatoire participe à la distribution de l’O2.
- Chez les planaires, il n’y a pas d’appareil circulatoire : l’O2 diffuse donc seul.
- Chez les collemboles, l’appareil circulatoire ne sert pas à la diffusion de l’O2.
2 Le système trachéen des insectes.
L’hémolymphe ne sert pas au transport des gaz respiratoires. Les trachées amènent les gaz jusqu’aux cellules.
Les insectes aquatiques continuent à utiliser les trachées : l’air utilisé sera soit sous forme de bulle d’air ou de l’O2 dissout dans l’eau qui rentrera dans les trachées par les trachéobranchies sous forme gazeuse (et pourra ainsi diffuser).
C Le problème de la diffusion.
Au niveau de toutes les surfaces d’échanges, le passage de l’O2 se fait par diffusion, par le gradient de pressions partielles (le « moteur »).
Facteurs s’opposant à la diffusion :
- Perméabilité de la surface prise en compte.
- Aptitude à diffuser du gaz (souvent la solubilité).
Dans un système clos, avec une membrane perméable à un gaz, les pressions partielles s’équilibrent et la diffusion s’arrête. Pour qu’il y ait toujours diffusion, il faut renouveler un ou les deux milieux. Le renouvellement du milieu externe est la ventilation et le renouvellement du milieu interne est la convection (sanguine) (pour les animaux avec du sang !).
A partir de là, on a plusieurs possibilités théoriques.
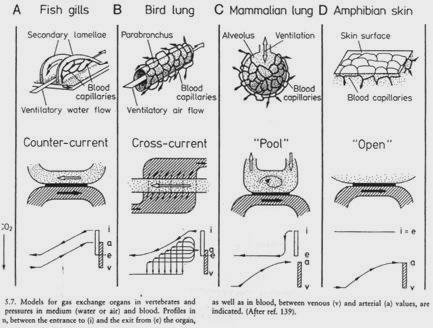
On observe des divisions à cause des mouvements relatifs de la ventilation et/ou de la convection.
En A, on a un système à contre-courant qui permet l’amélioration de l’extraction de l’O2 de l’eau.
En i, on a les pressions partielles en O2 du milieu inspiré.
En e, on a les pressions partielles en O2 du milieu expiré.
V représente le sang arrivant à la branchie (sang afférent).
A représente le sang artériel (sang efférent).
Grâce à ce système à contre-courant, le sang finit par avoir une pression partielle en O2 supérieure à celle de l’air inspiré.
En fait, le courant observé n’est pas à contre-courant mais est un courant croisé : le fluide circule perpendiculairement au sang.
 Ce système est plus efficace que le système à contre courant. On peut montrer ceci sur un canard où l’on inverse le sens du courant d’air : les performances sont conservées
Ce système est plus efficace que le système à contre courant. On peut montrer ceci sur un canard où l’on inverse le sens du courant d’air : les performances sont conservées
En C : on a le poumon alvéolaire. L’air alvéolaire est renouvelé à quelques pourcents par mouvement ventilatoire : si les poumons sont efficaces, on ventile peu car on a une assez grand apport en O2.
Le sang irrigant chaque alvéole s’équilibre à peu près avec l’O2 (à 100% pour le CO2).
En D : on observe trois problèmes : le renouvellement du fluide extérieur, la surface de la peau est faible, l’épaisseur du tégument s’oppose au passage.
II La ventilation des vertébrés.
A Les poissons.
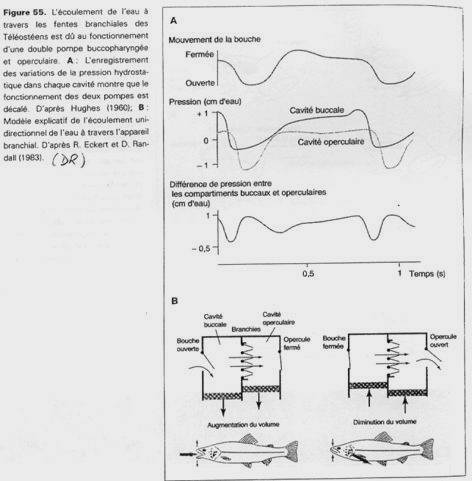
Le mouvement d’eau se fait de la bouche vers l’opercule. L’opercule agit comme une valve (operculaire).
Quand le poisson ouvre la bouche, on a un flux d’eau qui passe à travers les branchies. Ce mouvement d’eau ne s’arrête jamais.
La pression de la cavité buccale est presque toujours supérieure à la pression operculaire.
La fréquence respiratoire est fonction de la vitesse de la nage. Une fois une certaine vitesse passée, il n’y a plus de ventilation musculaire de l’eau : la bouche est ouverte et le courant d’eau se fait grâce à la vitesse. Dans ce cas, la « ventilation se fait par les muscles de la nage ».
B Les amphibiens.
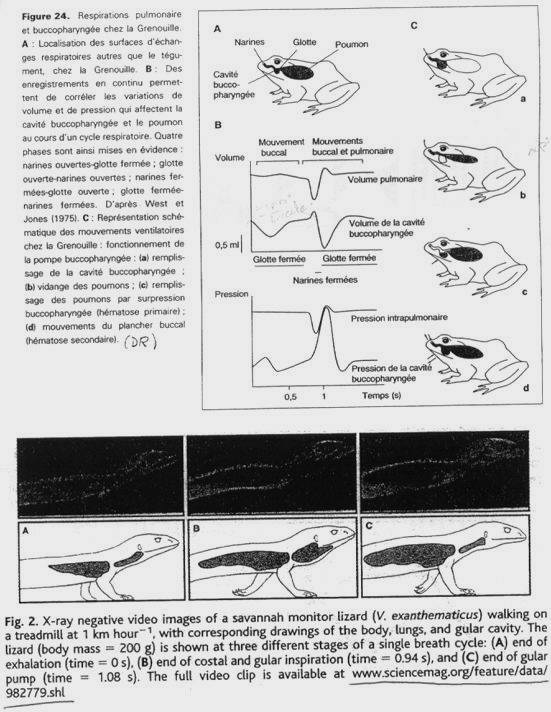
La glotte ouverte ou fermée et l’on a la même chose pour les narines.
Ces animaux ont souvent les narines ouvertes et on observe des mouvements ventilatoires du plancher buccal.
Pour la respiration par les poumons, l’air passe du milieu extérieur à la narine puis est ensuite poussé par la grenouille, vers les poumons, par action de la cavité bucco pharyngée.
 Dans ce cas, on parle de pression positive : l’animal force l’air à entrer.
Dans ce cas, on parle de pression positive : l’animal force l’air à entrer.
Remarques :
· Chez les mammifères, c’est à cause de l’augmentation de volume des poumons que l’air entre, grâce à la dépression créée.
· Les mouvements latéraux des reptiles perturbent la ventilation classique : ils ont donc besoin d’une ventilation par pression positive (de même principe que chez la grenouille).
C Les oiseaux.
Le poumon des oiseaux est irrigué par la trachée et par des sacs aériens (i n’y a pas de diaphragme). La trachée donne deux branches qui vont vers les sacs aériens postérieurs. Ces sacs sont très fins, sans muscles.
Avec l’expiration, l’air va de l’arrière vers l’avant en traversant. Dans ces poumons, le courant, d’air, est unidirectionnel.
Il existe des capillaires aériens entre les parabronches. Ce sont de très fins capillaires. On trouve en plus de nombreux capillaires sanguins.
A la première inspiration, presque tout l’air passe dans le sac postérieur.
A la première expiration, les deux sacs se vident : le sac antérieur envoie son air vers l’extérieur alors que le sac postérieur envoie son air dans les poumons.
A la seconde inspiration, les deux sacs se remplissent.
A la seconde expiration, les deux sacs se vident.
On voit ces phénomènes en faisant inhaler de l’azote radioactif puis en suivant cet azote marqué.
Remarque : chez les oiseaux, on observe un courant croisé et non un contre-courant.
D Les mammifères.
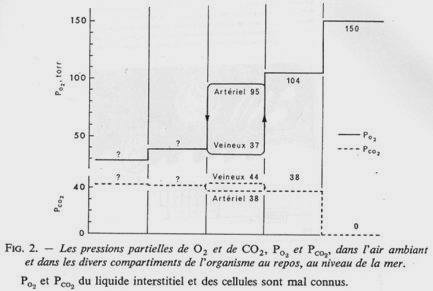
L’air entre par dépression dans les poumons (par élèvement des cotes et abaissement du diaphragme).
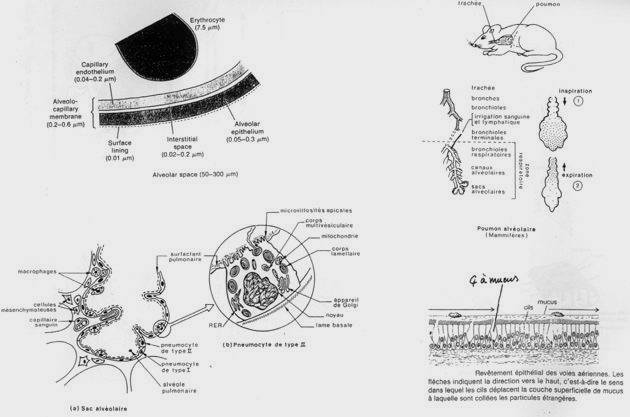
Ce document permet de mettre en évidence les différences entre la zone de conduction de l’air et la zone respiratoire.
La zone de conduction :
Cette zone ne participe pas aux échanges gazeux. Elle sert à humidifier, réchauffer et nettoyer (filtrer) l’air. La vitesse de conduction est décroissante tout au long du parcours car il y a diminution de diamètre à chaque niveau.
La trachée est un anneau cartilagineux avec peu de muscles : le diamètre est relativement constant. Le petites bronches ont, elles, beaucoup de muscles lisses : on pourra assister à des brochodilatations et des bronchoconstrictions.
L’inspiration fait augmenter le volume pulmonaire car les sacs alvéolaires, soumis à la dépression, s’accroissent. On trouve aussi une dépression autour des petites bronches.
La zone respiratoire :
L’épithélium est plat avec des pneumocytes 1 On a aussi des cellules saillantes qui sont les pneumocytes 2, sécréteurs de surfactant.
La barrière sang/air est formée de capillaires avec l’endothélium des capillaires, d’une lame basale et d’un épithélium alvéolaire.
1 Disposition anatomique.
Le poumon est emballé dans une plèvre (interne).
La cage thoracique est tapissée d’une plèvre (externe).
Entre les deux plèvres, on trouve le liquide pleural qui sert à diminuer les frottements et à empêcher de fortes augmentations de tension.
Dans le cas d’un pneumothorax, le poumon tend à se collaber car il ne peut pas respirer. Aucune dépression n’a lieu car l’air vient combler les débuts de dépression.
 Les mouvements des cotes sont transmis aux poumons par l’intermédiaire des plèvres.
Les mouvements des cotes sont transmis aux poumons par l’intermédiaire des plèvres.
2 Mécanique ventilatoire.
· L’inspiration.
L’inspiration se fait par :
- Abaissement du diaphragme (coupole de muscles striés squelettiques) (l’onglet en boucherie).
- Elévation des cotes : cette élévation est principalement fonction de la contraction des muscles intercostaux.
Les cotes peuvent pivoter autour de leur point d’insertion (les vertèbres). Comme ces cotes sont solidarisées par le sternum, elles restent parallèles entre elles.
Les muscles intercostaux externes font monter la cage thoracique. L’expiration peut être due aux muscles intercostaux internes qui vont provoquer un basculement des cotes vers le bas.
Remarque : Pour l’inspiration et l’expiration, il existe des muscles annexes.
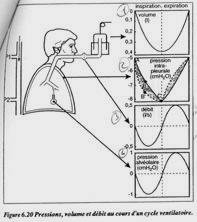
En haut (1), on a un enregistrement schématique spirométrique.
En 3, on enregistre le débit. En 4, on mesure la pression dans les alvéoles (la courbe de débit suit la courbe de pression dans les alvéoles). En 2, on a la pression intrapleurale : cette pression est estimée car elle est non mesurable ; en général, on prend la pression oesophagienne comme pression de référence. Cette pression intrapleurale est toujours négative. Pendant l’inspiration, la pression pulmonaire fait diminuer la pression intrapleurale. A l’expiration, la pression intrapleurale remonte jusqu’à retrouver sa valeur normale (en expiration passive).
Dans le cas de l’expiration active, la pression intrapleurale peut devenir positive.
Les traits pleins sont les valeurs obtenues en phase statique.
Les traits pointillés sont les valeurs obtenues en phase dynamique. Dans ce cas, il faut vaincre la force élastique mais aussi la résistance à l’écoulement.
3 Les « résistances » à vaincre.
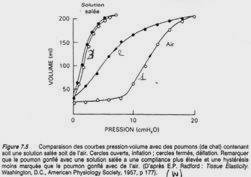
Cette expérience est faire sur un poumon isolé.
On rempli le poumon en envoyant de l’air.
La courbe 1 permet de mesurer la compliance pulmonaire. La courbe 2 est la courbe d’expiration : elle est complètement différente de la courbe 1 : c’est un hystérésis.
La courbe 3 est obtenue en remplissant un poumon avec de l’eau tamponnée : la compliance pulmonaire devient très supérieure au cas avec l’air. A courbe 4 montre que l’hystérésis, avec l’eau tamponnée, tend à disparaître.
 Pour vaincre le remplissement, il n’y a pas que l’élasticité vaincre !
Pour vaincre le remplissement, il n’y a pas que l’élasticité vaincre !
Dans le cas 1, on observe des force de tension superficielle : le travail pulmonaire sert à vaincre ces forces de tension.
La tension superficielle est la différence entre les deux courbes.
Les forces de tension superficielles.
On connaît des modèles d’étude de ces forces de tension : la bulle de savon, un gaz dans un liquide.
La pression est égale à deux fois la tension superficielle à l’interface, divisée par le rayon (P = 2T/r).
Si la tension est constante, cette formule nous donnerait des petites alvéoles avec une pression supérieure à la pression des grandes alvéoles. (à fonctionnement du système respiratoire impossible).
Il faut donc que la tension varie : cette variation est le rôle du surfactant.
4 Le surfactant pulmonaire.
· Propriétés :
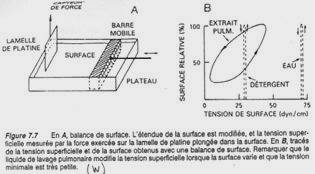
Sans surfactant, le nouveau né ne peut respirer : le surfactant fait chuter la tension superficielle.
Le récipient a une surface variable (une des faces est mobile).
Pour l’eau, une modification de surface ne modifie pas la tension superficielle.
Avec un produit tensio-actif, la tension superficielle devient inférieure à la tension superficielle de l’eau (pas de rapport avec la surface).
Avec des extraits pulmonaires, la tension superficielle est bien inférieure à celle de l’eau et devient dépendante de la surface.
La tension de surface est plus forte à l’augmentation de surface que oos de la diminution.
 Le surfactant permet donc de réduire la tension superficielle.
Le surfactant permet donc de réduire la tension superficielle.
· La tension dépend de l’étirement des surfaces
· Le surfactant est responsable de l’hystérésis.
Le surfactant se dépose en film à la surface des alvéoles ou de l’eau.
Dans ce surfactant, on a des phospholipides (85%) et des protéines (15%). Ce sont ces phospholipides différents de ceux des membranes.
Parmi les protéines, on trouve la SPA, la SPB, et la SPC. La SPA semble avoir un rôle structural (permet de dessiner le réseau). Elle est appelée myéline tubulaire quand elle est sous sa forme de stockage extracellulaire. Elle permet de faire venir des molécules dans le film.
85% des phospholipides sont recyclés par les pneumocytes 2. Les 15% restant sont perdus. Il y a quand même un gros recyclage des phospholipides.
La SPA stimule aussi les fonctions macrophagiques dans le poumon :
- Au niveau des bronches, le surfactant se mêle au mucus et va former deux phases dans le mucus bronchique. Il se fait un film au dessus du mucus, ce qui empêche ce dernier de s’évaporer.
5 Les variations régionales de la ventilation.
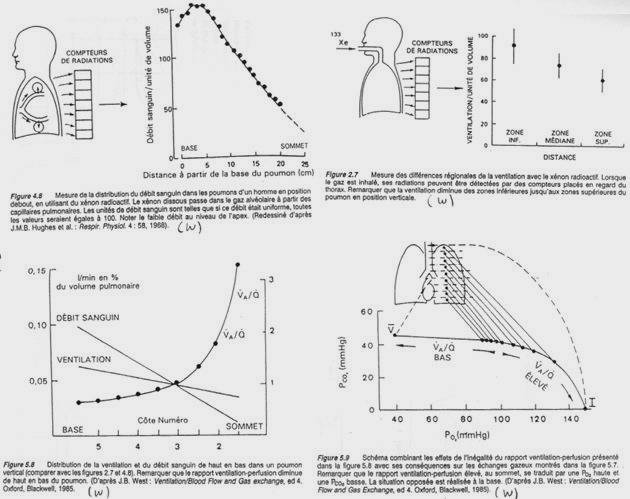
Dans le poumon, la ventilation n’est pas du tout homogène.
L’inspiration de xénon 133 à un sujet permet de voir le fonctionnement des poumons. Le sujet ayant respiré ce xénon va être placé devant un compteur de radioactivité.
La zone supérieure des poumons reçoit moins de xénon : il y a donc une moins bonne ventilation et cela, à cause du poids du poumon.
Si le sujet est couché, on ne voit pas de différence entre le bas et la haut des poumons mais entre la face dorsale et la face ventrale.
En position debout, les alvéoles du haut (à l’apex) ont une compliance faible.
L’irrigation des poumons est aussi hétérogène.
6 Composition du gaz alvéolaire.
Les composants du gaz diffusent selon les pressions partielles et non selon les concentrations. (N2 = 79% ; O2 = 21%). PB = 760mmHg (au niveau de la mer).
PO2 (mer) = 0.21 * 760 = 160mmHg
PN2 (mer) = 0.79 * 760 = 600mmHg
Un élément à ne pas ajuter est la vapeur d’eau : dans les alvéoles, on est toujours à 37°C à 100% de saturation d’eau.
La pression de vapeur d’eau de l’air à 37°C saturée d’eau est de 47mmHg (PH2O = 47mmHg).
PA(CO2) + PA(O2) + PA(N2) + PA(H2O) = PB. (760mmHg si l’on est au bord de l’eau)
L’azote prend la place disponible et donc, n’est pas à la même pression qu’à l’extérieur.
La composition de l’air alvéolaire ne change pas : la ventilation assure le renouvellement quand l’O2 est consommé et quand du CO2 est produit.
 L’air alvéolaire est seulement renouvelé entre 10 et 12% ! Ce faible renouvellement sert à ne pas faire d’à-coups et permet aussi de garder une composition constante.
L’air alvéolaire est seulement renouvelé entre 10 et 12% ! Ce faible renouvellement sert à ne pas faire d’à-coups et permet aussi de garder une composition constante.
E Contrôle de la ventilation.
En fait, la ventilation se déroule en trois temps.
Pour la contraction du diaphragme, on observe une phase pendant l’inspiration. A l’expiration qui suit, on a un relâchement progressif (frein). A la seconde expiration, le relâchement est total.
L’activité nerveuse :
Pendant l’inspiration, l’activité du nerf phrénique augmente.
Durant PI, l’activité va diminuer.
Durant E-2, l’activité est nulle et les nerfs intercostaux peuvent être activés.
1 Chez les mammifères.
a L’automatisme respiratoire.
On trouve 6 familles de neurones.
Le contrôle est automatique, neurogène (siège nerveux dans le système nerveux central). Sur cet automatisme vient se greffer des influences :
- Influences volontaires (corticales).
- Influences chimiques : adaptations aux besoins (O2, CO2).
- Influences mécaniques : toux, éternuements.
- Influences par les afférences venant du poumon lui-même.
b Les chémorécepteurs.
Les chémorécepteurs sont des structures sensibles au pH, à l’O2…
Expérience 1 :
Pour voir l’action des chémorécepteurs, on fait :
- respirer un mélange de plus en plus pauvre en O2. à La PAO2 va diminuer et le sujet va donc augmenter sa ventilation (si la PAO2 devient inférieure à 60mmHg).
- respirer un mélange de plus en plus riche en O2. Le sujet ne change pas sa ventilation.
En dessous de 60mmHg, la ventilation peut s’accroître jusqu’à 25L/minute. Plus le sujet ventile, plus la PACO2 va chuter. On ne fait donc pas que varier la PAO2.
Expérience 2 :
Si l’on maintien la PACO2 constante, on voit que l’hyperventilation arrive dès 100mmHg.
L’Homme est très sensible à l’excès de CO2 et, moins il y a d’O2, plus on y est sensible.
Cette sensibilité est due aux chémorécepteurs situés dans le système artériel et centraux :
- Pour les chémorécepteurs du système artériel, on voit qu’ils ne sont pas situés dans la paroi des artères : ils forment les glomus. Les glomus sont situés sur les carotides, sur l’aorte et placés près des zones barosensibles.
- Les glomus sont de petits organes proche des artères, très richement irrigués. On trouve aussi dans ces organes des terminaisons nerveuses sensitives. Ils sont sensibles à des baisses de PO2, des augmentations de PCO2 et des chutes de pH. A la surface de ces cellules, on trouve des protéines membranaires à structure de cytochrome, non identifiées pour l’instant. C’est cette protéine qui « mesure » la PO2. Quand la PO2 chute, il y a stimulation qui libère du Ca2+. Le Ca2+ entraînera la sécrétion de dopamine qui stimule le nerf.
- On pense que toutes les cellules devraient posséder cette protéine.
c Les chémorécepteurs centraux.
Une injection d’HCl très dilué dans le cerveau provoque une augmentation de la ventilation : ce sont les neurones du bulbe rachidien qui sont sensibles au pH.
Le liquide céphalo-rachidien, comme le liquide interstitiel, n’a pas de protéines : il est donc mal tamponné. Par conséquent, une augmentation de CO2 entraînera la formation de H+ qui ont un effet sensible : une faible augmentation de la PCO2 aura un effet en premier lieu au niveau du système nerveux central.
2 Chez les poissons.
Le principe du fonctionnement est identique. Ce qui change principalement est que les poissons sont sensibles à l’hypoxie, à la concentration en O2.
On a mis en évidence une forte sensibilité périphérique à l’hypoxie. Les organes des sens sont dans l’épithélium branchial :
- ils voient la diminution de la PO2 de l’eau
- et voient la diminution de PO2 dans le sang.
 Les poissons peuvent anticiper leur comportement en fonction de la PO2 de l’eau. Ils ne sont pas sensibles au CO2. En effet, l’eau va accepter beaucoup de CO2 en solution alors qu’elle n’accepte que peu d’O2.
Les poissons peuvent anticiper leur comportement en fonction de la PO2 de l’eau. Ils ne sont pas sensibles au CO2. En effet, l’eau va accepter beaucoup de CO2 en solution alors qu’elle n’accepte que peu d’O2.
Le quotient respiratoire (r) est de 0,85.
Dans le poumon, si la ventilation diminue, la PO2 va chuter et la PCO2 va augmenter.
Dans la branchie, si la ventilation diminue beaucoup (donc, PO2 atteint presque 0), la PCO2 atteint à peine 5mmHg è le CO2 diffuse très facilement dans l’eau.
II Le transport des gaz respiratoires.
A La circulation pulmonaire.
1 Comparaison avec la circulation systémique.
La pression dans la circulation pulmonaire est bien inférieure à la pression de la circulation systémique.
La pression péricapillaire est variable. Ceci va modifier la pression intramurale.
Les muscles lisses de la circulation pulmonaire ont une perméabilité inverse à l’O2. Dans le poumon, à l’inverse des autres organes, l’hypoxie provoque la vasoconstriction (vasoconstriction hypoxique).
Normalement, le poumon sature le sang d’ O2. Si un poumon est hors service, le sang qui y va ne sera pas saturé d’ O2 et en se mélangeant, cela posera de gros problèmes. Pour empêcher cela, il y a la vasoconstriction hypoxique.
La résistance de la circulation pulmonaire est variable.
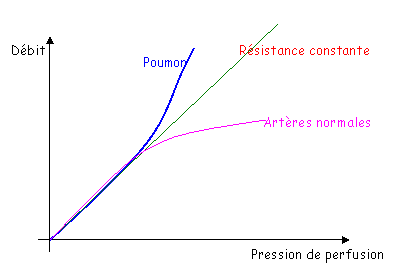
 On voit que la résistance diminue.
On voit que la résistance diminue.
En réalité, deux phénomènes sont responsables de cela :
- Des capillaires inutilisés, quand la pression augmente, vont être utilisés.
- Il y a distension des capillaires qui, lorsque la pression augmente, voient leur diamètre augmenter.
2 L’hétérogénéité de la perfusion pulmonaire
Cette hétérogénéité est mise en évidence par l’injection de xénon 133 dans la circulation sanguine. Ce produit va être éliminé par les poumons en fonction de la proportion de la perfusion pulmonaire.
 C’est à la base du poumon que l’on trouve le plus de radiation : la base reçoit plus de sang que le sommet (grâce à la faible pression du système). Au final, ce qui compte est que la partie haute du poumon est mal irriguée et mal ventilée alors que la partie basse est bien irriguée et bien ventilée.
C’est à la base du poumon que l’on trouve le plus de radiation : la base reçoit plus de sang que le sommet (grâce à la faible pression du système). Au final, ce qui compte est que la partie haute du poumon est mal irriguée et mal ventilée alors que la partie basse est bien irriguée et bien ventilée.
3 Ventilation – Perfusion.
Les pentes des deux courbes ne sont pas identiques : le rapport entre ventilation et perfusion est donc différent, plus important au sommet qu’à la base.
La conséquence de ce phénomène est que si le rapport est élevé, on trouvera beaucoup d’O2 et peu de CO2, et que si le rapport est faible, on aura de faibles taux de renouvellement, donc, une pauvreté en O2 et une richesse en CO2.
 On voit bien que le comportement du poumon n’est absolument pas homogène. Selon la position (allongé, debout…), on observera des ventilations différentes.
On voit bien que le comportement du poumon n’est absolument pas homogène. Selon la position (allongé, debout…), on observera des ventilations différentes.
B Le transport de l’oxygène.
Pour ce transport, on notera la mise en jeu de nombreux pigments respiratoires.
1 Nature chimique et localisation des pigments respiratoires.
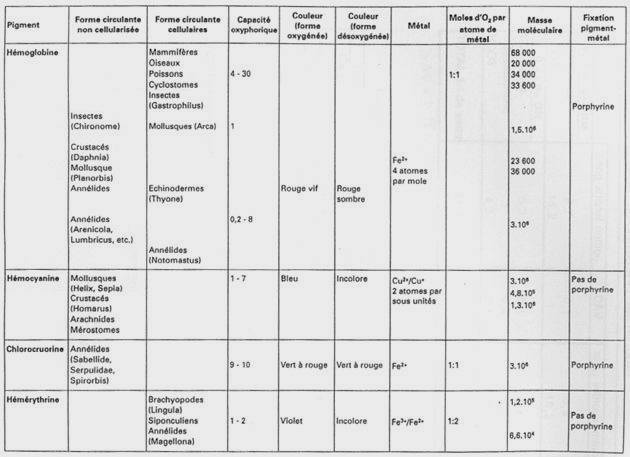
· Les pigments héminiques.
Ces pigments contiennent un hème (un hème entouré de 4 cycles pyroles).
On peut citer, pour exemple, la Chlorocruorine, trouvée chez certains annélides.
· Les pigments hémérythrines.
Ces pigments montrent un atome métallique non inclus dans un hème.
On retrouve ce pigment chez divers animaux comme les brachiopodes, des annélides. Les hémérythrines se trouvent toujours dans des cellules.
· Les hémocyanines.
Ces hémocyanines sont toujours des pigments extracellulaires. On les trouve chez les scorpions, certains mollusques, où ils forment des molécules géantes. Par comparaison, on va retrouver des molécules géantes d’hémoglobine chez certains annélides.
 Il faut que les molécules soient concentrées pour bien fixer l’O2, ainsi que pour ne pas faire augmenter la pression oncotique.
Il faut que les molécules soient concentrées pour bien fixer l’O2, ainsi que pour ne pas faire augmenter la pression oncotique.
Un pigment emballé permet de bien maîtriser son environnement afin, entre autre, de faire varier son affinité pour les substrats.
2 Propriétés de l’hémoglobine des vertébrés.
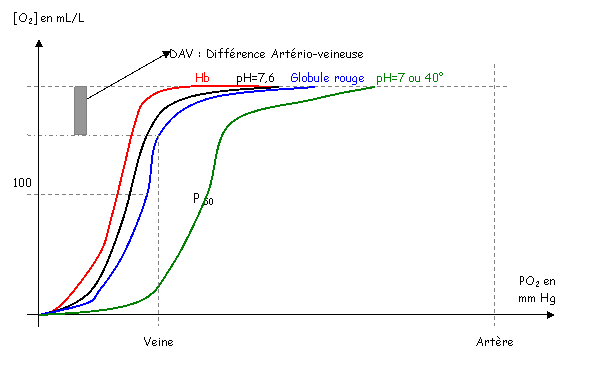
On va observer une coopérativité entre les sites car l’on est en tétramères. La saturation est obtenue quand le pigment ne peut plus recevoir de produit, qu’il est à saturation.
P50 = pression de demie saturation.
Les ¾ d’O2 restant sont une réserve facilement exploitable, sans besoin d’augmentation de débit cardiaque. Si l’on fait l’expérience avec une solution d’hémoglobine, la forme libre aura une affinité trop forte è il y a donc dans les globules rouges, une molécule qui permet de diminuer l’affinité de l’hémoglobine pour l’O2. Le DiPhosphoGlycérate est chez les mammifères la molécule en question. Chez les poissons, ce sont les molécules d’ATP et de GTP qui joueront ce rôle.
 Ces molécules permettent de moduler l’affinité en fonction des milieux, des besoins.
Ces molécules permettent de moduler l’affinité en fonction des milieux, des besoins.
Les globules rouges de mammifères fonctionnent en anaérobie (à l’intérieur) car il n’y a pas d’organite à l’intérieur.
Ces courbes sont observées pour des conditions « standards » (pH 7,4 ; Température 37°C).
Si l’on acidifie le milieu, la courbe est déplacée sur la droite : l’affinité pour l’O2 diminue, ce qui améliore la distribution de l’O2 aux tissus actifs.
C’est ce que l’on appelle « l’effet Bohr ».
Si le pH est alcalin, la courbe sera déplacée vers la gauche et les effets seront une augmentation de l’affinité pour l’O2.
On remarquera, par expérimentation, qu’une augmentation de température a les mêmes effets que l’acidification du milieu (effet Bohr).
3 Adaptation de l’hémoglobine au milieu de vie.
Attention, il faut bien dissocier les deux notions d’adaptation et d’acclimatation.
Les animaux vivant dans des milieux pauvres en O2 ont une hémoglobine de forte affinité.
Pour l’acclimatation :
L’hémoglobine d’une espèce peut avoir une affinité différente selon le milieu où elle se trouve.
Dans le cas des poissons, il n’y a aucun problème.
Pour les mammifères, (hors Lama, qui est adapté), on observe une chute de l’affinité (inversement pour le lama)
4 Quelques mots de la biologie des hématies.
La diminution de la quantité de globule rouge entraîne l’augmentation de la libération d’EPO, qui va agir à de nombreux endroits où l’érythropoïèse a lieu.
Le stade « réticulocyte » est le stade qui précède le stade « hématie » : en fait, on observe des organites, de l’ARN… Au bout de 24 heures, ces organites divers vont être expulsé, ce qui donne le stade « hématie ». La vie de ces dernières est environ de 120 jours.
Le cycle est anaérobie car il n’y a pas de mitochondrie : la glycolyse est obligatoire.
L’hémoglobine a un fer ferreux (Fe2+) ; à l’état de sursaturation en O2, Fe2+ à Fe3+ è MetHb (met-hémoglobine) qui est inactive. L’enzyme de conversion de Fe3+ en Fe2+ est la diaphorase ou MetHb réductase.
Lorsque l’hématie meurt, il va y avoir dégradation de l’hémoglobine par le foie mais le fer hémique est recyclé par les macrophages. On est face à une grande régulation du fer.
C Transport du CO2.
Il existe des différences entre le CO2 transporté dans le courant sanguin et le CO2 échangé au niveau tissulaire.
1 Les « formes » transportées.
Une partie reste dissoute (CO2 gazeux dans un liquide).
Quand cette forme passe dans le globule rouge, le CO2 s’hydrate grâce à l’anhydrase carbonique (à HCO3-)
Dans le poumon, le HCO3- revient dans les hématies, mais là, ce sera du CO2 qui sera expulsé.
Le CO2 dissout représente 5%. La forme HCO3- représente les deux tiers du CO2 transporté.
Cette enzyme, l’anhydrase carbonique, est intra-érythrocytaire. Quand le HCO3- est formé, il sort par une protéine (bande 3) qui permet un antiport HCO3- (vers l’extérieur)/Cl- (vers l’intérieur). Le HCO3- arrive finalement dans le plasma.
On trouve aussi du CO2 participant à la formation de carbamines : CO2 + fonction amine d’une protéine.
Hb-NH2 + CO2 ó Hb-N(-H)-COOH.
La carbamine majoritaire est l’hémoglobine.
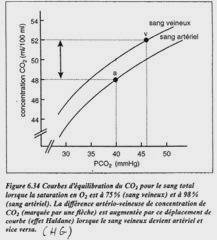
Il s’agit de la concentration totale en CO2 (somme des trois formes).
On observe ainsi deux courbes différentes selon la concentration en O2 (Effet Aldal), avec du sang pauvre en O2, et une pression en CO2 (PCO2) de 40 mm Hg.
Si l’on retire de l’O2, le sang va accepter de plus en plus de CO2. L’effet Aldal permet de doubler la quantité de CO2 dégazé.
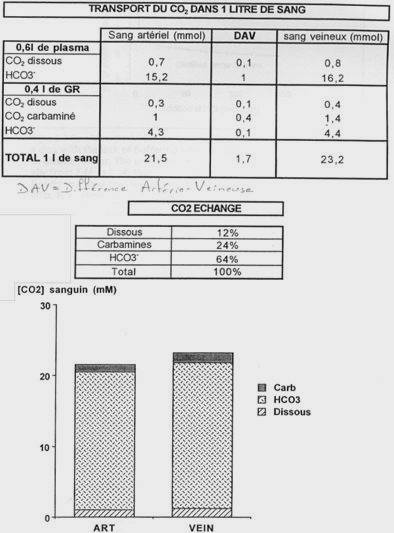
Transport du CO2 dans un litre de sang.
Pour le sang veineux, HCO3- est la forme la plus importante. On la retrouve surtout dans le plasma et peu dans les hématies.
2 Le CO2 échangé.
Les carbamines jouent un rôle dans ces échanges. L’hémoglobine set à cette sortie. Hémoglobine-O2 réagit moins bien que la forme Hémoglobine pour faire des carbamines.
En arrivant dans le tissu, Hémoglobine-O2 arrive, de l’O2 est libéré, donc, on l’hémoglobine qui réagit avec le CO2 et forme l’hémoglobine-CO2.
Une fois dans le poumon, la forme hémoglobine-CO2 va libérer le CO2 pour prendre de l’O2.
L’effet Aldal n’est pas que sous le contrôle des carbamines.
Quand l’hémoglobine fixe l’O2, elle perd son pouvoir tampon : quand l’hémoglobine-O2 arrive dans un tissu, l’O2 est normalement libéré, puis, l’hémoglobine s‘associe de la façon suivante :
CO2 + H2O à (anhydrase carbonique) HCO3- + H+ à Hémoglobine-H
Cette forme couplée à l’hydrogène favorise le transport d’HCO3-
Hémoglobine-H + O2 à Hémoglobine-O2 + H+ (+HCO3-) à CO2 + H2O
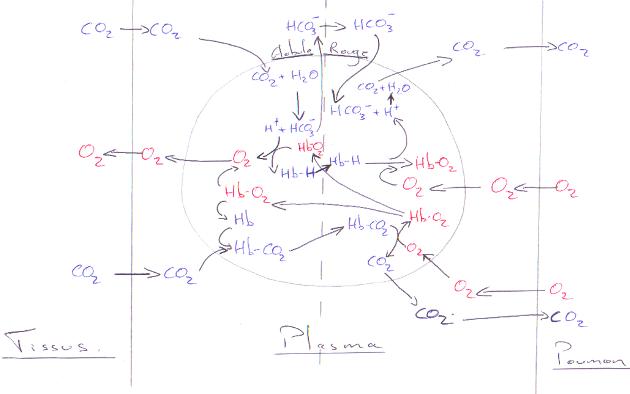
IV Ventilation et pH sanguin.
Deux organes sont chargés de réguler le pH sanguin : les poumons et les reins.
Dans l’organisme, divers produits peuvent assurer un pH stable. Le principal tampon trouvé est : H2CO3/HCO3- (ou bien le couple CO2/HCO3-).
pH = 6.2 + log ([HCO3-]/[CO2(g)])
6.2 est une constante.
Le poumon règle la concentration en CO2. La concentration en HCO3- est régulée par le rein.
Le poumon peut corriger un déséquilibre mais peut aussi être à l’origine d’un déséquilibre.
1 Acidose métabolique.
Les protons qui arrivent se tamponnent avec le HCO3- et vont ainsi former du CO2 gazeux.
La réaction de l’organisme à cela est le déclenchement d’une hyperventilation qui va encore soustraire des ions H+, mais aussi des ions HCO3-, ce qui va utiliser les réserves en HCO3-.
2 Acidose d’origine respiratoire.
On se place dans le cas d’une insuffisance respiratoire.
Le CO2 va s’accumuler et créer une acidose respiratoire. L’accumulation de protons se fait par le rein, puis, par sécrétion de H+ ou par production de HCO3-.
Selon chaque animal, il faut garder le rapport [HCO3-]/[CO2(g)] a peu près constant, quelle que soit la concentration en CO2 : du HCO3- doit alors être sécrété ou produit selon les cas.
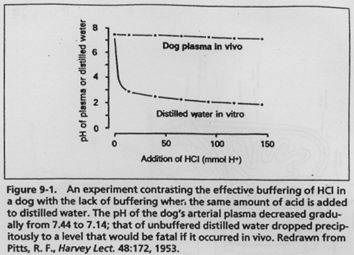
Ceci est une expérience théorique :
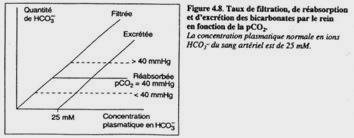
La réabsorption dans le rein est sensible à la PCO2.
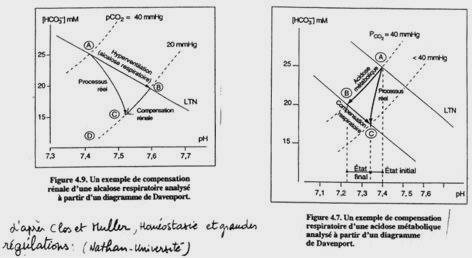
A droite : Il y a compensation ventilatoire d’une acidose métabolique (de A vers B). S’il y a hyperventilation, de plus en plus de protons vont être éliminés mais la concentration en HCO3- sera toujours trop faible (en C).
A gauche : on observe ici une alcalose repiratoire. Il y a élimination de CO2 et donc, de moins en moins de H+ et de HCO3- seront disponibles. La conséquence est que le rein diminue sa réabsorption de HCO3-, ce qui permet un retour vers un pH un peu plus acide.
Chapitre 4 :
La Fonction Rénale.
I Introduction et présentation générale.
A Fonctions essentielles du rein.
1 Maintien de la composition du milieu interne.
Chez un sujet normal, le milieu intérieur dans lequel baignent les cellules, a une composition constante. Les électrolytes et l’eau apportées par l’alimentation sont absorbées par le tractus digestif et tendent à modifier ce milieu intérieur.
Les reins vont éliminer les surplus (en eau et électrolytes), de façon à maintenir un volume et une composition constante.
 Les reins maintiennent donc un bilan nul pour l’eau et les substances dissoutes.
Les reins maintiennent donc un bilan nul pour l’eau et les substances dissoutes.
2 Excrétion des produits de dégradation du métabolisme cellulaire et des substances étrangères.
Les produits dérivés du métabolisme cellulaire qui n’ont pas de fonction connue doivent être éliminés (passer dans l’urine).
Par exemple : les acides, l’urée, l’acide urique (métabolisme des purines), la créatinine (provient de la créatine musculaire), la bilirubine et divers autres métabolites comme les dérivés de l’hémoglobine ainsi que des hormones à l’état de traces.
On trouve aussi des substances étrangères (xénobiotiques) qui y sont présentes et qui peuvent être toxiques ou thérapeutiques.
Par exemple, l’urée (O=C(-NH2)-NH2) a été la première molécule organique a être synthétisée, vers 1850, par Wholer (Suisse).
Beaucoup d’hormones ont été extraites à partir de quantités considérables d’urine.
3 Régulation de la pression artérielle systémique.
Le rein participe à cette régulation de deux manières :
- Par un contrôle du volume plasmatique (un des déterminants de la pression artérielle) et celui du volume extracellulaire, en ajustant les sorties des Na (sodium) aux entrées.
- Par la production d’une enzyme, la rénine, qui circule dans le sang et permet la mise en action d’un puissant agent vasoconstricteur qui intervient dans la régulation de la pression artérielle : l’angiotensine 2.
4 Fonction endocrine du rein.
On peut distinguer deux fonctions endocrines assurées par le rein.
Il va produire un métabolite de la vitamine D : le 1,25(OH)2D3. C’est une hormone qui contrôle l’absorption digestive du Ca (calcium) et qui intervient dans le métabolisme osseux.
Il produit également 90% de l’EPO (érythropoïétine).
B Compartiments liquidiens et échanges.
1 Compartiments liquidiens.
a L’eau totale.
L’eau représente en moyenne 60% du poids du corps. Cette valeur est plus importante chez le jeune, moins importante chez les personnes âgées. Chez la femme, le pourcentage est moindre, à cause de la quantité de tissu adipeux.
Pour une personne de 70kg, on va trouver 42 litres d’eau.
b L’eau du compartiment liquidien.
Ce volume est assimilé à 1/3 de l’eau totale (soit environ 14 litres). Cette eau est divisée en deux liquides :
· liquide interstitiel (80% soit 11,2 litres)
· plasma (20% soit, 2,8 litres).
Le cation prédominant est le sodium (Na) et les anions majoritaires sont Cl- et HCO3-.
c L’eau du compartiment intracellulaire.
Cette eau représente les 2/3 de l’eau totale (28 litres). Les cations prédominants sont le K+ et le Mg2+ ; pour les anions, on va trouver les phosphates organiques et les protéines.
Cette eau est très hétérogène selon les tissus.
On peut mesurer ces compartiments liquidiens par une méthode de dilution à partir d’indicateurs colorés. Le « bleu Evans » permet de mesurer le plasma.
On a aussi d’autres méthodes utilisant la radioactivité ou la chaleur.
2 Les masses échangeables.
Une part faible des électrolytes est bloquée par des liaisons chimiques dans les tissus. La grande partie est soumise à des échanges rapides (c’est la masse échangeable).
Le sodium échangeable : 90% dans le liquide extracellulaire ; 5% dans le liquide intracellulaire ; 5% dans les tissus conjonctifs.
Le potassium échangeable (K) : 98% dans le liquide intracellulaire ; 2% dans les liquides extracellulaires.
3 Mouvements d’eau et de substances dissoutes.
L’entrée se fait à travers l’endothélium capillaire, et ces échanges sont connus sous le nom de « loi de Starling », avec deux forces opposées mises en jeu :
- la pression hydrostatique (ou sanguine). Son sens est du plasma vers le milieu interstitiel
- la pression osmotique qui va en sens inverse.
A titre de bilan, au niveau des capillaires, 20 litres d’eau sortent du système vasculaire vers le système interstitiel. Seuls 18 litres font le trajet de retour. Les deux litres restant rejoignent indirectement le système des capillaires puis les vaisseaux lymphatiques.
II Physiologie du glomérule.
Cf. pages 52, 73, 74, 77.
Corpuscule (rénal) = Glomérule de Malpighi + Corpuscule.
Quelques valeurs :
- Débit sanguin rénal (DSR) : 1 litre par minute (103mL), soit 20% du débit cardiaque. On a donc 1440 litres qui passent dans les reins chaque jour (/24heures).
- Débit plasmatique rénal (DPR) : 600 mL/min, soit 864L/24h
- Débit de filtration glomérulaire (DFG) : 125mL/min, soit 180L/24h. La fraction filtrée (FF) est le rapport entre DFG sur DPR, soit environ 20%.
- Débit urinaire (DU) moyen : 1mL/min, soit 1,44L/jour.
- Les éléments figurés ne sont pas concernés par la filtration.
A Le filtrat glomérulaire ou urine primitive.
1 Composition.
Le filtrat glomérulaire correspond à du plasma pratiquement sans protéine. Les traces autorisées de protéines dans l’urine sont de 10 à 20mg/L alors que le plasma contient environ 70g/L.
Dans cette urine primitive, on trouve des substances dissoutes non ionisées comme l’urée ou le glucose, qui traversent librement, mais aussi des substances ionisées (anions et cations) et d’autres substrats de petite taille.
A ce niveau, des éléments du sang sont liés aux protéines et ne peuvent passer la barrière glomérulaire (médicaments, hormones, lipides).
2 « Barrière » glomérulaire et macromolécules.
La barrière glomérulaire est assimilée à un filtre. On y trouve les pores de l’endothélium fenestré (Lamina fenestrata) dont le diamètre moyen est de 0,1 micron.
Par ailleurs, il y a la structure générale de la membrane glomérulaire, avec les podocytes et les pédicelles (Capsule de Bowman) qui forment des fentes de filtration de 7nm.
Pour passer ce filtre, différentes caractéristiques seront exigées :
- taille de la molécule (Poids moléculaire), par exemple, les albumines (70 000Da) sont les plus grosses molécules à pouvoir passer ;
- charge électrique : les molécules de poids moléculaire faible, mais chargées négativement passent mal la membrane glomérulaire car celle-ci a un charge négative.
Ces caractéristiques ont été mises en évidence grâce à une molécule de taille et de charge variable : le Dextran.
On doit citer le problème de protéines et de leur présence problématique dans les urines : protéinurie ou albuminurie. Le taux normal de protéines est inférieur à 0,15g/24heures. Au-delà, la présence de protéines dans l’urine est pathologique.
Quelques explications à ce phénomène :
· La diminution du DSR : il y a contact plus prolongé entre l’albumine plasmatique et la barrière glomérulaire. Ce phénomène peut être due à des exercices musculaires violents, des états fébriles, des insuffisances cardiaques.
· L’augmentation pathologique de la perméabilité de la membrane glomérulaire aux albumines. Cet accroissement peut être observé à cause d’hypertension prolongée et de glomérulopathies (seul cas où l’urine contient des lipides).
3 Déterminants ou facteurs de la filtration glomérulaire (FG).
La filtration glomérulaire est un phénomène passif. On appelle Pression Nette de Filtration (ou PNF) è PNF = PS – (PC + PO) (PC = Pression Capsulaire).
ó 6,65 – (1,33 + 4,00) = 1,32 KPa
PNF = ΔP – σΔπ = 50 – 10 – 30 = 10mmHg
ΔP est la différence de pression hydrostatique entre les capillaires glomérulaires et la capsule de Bowman.
Σ est le coefficient d’extraction qui est déterminé par la perméabilité aux protéines dans le filtre glomérulaire à σ est voisin de 1.
Δπ est la différence de pression coloïdo-osmotique. Cette différence est associée à l’équilibre de Donnan et tend à retenir l’eau et les électrolytes (ou osmolytes) dans la capsule de Bowman.
L’équilibre de Donnan équivaut à une inégale répartition des solutés ioniques entre deux compartiments liquidiens de l’organisme, associée à l’inégale concentration en gros anions non perméants (protéines).
1mm de Hg équivaut à 0,133KPa
La formule globale montre qu’il s’agit d’un système dynamique qui varie selon la longueur des capillaires des glomérules.
Le ΔP varie peu en diminuant; Δπ augmente progressivement car, comme la barrière glomérulmaire est perméable aux protéines, elles se concentrent dans les capillaires au fur et à mesure que se développe la filtration glomérulaire.
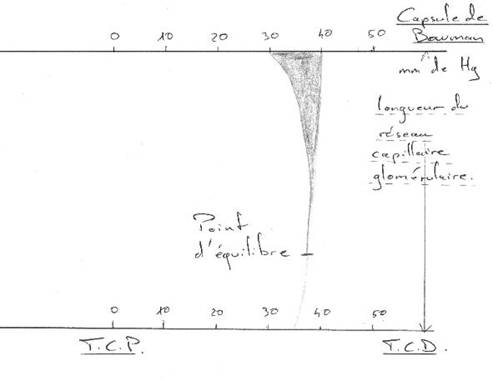
En gris, on a la zone de PNF (Pression Nette de Filtration). ΔP diminue peu (d = 40 à 35). Δπ augmente à partir de 30 mmHg et, arrivé au 2/3 de la longueur du capillaire artériel glomérulaire, elle rejoint ΔP (point d’équilibre) è La filtration glomérulaire n’exploite pas la totalité de la surface capillaire du glomérule.
4 Facteurs influençant la DFG (Débit de filtration glomérulaire).
a Débit Plasmatique Rénal (DPR).
Ce débit est un facteur important pour le DFG, par exemple, si le DPR croit, on va avoir un DFG qui croit à son tour.
b Résistances artériolaires.
On envisage une vasoconstriction de l’artériole afférente. Il y a :
- résistance à l’écoulement,
- diminution du DPR,
- diminution de la pression hydrostatique capillaire.
 Les deux derniers facteurs dont une diminution du débit de la filtration glomérulaire (DFG).
Les deux derniers facteurs dont une diminution du débit de la filtration glomérulaire (DFG).
c Pression artérielle systémique.
Cette pression varie entre 80 et 160 mmHg. Malgré cette variation, le DSR ne varie pas et le DFG reste stable. Mais, si la pression artérielle devient inférieure à 80 mmHg, il va y avoir une diminution du DSR et du DFG.
d Autres déterminants.
Une obstruction aigue, ou incomplète des voies urinaires va provoquer une augmentation de la pression hydrostatique dans la capsule de Bowman. La conséquence de cette augmentation de pression est une diminution du DFG.
III Régulation du Débit Sanguin Rénal (DSR) et du Débit de Filtration Glomérulaire (DFG).
A Facteurs influençant le DSR et le DFG.
1 Contrôle nerveux.
Les vaisseaux du rein reçoivent une riche innervation par le système orthosympathique qui permet l’action de vasoconstriction avec diminution du DSR. Toutefois, le DFG va diminuer peu car l’action du système orthosympathique porte surtout sur l’artériole afférente, ce qui maintient une différence de pression.
2 Contrôle hormonal.
a Le système Rénine-Angiotensine.
La rénine est une enzyme protéolytique sécrétée par les cellules granulaires de l’appareil juxta-glomérulaire (puis, passage dans le sang).
On trouve la séquence classique :
Angiotensinogène à Angiotensine (décapeptide) grâce à l’action de la rénine à Angiotensine 2 grâce à l’action d’une convertase, présente dans les cellules épithéliales. Le dernier produit formé a une action de vasoconstriction.
Remarque : il y a passage de la forme Angiotensine 2 à la forme Angiotensine 3.
L’angiotensinogène est un précurseur inactif de type protéine globuline, hépatique.
La vasoconstriction observée est principalement localisée dans l’artériole afférente et va provoquer une chute du DSR et à un degré moindre, une chute du DFG.
La rénine est sécrétée quand le rein est mal irrigué : quand la pression artérielle chute et que cette chute est perçue par les cellules granulaires, ce qui va stimuler des fibres du système orthosympathique, puis stimuler des cellules de la Macula Densa qui sont des réceptrices de la composition en Na+ dans le tube contourné distal.
b L’ensemble des prostaglandines.
Les prostaglandines sont synthétisées dans le rein, au niveau des tubes collecteurs. A leur origine, on trouve l’acide arachidonique modifié par l’action de la cyclo-oxygénase.
Ici, on trouve PGL1.
L’action de cette molécule est une vasodilatation.
c L’ensemble des kininogènes.
Kininogène à BradyKrinine (grâce à la Kallicréine)
Précurseur inactif peptide synthétisée par les cellules du TCD
La Bradykinine a une action vasodilatatrice et va donc faire croître et le DSR et le DFG.
d Malpighi ou Facteur Atrial Natriurétique.
Malpighi est un peptide sécrété par les myocytes cardiaques de l’oreillette, lorsque celle-ci est trop dilatée. Son action est vasodilatatrice
C’est un facteur inverse à celui de l’hémorragie.
 On peut voir que ces trois familles de produits ont une action antagoniste à l’angiotensine
On peut voir que ces trois familles de produits ont une action antagoniste à l’angiotensine
B Autorégulation du DSR et du DFG.
Les travaux ont été réalisés sur des reins isolés et perfusés (sans innervation), mais avec l’action d’hormones. Seule la pression de perfusion sera changée.
La variation va être comprise entre 80 et 160 mmHg, alors que les variations de DSR et de DFG vont être très faibles.
Deux mécanismes sont proposés pour expliquer ce phénomène.
1 Mécanisme myogénique.
Si on augmente le débit de perfusion, on provoque un étirement de la paroi vasculaire de l’artériole afférente. Il y a alors immédiatement une vasoconstriction et une diminution du diamètre de celle-ci. Le DSR reste ainsi à peu près constant.
2 Rétrocontrôle tubulo-glomérulaire.
Ce rétrocontrôle est un mécanisme au niveau de chaque néphron. Ici, le DSR et le DFG de chaque néphron seront sous le contrôle des variations de débit et de la composition du fluide tubulaire, au niveau de la macula densa, après l’anse de Henlé.
Ces mécanismes sont toujours mal connus.
3 Adaptations aux variations de la volémie3
a Régime sans sodium.
Si ce régime est modéré et chronique, on assiste à une hypovolémie de l’ordre de 5%, et donc, à une chute du retour veineux, du retour cardiaque et de la pression artérielle.
On a diverses réactions possibles de l’organisme :
- stimulation des barorécepteurs artériels de la crosse aortique et des carotides
- stimulation du système orthosympathique
- stimulation de l’artériole afférente qui va produire la rénine, et donc, une vasoconstriction.
Le rôle du rein pour la régulation de la pression artérielle est modéré ; l’essentiel de son action est de maintenir constante la filtration glomérulaire.
Dans le cas d’une hémorragie aigue, on observe successivement : une hypovolémie, une chute d’environ 30% de la pression artérielle, puis une baisse d’environ 30% du DSR mais seulement 20% de baisse du DFG.
IV Physiologie du tubule.
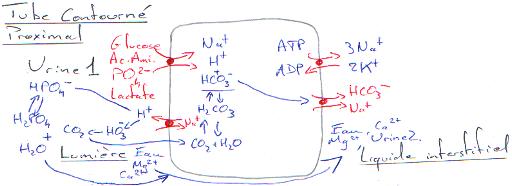
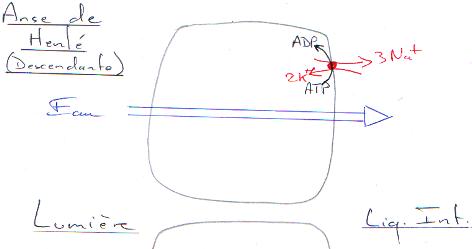
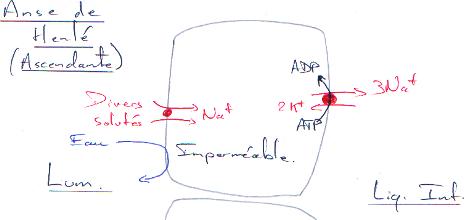
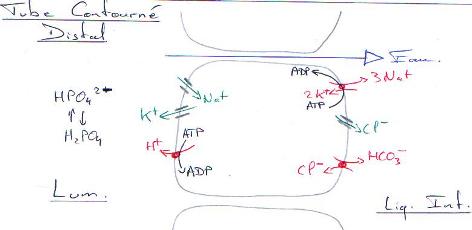
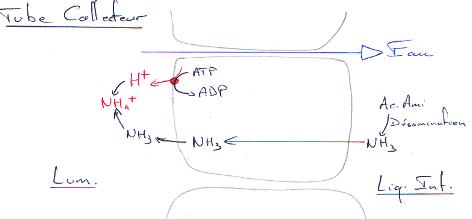
Dans les cellules, on va distinguer deux niveaux :
- Membrane apicale : placée du coté de la lumière du tube, avec beaucoup de jonctions.
- Membrane baso-latérale : coté liquide interstitiel.
On distingue deux types de passage :
- Trans-cellulaire : où il faut traverser la cellule.
Ce transport est lié à un gradient actif de sodium. On le trouve dans le tube proximal, la branche ascendante, large de Henlé, et le tube contourné distal.
- Paracellullaire : entre deux cellules voisines.
Dans ce cas, on a un flux d’eau qui emprunte les passages entre les cellules. On trouve ce passage au niveau du tube contourné proximal, du tube contourné distal et du tube collecteur.
Le tubule proximal est le siège d’une réabsorption intense. Le gradient de sodium dans les tubules proximaux est déterminant dans les mécanismes de réabsorption.
La pompe Na/K – ATPase de la membrane exporte activement le sodium dans le liquide interstitiel. Le gradient intracellulaire provoque l’entrée passive de sodium.
V Gradient osmolaire de concentration à contre-courant cortico-médullaire.
Ce gradient est possible dans la anse de Henlé et uniquement dans les néphrons profonds et juxta-glomérulaires ; ce qui correspond à 20% des néphrons chez l’Homme.
Le rein est irrigué par 1.25 litre par minute. Les éléments figurés de sont pas concernés. On a 700mL de plasma et 20% du plasma est filtré par les glomérules : soit, 125mL au total.
A Au niveau des tubules.
1 Le tube contourné proximal.
Ici, la réabsorption est intense : 100% du glucose et du potassium (K). Pour le sodium (Na), l’eau et le bicarbonate, la réabsorption est d’environ 85%. Le phénomène de réabsorption d’eau est OBLIGATOIRE.
2 La anse de Henlé.
On trouve ici un système à contre-courant (branches ascendante/descendante) mais surtout un sens de mouvement du filtrat et un sens de mouvement du sang des vasa recta.
Il y a réabsorption active du sodium (Na) qui va permettre la réabsorption de l’eau.
3 Le tube contourné distal.
A ce niveau, du sodium est réabsorbé. Des ions K+ et des ions NH4+ vont être sécrétés.
4 Le tube collecteur.
Ici, la réabsorption d’eau est possible grâce à l’action de l’ADH qui permet de concentrer l’urine.
B Fonctionnement des branches de la anse de Henlé.
La branche ascendante, dans sa partie fine est imperméable à l’eau et n’est le siège d’aucun mécanisme actif : les solutés diffusent selon le gradient (du filtrat vers l’interstitium pour le Na+ et l’inverse pour l’urée).
L’absorption de Na+ constitue l’effet élémentaire du gradient d’osmolarité entre le tubule ascendant et l’interstitium.
La branche descendante est très largement perméable à l’eau. Cette perméabilité permet un rééquilibrage osmotique entre le filtrat descendant et l’interstitium.
Ainsi, à la fin de la anse, l’osmolarité est la même dans l’espace intercellulaire, soit environ 1400mOsl/L (valeur maximale pour l’Homme).
Cette concentration progressive du filtrat entraîne son alcalinisation le long de la branche descendante : l’ion HCO3- diffuse mal alors que le CO2 est très diffusible.
Le filtrat tubulaire a son pH qui passe de 6,8 à 7,4 è On assiste donc à la transformation d’une partie du NH4+ en NH3 qui est facilement diffusible et qui s’accumule dans la zone médullaire interne. Cette concentration en NH3 est estimée comme étant 12 à 20 fois supérieure à celle de la zone corticale
 On est en présence d’un gradient d’ammoniac.
On est en présence d’un gradient d’ammoniac.
C Les mécanismes multiplicateurs à contre-courant.
1 Le moteur de la création du gradient est donc :
- La réabsorption du Na+ le long de la branche ascendante de façon active dans sa partie large et passive dans la partie fine.
- La diffusion de l’urée de long du tube collecteur.
La dynamique de circulation de filtrat et la disposition à contre-courant des deux branches aboutissent à une multiplication progressive de l’écart des concentrations en soluté entre le cortex et la médullaire. Il en résulte :
 l’installation d’un gradient de concentration proprement dit (300 à 1400)
l’installation d’un gradient de concentration proprement dit (300 à 1400)  Mécanisme amplificateur ;
Mécanisme amplificateur ;
 le filtrat issu du tube contourné proximal est en équilibre osmotique avec le plasma (300) alors que le filtrat du tube contourné distal est hypotonique (100)
le filtrat issu du tube contourné proximal est en équilibre osmotique avec le plasma (300) alors que le filtrat du tube contourné distal est hypotonique (100)
2 Entretien du gradient osmotique cortico-médullaire.
Le maintien de ce gradient est assuré par l’action de deux mécanismes :
- la disposition antiparallèle des vasa recta avec les deux branches de l’anse de Henlé ;
- le débit sanguin dans les vasa recta est faible à cause de la forte résistance vasculaire de l’artériole efférente glomérulaire. Cette diminution du débit sanguin améliore les échanges entre le plasma et l’interstitium et porte ainsi le gradient cortico-médullaire à sa valeur maximale.
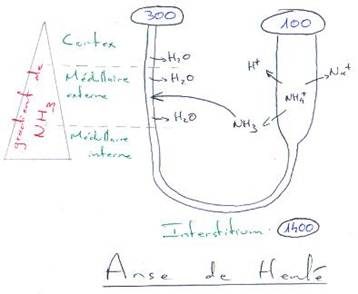
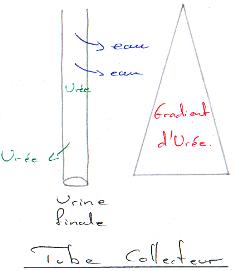
D Le glucose et le rein ou Glycémie et glycosurie.
La concentration en glucose du plasma est de l’ordre de 0,8g/L, soit 4,44 à 5,55 mMole/L, dans des conditions physiologiques normales, avec une élimination urinaire nulle pour le glucose.
Si l’on réalise une injection de glucose en intraveineuse, du glucose va apparaître dans les urines : c’est la glycosurie.
Le seuil où apparaît la glycosurie est atteint pour 14 mMole/L (ou 2,5 g/L). Cela signifie que la réabsorption du glucose dans le tube contourné proximal est contrôlée et qu’il y a réabsorption jusqu’à ce seuil de 2,5 g/L. Au-delà de cette valeur, le glucose est excrété dans l’urine.
1 Notion de taux maximal de glucose (= TmG).
Le débit de réabsorption de glucose augmente jusqu’à une valeur de 22mMole/L, soit 4 g/L. Ensuite, il y a stabilisation à cette valeur maximale. Cette valeur est appelée TmG : elle est très constante et est d’environ 2mMole/min.
Cela s’explique par une saturation des protéines du cotransport Na+/Glucose au niveau de la membrane apicale des cellules du tube contourné proximal.
2 Epaulement.
La glycosurie apparaît souvent quand le débit de réabsorption n’atteint pas sa valeur maximale.
Cela peut s’expliquer soit par des propriétés intrinsèques aux protéines de cotransport Na+/glucose ; soit par une diversité du TmG entre les néphrons. De cette façon, les courbes de réabsorption et de sécrétion sont arrondies (on parle aussi d’épaulement).
Chapitre 5 :
Eléments de physiologie comparée,
L’excrétion chez les poissons, oiseaux et quelques mammifères adaptés.
I Osmorégulation chez les animaux.
L’osmorégulation est le mécanisme d’équilibration vis-à-vis de l’eau et des sels.
A Le milieu aquatique.
1 Le milieu marin.
a Généralités.
L’eau de mer a une osmolarité comprise entre 1000 et 1100 mOsmol, soit 3,3 fois plus que chez l’animal.
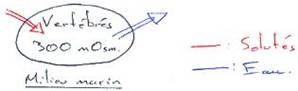
b Vertébrés marins.
α La myxine.
On trouve la même osmolarité entre le liquide extracellulaire de l’animal et l’eau de mer. La myxine a donc les mêmes mécanismes osmorégulateurs que les invertébrés marins.
β Les sélaciens.
Le milieu intérieur est à 300 MAIS avec de l’urée, ce qui donne environ 1000.

L’urée est très concentrée car il y a réabsorption active par le rein. Les solutés pénètrent dans l’animal par l’eau et les aliments, mais aussi par les branchies.
Les solutés en excès sont rejetés avec l’urine (par les reins) mais aussi par, les glandes rectales et les branchies.
γ Téléostéens marins.

On observe chez ces animaux de grandes déperditions d’eau par les branchies, par la peau (tégument) et par les reins, car il y a production d’une urine HYPOtonique.
On note aussi le fait que les solutés tels que Na+, Cl- et SO42- sont rejetés par les branchies et la peau.
Ces animaux doivent boire beaucoup d’eau de mer : 0,3 mL à 2mL/heure pour 100g de poids.
c Adaptation à l’environnement marin.
C’est le cas des vertébrés aériens qui présentent une adaptation à l’environnement aérien, puis « liquide ».
Il n’y a pas de branchies. Il va y avoir des pertes d’eau et une consommation d’aliments surtout riches en sels.
α Reptiles et oiseaux marins.
Les reins de tortue de mer et des autres reptiles marins ne peuvent élaborer une urine hypertonique au plasma, alors que les reins des oiseaux marins peuvent produire une urine à 700-800mOsm, ce qui reste toutefois insuffisant pour l’équilibre hydrominéral.
Dans les deux cas, on va retrouver des structures céphaliques spécialisées (glandes à sel) dont les conduits excréteurs débouchent dans des cavités à différents niveaux (orbitaires, nasales, buccales… selon les espèces). Ces structures élaborent une sécrétion d’osmolarité supérieure à celle de l’eau de mer (2000mOsm pour les albatros).
Ces glandes ont une activité intermittente. Elles émettent leurs sécrétions, uniquement après un accroissement de l’osmolarité du milieu interne. Leur efficacité d’élimination des sels est très supérieure à celle des reins de mammifères. Elles sont contrôlées par les surrénales et le système nerveux parasympathique.
β Les mammifères marins.
Les cétacés (baleines, dauphins) mais aussi d’autres groupes, comme les phoques ou les morses s’adaptent en émettant une urine plus concentrée que l’eau de mer (environ à 1500mOsm). Cela leur permet d’éliminer les ions en limitant la perte d’eau.
Remarque sur l’adaptation des poissons furyhalins (anguilles) :
Ces animaux passent de l’eau de mer à l’eau douce et inversement. Quand il y a changement de milieu, il va y avoir inversion du flux osmotique et des flux d’ions échangés au niveau des branchies. L’hypothèse retenue pour le fonctionnement est une sécrétion d’adrénaline qui serait un des facteurs responsables de ces modifications de perméabilité.
2 Le milieu d’eau douce.
a Généralités.
L’osmolarité de l’eau douce varie de 0,1 à 10, ce qui est donc très inférieur à l’osmolarité des êtres vivants. Les flux qui auront tendance à s’installer sont : un flux entrant d’eau ; un flux sortant de solutés.
Un organisme vivant, dans un tel milieu, doit compenser cette entrée d’eau et la perte de solutés.
b Vertébrés d’eau douce.
α Poissons téléostéens.

L’eau pénètre dans l’organisme par les branchies et la peau (essentiellement). Seule une faible quantité d’eau peut pénétrer par le tube digestif car ces poissons boivent peu.
L’eau va être éliminée par le rein avec une urine abondante mais très diluée : on arrive à 30g d’eau éliminée pour 100g de poids corporel, le tout par 24 heures.
La perte de solutés par les branchies et l’urine est compensée par une réabsorption active due aux cellules à chlore.
β Les amphibiens.
La plupart des amphibiens sont aquatiques ou dépendent étroitement de ce milieu (ponte et développement des têtards). Dans l’eau les batraciens sont soumis (comme les poissons d’eau douce) à un efflux entrant d’eau par la peau.
La perméabilité osmotique à l’eau serait modulée par l’ADH.
Ces animaux éliminent l’eau en synthétisant une urine très diluée (par rapport au milieu intérieur). La perte de solutés est compensée par une absorption active d’ions au niveau de la peau.
Ce groupe fait la transition avec les animaux terrestres.
B Le milieu terrestre.
1 Généralités.
Les animaux terrestres accèdent à l’O2 mais sont soumis à une déshydratation permanente, par évaporation des téguments (si perméables à l’eau) et par les poumons.
Il y a diverses adaptations se rencontrant et formant un continuum, des animaux très dépendants de l’eau (amphibiens terrestres des régions tempérées) jusqu’aux animaux qui se passent totalement d’eau (Rat kangourou).
2 Les amphibiens terrestres.
Leur peau est le siège d’échanges permanents, ce qui entraîne la dépendance vis-à-vis de l’eau. Ils ne boivent pas mais contrôlent leur production d’urine dès qu’ils sont hors de l’eau. La plupart des espèces réabsorbent même l’eau urinaire qui sert de réserves hydriques en milieu terrestre.
Des espèces vivent en contrés désertiques et sont capables de stocker le 1/3 de leur poids total en eau urinaire. Ces espèces vivent dans des terriers profonds et profitent de l’humidité de l’environnement en absorbant l’eau du sol à travers la peau (imbibition).
3 Les vertébrés terrestres.
a Les reptiles.
Les reptiles perdent l’eau de trois façons :
- par les téguments (la majeure partie)
- par la respiration
- par l’urine (pourcentage infime car l’urine est très concentrée).
Cependant, ces animaux montrent une grande résistance à la dessiccation. Leurs sources d’eau sont, les boissons, les aliments, l’eau métabolique.
b Les oiseaux et mammifères.
Oiseaux et mammifères sont des endothermes, ce qui est une de leur contrainte physique majeure : contrôler la température interne, ce qui fait appel à des mouvements d’eau et qui complique la régulation d’osmolarité du milieu intérieur. Les pertes d’eau peuvent être modulées par transpiration ou par polypnée thermique.
Le rein contrôle l’excrétion azotée et l’élimination de solutés minéraux.
Il y a des adaptations remarquables à des environnements très pauvres en eau, où l’animal va être amené à se passer d’eau : le rat kangourou (Dipodomys spectabilis). Il couvre ses besoins en eau avec celle contenue dans les graines (moins de 10% d’eau !!!) et avec l’eau métabolique. Dans cette adaptation, l’animal émet une urine très hypertonique (5500mOsmol). Certains rongeurs australiens ont une osmolarité de 9000mOsmol.
Conclusion :
Ces mécanismes sont des adaptations selon les milieux de vie à On voit différentes stratégies de maintien de l’équilibre hydrominéral.
Bilan hydrique : comparaison entre les entrées et les sorties d’eau.
Entrées : Eau de boisson à 1.5L * ; eau des aliments + eau métabolique à 1,5L
1g de glucose métabolisé à 0,6g d’eau
1g d’amidon à 0,54g d’eau
1g de lipides à 1,07g d’eau
1g de protéine à 0,39g d’eau si le produit terminal est de l’urée
1g de protéine à 0,5g d’eau si le produit terminal est de l’acide urique
Sorties : Urine à 1,5L * ; peau (perspiration et sueurs) + selles (1/3L) + poumons à 1,5L
* = compartiment réglable.
II L’excrétion azotée.
A Généralités.
La régulation du métabolisme hydrominéral implique des pertes d’eau plus ou moins importantes. Le métabolisme oxydatif des glucides et des lipides produit de l’eau.
Le métabolisme des protéines et des acides nucléiques fournit des substances azotées à éliminer comme l’ammoniac, l’urée, l’acide urique.
Chez l’Homme et les vertébrés terrestres, il y a de l’ammoniac éliminé dans les urines, mais cette fraction ne vient pas du catabolisme des protéines. Ici, l’ammoniac est utilisé pour tamponner les excès en ions H+.
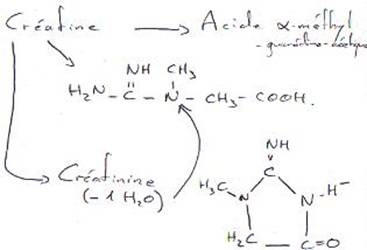
On trouve d’autres molécules, mais moins importantes :
- La créatinine : elle est endogène, émise par le rein, liée au métabolisme cellulaire et vient de la créatine.
- L’acide hippurique.
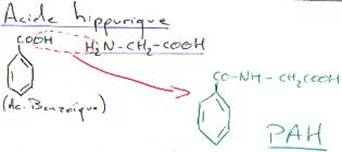
La clairance rénale : inuline – DFG (125mL/min) ; PAH – DPR 700mL/min.
L’élimination d’un gramme d’azote sous forme d’ammoniac (NH3) équivaut à éliminer 500mL d’eau ; 50mL sous forme d’urée et 10mL sous forme d’acide urique.
B L’ammoniac, NH3.
C’est une molécule très petite, soluble dans l’eau, et qui diffuse dans tous les compartiments liquidiens.
Les animaux éliminant l’azote sous cette forme sous dits : ammoniotéliques.
Ce sont surtout des animaux aquatiques, avec une grande surface de contact avec l’eau.
Certains dipneustes, têtards et crocodiles sont dans ce cas.
C L’urée (CH4ON2).
Les animaux qui éliminent l’urée sont des uréotéliques.
L’uréotélie existe chez les animaux qui possèdent le cycle de l’urée (cycle de Krebs-Henseleight).
C’est le déchet majeur des organismes terrestres, synthétisé par le foie, et éliminée par le rein (comme constituant urinaire).
C’est le cas chez les poissons cartilagineux et autres dipneustes ou des amphibiens adultes et bien sur, les mammifères.
D L’acide urique.
Cet acide est très peu soluble dans l’eau. Il précipite en cristaux d’urate. Les animaux qui le produisent sont dits uricotéliques (uricotélie).
L’acide urique domine chez les animaux à problème importants en eau (milieu sec) ou avec des problèmes de poids (pour le vol) : c’est le cas des reptiles et des oiseaux. Ces derniers ont les fientes qui s’accumulent dans un cloaque.
E Conclusion.
Le clivage en ces trois catégories soit être nuancé car il n’est pas strict et il y a le plus souvent présence de deux composés azotés dans l’urine.
- Ammonio-uréotèles : NH3 + urée (écrevisse, dipneuste).
- Uréo-uricotèles : exemple, l’Homme, avec 15 à 25g d’urée par litre contre 0,5g d’acide urique (par litre).
- Ammonio-uricotèles : NH3 + Acide urique (crocodiles).
TD (n°2) :
La flore Digestive chez l’Homme.
100 milliards de bactéries réparties en 400 espèces différentes. Cela donne une biomasse considérable qui se traduit par la production d’enzymes et de métabolites in vivo.
C’est un écosystème intégré avec des interactions.
I Répartition.
On a une variabilité selon : les segments (étages) du tube digestif, la teneur du milieu en O2, les sécrétions du tube digestif, les nutriments disponibles, la vitesse de transit (rapide jusqu’au caecum, puis ralentie).
Globalement, on a un gradient oral/aboral.
La bouche présente peu de flore qui est peu active car le temps buccal est court.
L’estomac a une flore faible adaptée à un pH très bas (moins de 10^3)
L’intestin grêle présente une variabilité quantitative (duodénum : 10 3 ; jéjunum : 10 4 à 10 6 ; iléon : 10 6 à 10  et une variabilité qualitative par la diminution progressive des bactéries aérobies au profit des bactéries anaérobies strictes.
et une variabilité qualitative par la diminution progressive des bactéries aérobies au profit des bactéries anaérobies strictes.
Le colon est un milieu où le contenu est ralenti : il y a une stase et une augmentation de la population bactérienne (10 9 à 10 11). C’est une « chambre de fermentation ». Il est le siège de biotransformation des aliments non assimilés par l’intestin. Cette zone est colonisée de façon permanente. La flore anaérobie est dense, active et produit de nombreux métabolites.
Ces bactéries sont xénobiotiques, responsables d’une stimulation non spécifique du système immunitaire.
La stase du contenu n’explique pas à elle seule, l’importance de cette flore. Des bactéries ont une capacité d’adhésion aux mucines, aux cellules choliques par des liaisons spécifiques : les adhésines.
II Composition classique.
Cette flore est difficile à quantifier et les résultats sont variables à cause de plusieurs facteurs : mode de prélèvement, méthode microbiologique, présence de bactéries d’origine alimentaire, physiologie intestinale, contexte environnemental de l’hôte selon son régime alimentaire, les bactéries exogènes et les substrats antibiotiques.
L’intestin grêle :
Les bactéries de ce segment appartiennent au genre Lactobacillus et Streptococcus. De plus, quelques espèces de la famille des Entérobactériaceae sont présentes.
Le colon :
On trouve quatre types de flore :
- une flore dominante : exclusivement anaérobie, Eubactérium, Clostridium, Propionylbacterium, Bifidobacterium.
- Une sous-dominante : on a diverses espèces de la famille des Enterobacteriaceae (E. coli) et les genres Lactobacillus, Streptococcus et Enterococcus.
- Une résiduelle : les bactéries en transit ou réprimées par la flore dominante.
- Une fécale, avec de nombreuses espèces mortes. La flore n’est pas représentative des diverses « niches écologiques » de l’écosystème digestif.
Les flores sont étudiées pour retrouver des souches pathogènes ou potentiellement pathogènes pour l’Homme.
III Les rôles de la flore intestinale.
A Effets digestifs.
Des modifications anatomiques et histologiques vont être liées à la présence de la microflore et qui sont mises en évidence par comparaison d’un animal sans germe avec un animal normal.
Une augmentation de la flore entraîne un ralentissement du transit et une dilatation du caecum.
La vitesse de renouvellement cellulaire (index mitotique) est réduite chez l’animal axénique.
B Effets nutritionnels.
1 Effets bénéfiques pour l’hôte.
Il va y avoir production d’acides gras à chaîne courte qui diminue la synthèse hépatique du cholestérol. On trouve aussi la dégradation des glucides non absorbés (amidon, pectine, cellulose) qui entraîne la production d’acides organiques assimilables par l’hôte (acétate, butyrate, propionate) et de gaz (CO2 et H2).
L’hydrolyse des lipides alimentaires non absorbés se fait grâce aux lipases bactériennes.
La dégradation de certaines protéines en acides aminés permet la récupération d’azote.
Il peut également y avoir des apports vitaminiques grâce à certaines bactéries capables de synthétiser, in vitro, un large éventail de vitamines (riboflavine β2, acide pantothénique β5, pyridoxine B6, Biotine B8, vitamine K).
Des bactéries anaérobies strictes, comme Clostridium butyricum, sont capables de synthétiser de la vitamine B12 qui est d’une grande utilité pour la croissance locale des bactéries.
Les gaz intestinaux sont le résultat de fermentation microbienne dans le gros intestin à partir des glucides et des protéines arrivant à ce niveau. Il s’agit de traces comparées aux ruminants.
2 Effets néfastes pour l’hôte.
Les cotés néfastes touchent généralement le métabolisme :
- Métabolisme glucidique et apparition de composés aglycones (dérivés des glucoronides qui sont cancérigènes)
- Métabolisme azoté : les nitrates et amines donnent des composés cancérogènes à les nitrosamines.
- Métabolisme xénobiotique avec possibilité d’inactivation de médicaments ou production de métabolites toxiques.
3 effets divers.
La flore résidente a un effet de barrière vis-à-vis des bactéries exogènes : il y a élimination totale (effet drastique) ou maintien à l’état de sous dominance (effet permissif).
La flore stimule l’immunité locale et maintien le statut immunitaire à un certain niveau.
IV Conclusion.
Quelles que soient les techniques d’étude, on constate que la flore reste stable.
Il faudrait éviter les agressions (jeûne alimentaire, modification brutale de régime, modification péristaltique, antibiothérapie).
La flore est un écosystème complexe et doit être protégée.